Ano: 2013 Vol. 79 Ed. 6 - Novembro - Dezembro - (5º)
Seção: Artigo Original
Páginas: 673 a 680
Correlação entre sintomas e tempo de evolução do câncer do trato aerodigestivo superior com o estádio inicial e avançado
Correlation between symptoms and course duration of upper aerodigestive tract cancer at early and advanced stages
Autor(es): Francis Balduino Guimarães Santos1; Jose Jacinto Branco Vasconcelos-Raposo2; Maria do Carmo Tolentino Figueiredo3
DOI: 10.5935/1808-8694.20130125
Palavras-chave: diagnóstico tardio; evolução clínica; neoplasias de cabeça e pescoço; prevenção primária; sinais e sintomas.
Keywords: clinical course; late diagnosis; neoplasms of the head and neck; primary prevention; signs and symptoms.
Resumo:
Muitos dos aspectos clínicos e biológicos da história natural do câncer do trato aerodigestivo superior estão por elucidar, o que no Brasil tem como consequência direta a falha sistemática das campanhas de prevenção e de diagnóstico precoce.
OBJETIVO: Analisar os sinais e sintomas apresentados por portadores da doença em estadiamentos iniciais e avançados. Outras variáveis como o tempo de evolução da doença, o estado geral e nutricional foram consideradas.
MÉTODO: Estudo de coorte histórica com corte transversal em 895 indivíduos portadores do câncer do trato aerodigestivo superior.
RESULTADOS: Os sinais e sintomas encontrados não se correlacionaram de forma estatisticamente significativa com o tempo de evolução da doença nem com a doença em fases iniciais, mas evidenciaram um desenvolvimento rápido da doença.
CONCLUSÃO: Os resultados sugerem uma doença de início insidioso nas fases iniciais e de rápida evolução. O tempo longo de evolução - maior que três meses, associou-se às pioras nos estados geral e nutricional dos pacientes.
Abstract:
There still are many clinical and biological aspects of the natural history of cancer of the upper aerodigestive tract to be unveiled; which in Brazil is a direct consequence of the failure of systematic prevention and early diagnosis campaigns.
OBJECTIVE: To analyze the signs and symptoms presented by patients with the disease at initial and advanced stages. Other variables such as disease duration, general and nutritional status were considered.
METHOD: A historical cohort study with a cross-section involving 895 subjects with cancer of the upper aerodigestive tract.
RESULTS: Clinical findings were not statistically correlated with disease progression, nor with the disease in early stages, but it showed rapid disease development.
CONCLUSION: The results suggest a disease of insidious onset in the early stages and fast course afterwards. The long disease duration - greater than three months, was associated with worsening in general and nutritional states of patients.
![]()
INTRODUÇÃO
O câncer de localização na cabeça e pescoço é a sexta maior prevalência de neoplasias malignas primárias no mundo, responde por 5% de todos os cânceres no homem, 2,5% nas mulheres1 e apresenta-se com importância epidemiológica em vários países do mundo, dentre eles o Brasil2,3.
O sítio anatômico mais acometido pelo câncer na cabeça e pescoço é o do trato aerodigestivo superior, distribuído entre a cavidade oral (35%-40%), orofaringe (30%), laringe (25%) e hipofaringe (7%)4. O tipo histológico mais prevalente do câncer localizado no trato aerodigestivo superior é o Carcinoma de Células Escamosas (CETADS) em 90% dos casos, sendo os principais fatores etiológicos o consumo do tabaco e das bebidas alcoólicas5-7, embora a infecção pelo papiloma vírus humano (HPV) tenha sido responsabilizada por pelo menos 10% a 30% dos cânceres da orofaringe8.
O fator prognóstico mais importante para a sobrevida é o estadiamento clínico ao momento do diagnóstico, mas este se encontra avançado em torno de 75% dos casos, especialmente nos países em desenvolvimento. Como consequência disto, cerca de 40% a 60% dos portadores de CETADS apresentam recidiva locorregional e 20% a 30% evoluem com metástases à distância8. Após o tratamento, a mortalidade global situa-se em torno de 40% a 60% nos países desenvolvidos, com média mundial em torno dos 46%9. Os motivos descritos na literatura para justificar essa elevada incidência em fases avançadas distribuem-se numa miscelânea de situações: fatores culturais e econômicos, pobre suporte social, estilos de vida, aspectos demográficos e geográficos, assim como dificuldade de acesso ao serviço de saúde10-13. Não há consenso pela literatura atual no que tange às barreiras para o diagnóstico precoce do CETADS.
Estudos realizados no Brasil evidenciam que a população desconhece os fatores de risco associados a estes cânceres14,15. Em parte, isto se deve aos baixos índices de escolaridade e rendimento per capita por agregado familiar16,17. Outro estudo sugere que o diagnóstico precoce do CETADS talvez seja dificultado pelo fato de que as lesões iniciais, com poucos sintomas, não sejam valorizadas quer pelo indivíduo quer pelos profissionais de saúde12. Sugerem, ainda, que esses sintomas possam ser confundidos com outros que tipificam doenças comuns à população. Mais ainda quando esses sintomas nunca lhes foram apresentados como sendo denunciantes de câncer18,19. Concepções modernas de saúde alicerçam-se na corresponsabilização do indivíduo pelo seu estado de saúde20.
No Brasil, ocorrem campanhas pontuais contra o CETADS nos sítios da cavidade oral ou laringe e estas, em sua maioria, têm se mostrado altamente ineficazes, sugerindo a necessidade de maior elucidação dos processos biológicos e epidemiológicos destes tipos de cânceres15,16,21, daí que o achado da lesão cancerizável continue a ser a forma mais eficaz de intervenção clínica com sucesso22,23. Em termos de pesquisa, muita ênfase tem sido dada aos fatores de risco e suas relações causais e menos se tem feito sobre a sua história clínica natural.
Por fim, a doença continua a ser desafiadora pelo diagnóstico em estádio avançado, pela elevada morbimortalidade24 e, consequentemente, pelo impacto negativo ao erário. Poucos são os estudos correlacionais entre os vários sintomas, o estadiamento clínico e o tempo de evolução com vistas ao diagnóstico inicial da doença, uma vez que podem auxiliar na compreensão do comportamento humano nas diversas regiões do mundo e delinear um perfil epidemiológico com ações de saúde específicas à determinada população exposta aos fatores de risco.
O CETADS pode ser apresentado como doenças distintas segundo os quatro sítios anatômicos e uma visão tradicionalmente centrada no especialista ou ser apresentado como doença única25,26. Nesta abordagem, há um forte incremento em sua incidência, levando em consideração semelhantes aspectos epidemiológicos e podem-se confluir ações de saúde conjuntas com redução de custos - visão focada na saúde pública. Com ambas as abordagens, o presente estudo tem como "objetivo geral" descrever as características sociodemográficas, comportamentais e clínicas da amostra. Os "objetivos secundários" são associar o tempo de evolução do CETADS ao estadiamento em fases iniciais e avançadas, bem como estabelecer a relação temporal dos sinais/sintomas com o estado geral e nutricional apresentado pelos pacientes ao momento do diagnóstico.
MÉTODO
Estudo de coorte histórica com corte transversal - segue as mesmas características da coorte histórica longitudinal, porém, estabelece um momento temporal restrito (corte) para a avaliação dos elementos estudados, não havendo seguimento no decorrer do tempo. Foram selecionados para o estudo 895 pacientes portadores de CETADS, entre o período de março de 1996 a janeiro de 2009, atendidos pelos serviços de cirurgia de cabeça e pescoço localizados no município de Montes Claros/Minas Gerais - Brasil. Foram utilizados prontuários padronizados de um único especialista. O presente estudo foi aprovado (Resolução 131 - CEPEX/2008, Conselho de Ética sob o parecer 005/2008) e não recebeu financiamento para a sua realização. As variáveis utilizadas encontram-se descritas a seguir.
Sociodemográficas (gênero, estado civil, grupo etário, procedência e profissão) e hábitos de vida deletérios à saúde, como fumar e beber bebidas alcoólicas, além das variáveis clínicas a seguir: sítios e subsítios anatômicos conforme a Classificação Internacional de Doenças (ICD, 10ª ed., 2000)27 a saber: cavidade oral, orofaringe, laringe e hipofaringe. O critério de estadiamento utilizado obedeceu ao sistema TNM da União Internacional Contra o Câncer (TNM-UICC, 6ª ed., 2002)28. Pacientes com datas anteriores a 2002 tiveram os seus estadiamentos atualizados conforme as regras do TNM em uso corrente. O tempo de evolução da doença foi considerado como aquele relatado pelo paciente (delay's patient), entre as datas dos primeiros sintomas até a primeira consulta com o especialista em cirurgia de cabeça e pescoço (curto < 3 meses; longo > 3 meses). O estado nutricional foi avaliado conforme a avaliação global subjetiva do estado nutricional29,30, considerando o relato da perda de peso pelo paciente, pelo peso atual do paciente, pelas características clínicas e físicas apresentadas pelo paciente ou pela associação destas informações. O estado geral de saúde foi avaliado pela classificação clínica do Performance Status de Zubrod-Karnofsk31 apresentada pelos pacientes.
Foram calculadas as frequências, médias e as razões de probabilidades para verificar possíveis associações entre as variáveis investigadas. Foi usado o Statistical Package for the Social Science (SPSS, V. 19®). Inicialmente, foi realizada uma análise descritiva dos dados. Posteriormente, pela natureza das variáveis recorremos aos testes não paramétricos, a uma análise bivariada (teste do χ2, Mann-Whitney) e multivariada dos dados (regressão logística binária). O nível de significância de 5% foi mantido para os procedimentos estatísticos efetuados (p = 0,05*).
RESULTADOS
As condições mais frequentemente encontradas foram o sexo masculino (84,8%) numa proporção 5,6 ♂:1 ♀. A idade variou de 7 a 92 anos de idade, com média de 59,6 anos e picos de incidência entre a 5ª (28,6%) e 6ª (24,8%) décadas de vida. Foi encontrada maior frequência de tabagista/ex-tabagistas (91,5%) e de etilista/ex-etilistas (86,4%). Quanto à cor da pele, ficou assim distribuído: leucoderma 227 (30,6%), feoderma 417 (56,1%) e melanoderma 99 (13,3%). Quanto ao estado civil, os casados (as) representaram 64,8% (449), solteiro (as) 17,3% (120), viúvo (as) 12% (83), separado (as) 4% (28) e outros 1,9% (13).
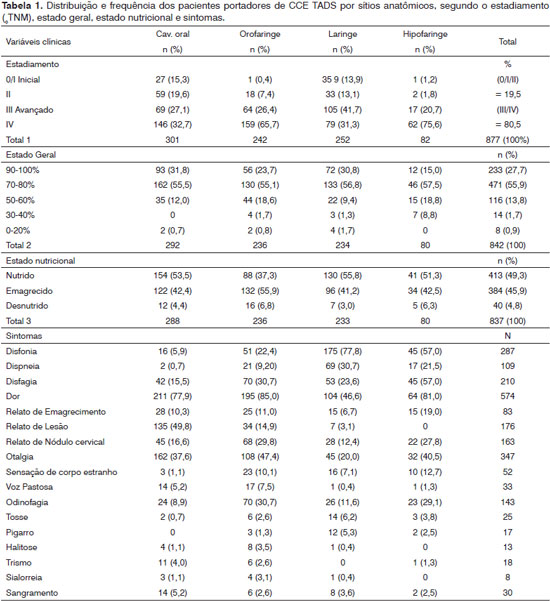
Os sítios anatômicos acometidos distribuíram-se da seguinte maneira: cavidade oral (33,9%), laringe (28,8%), orofaringe (27,9%), e hipofaringe (9,4%) - Tabela 1. Observam-se também, nesta tabela, os subsítios mais acometidos. Considerando-se todos os sítios anatômicos, o estadiamento clínico ao diagnóstico mostrou-se avançados em 80,5% dos pacientes. O sítio anatômico pelo qual a doença mostrou-se mais avançada em estádios III/IV foi na hipofaringe com 96,3% - Tabela 1.
Considerando o estado nutricional, 52,1% dos pacientes encontravam-se emagrecidos ou desnutridos ao diagnóstico e, quanto ao estado geral, 55,9% com repercussão leve a moderada - Tabela 1.
Os sintomas foram observados sob dois aspectos: isoladamente para cada sítio anatômico e em conjunto - considerando neste o CETADS como doença única. Na primeira, e conforme o esperado, os sintomas mais frequentes distribuíram-se de formas distintas para cada sítio anatômico. Para a cavidade oral, os três principais sintomas ocorreram por ordem de frequência da seguinte maneira: a dor, o relato da lesão pelo paciente e a otalgia. Para a orofaringe, ficou assim distribuído: a dor, a disfagia e a odinofagia. Para a laringe, foram a disfonia, a dor e a dispneia e, para a hipofaringe, a dor, a disfagia e a disfonia.
De outra maneira, ao considerarem-se todos os sítios anatômicos juntos, algumas diferenças já são notadas e o sintoma mais prevalente da amostra é representado pela dor tumoral (71,5%). Esta foi seguida pela otalgia reflexa, disfonia, disfagia, relato da lesão, relato pelo paciente do nódulo em pescoço e da dispneia - Tabela 1.
Após considerar as diferenças do comportamento clínico (sinais e sintomas) do CETADS obtidas pela avaliação separada e conjunta dos sítios anatômicos, pode-se observar a associação desses com o estadiamento inicial e avançado.
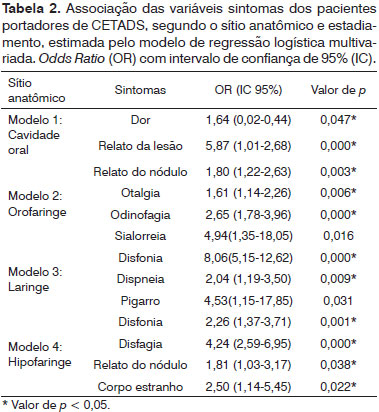
Considerando novamente os sítios anatômicos em separado, por meio de uma regressão logística multivarada entre estadiamento, sítio anatômico e os sintomas, os resultados mostram associações estatisticamente significativas para a doença avançada. Foram estatisticamente significativos na cavidade oral a dor e o relato da lesão pelo paciente; na orofaringe, o relato do nódulo pelo paciente, a otalgia e a sialorreia; na laringe a disfonia, o pigarro e a dispneia; e na hipofaringe a disfonia, a disfagia, o relato do nódulo pelo paciente e a sensação de corpo estranho - Tabela 2.
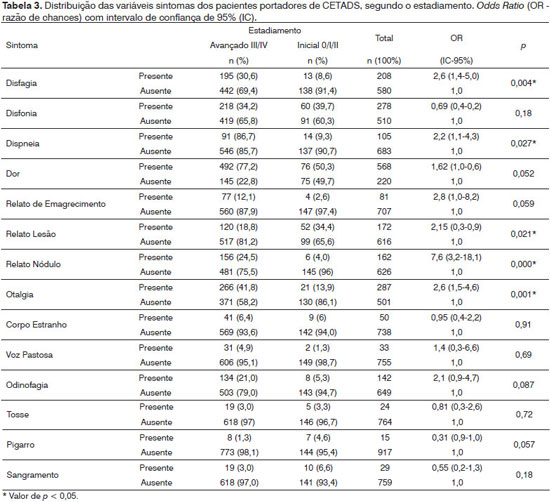
Considerando agora os sítios anatômicos em con-junto, por meio da distribuição dos sintomas segundo o estadiamento, foram obtidas associações estatisticamente significativas dos sintomas com o estadiamento avançado, sendo esses o relato do nódulo, a otalgia, a disfagia, relato da lesão e a dispneia - Tabela 3.
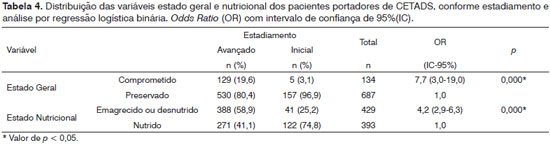
Associações estatisticamente significativas foram encontradas entre o estadiamento em fase avançada da doença com as variáveis estado geral e nutricional - Tabela 4.
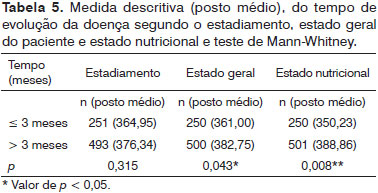
Não se observou associação entre o tempo de evolução da doença e o seu estadiamento. Não foi encontrada diferença estatisticamente significativa entre o tempo de evolução da doença com os estadiamentos iniciais ou avançados. Ao contrário do aventado (H1), o tempo de evolução da doença não se correlacionou com o estadiamento, porém, o tempo de evolução longo (acima de três meses) se correlacionou com as pioras nos estados nutricional e geral dos pacientes - Tabela 5. O tempo das queixas relatadas pelos pacientes (n = 778) variou entre 1 a 60 meses (30 a 1.800 dias), com média de 150 dias (DP = 235,44).
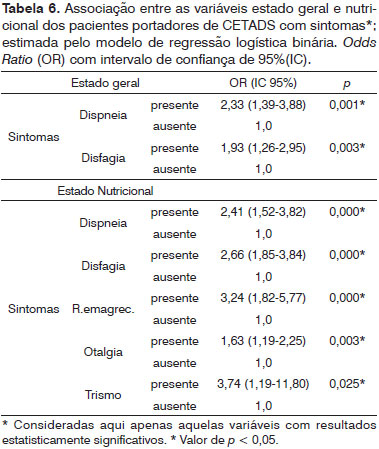
Pode-se observar as variáveis que se correlacionaram com uma piora no estado nutricional apresentada pelos pacientes, tais como a dispneia, a disfagia, o relato de emagrecimento pelo paciente, a otalgia e trismo. De igual forma, a variável estado nutricional se correlacionou com pioras no estado geral apresentado pelos pacientes. Já os sintomas 'disfagia e dispneia' se relacionaram de forma estatisticamente significativa para o comprometimento no estado geral desses - Tabela 6.
DISCUSSÃO
Neste estudo, o perfil epidemiológico dos pacientes portadores de CETADS foi semelhante aos achados pela literatura32-34. Os achados expressivos quanto ao gênero de 5,6 ♂:1 ♀, são em parte justificados por fatores socioculturais, encontrando-se o homem mais exposto aos agentes carcinogênicos para o desenvolvimento do CETADS (fatores de risco: cigarro e bebidas alcoólicas). O estadiamento avançado em 80,5% dos pacientes não destoou daquele encontrado na literatura33,34, mas corrobora para a gravidade no que tange à epidemiologia do CETADS.
A dor, em suas diversas formas, foi o sintoma geral mais prevalente, acometendo 71,5% dos pacientes portadores de CETADS, possivelmente devido ao elevado número de pacientes com doença avançada, semelhante a outro estudo35. É sabido que a dor eleva o grau de sofrimento dos pacientes, com importante redução das horas de sono, levando à queda da capacidade produtiva, faltas ao trabalho e gastos com medicamentos, o que finda numa via crucis por suporte social e atendimento médico. Este fato mostra a importância da dor como um fator de reconhecimento do estado de doente pelos pacientes com CETADS19, mas esta, infelizmente, já prediz uma doença avançada. Tal como a dor, diversos sinais e sintomas se associaram com a doença avançada de maneira estatisticamente significativa, o que não favorece ao prognóstico.
O CETADS o qual foi avaliado por duas abordagens, como doenças diferentes ou como doença única, apresentou informações pouco distintas. A primeira apresentou sintomatologia heterogênea, a qual se distribuiu desigualmente entre os quatro sítios anatômicos, mas não evidenciou nenhum sinal ou sintoma patognomônico a uma ou outra localização. Embora os sítios anatômicos sejam distintos e tenham funções diferentes entre si, a proximidade anatômica desses faz com que os grandes tumores possam acometer mais de um sítio ou subsítio anatômico simultaneamente, produzindo, assim, uma sintomatologia mista. Os sintomas aqui relacionados associaram-se à doença avançada. O CETADS avaliado como doença única apresentou sintomatologia associada à doença avançada tal como o relato do nódulo, a disfagia, o relato da lesão e a dispneia.
É difícil compreender porque o diagnóstico do CETADS não acontece em estadiamento inicial, mas os diversos sintomas associaram-se, em sua maioria, a um estadiamento avançado. Possivelmente, os sintomas iniciais sejam sutis, desvalorizados pelo paciente e a doença evolua progressiva e rapidamente ao estadiamento avançado, não dando, então, chances a um diagnóstico inicial em tempo ágil19.
A população, por outro lado, não tem conhecimento ou condições clínicas para a identificação das lesões iniciais ou cancerizáveis do CETADS12,19,23, achado este essencial para a sua prevenção. A busca ativa por lesões precursoras do CETADS (screening) deve ser repensada para os indivíduos com fatores de risco ao seu desenvolvimento (acima de 45 anos de idade, tabagista e/ou etilista), como já observado por outros estudos com resultados favoráveis35-37. Atualmente, encontra-se disponível uma série de equipamentos médicos para a realização de exames de imagem do trato aerodigestivo superior (videolaringoscopia), que podem ser ofertados à comunidade pela rede pública de saúde, mas com custo-benefício a ser avaliado. A atenção em nível primário e secundário necessitaria de investimentos em estrutura física e em tecnologia para uma adequada atuação na prevenção e no diagnóstico inicial dos CETADS, tal qual foi feito para o câncer do colo uterino38.
Alguns sintomas se associaram de maneira significativa com o declínio físico dos pacientes, tais como a dispneia, a disfagia e o relato de emagrecimento. Indivíduos com restrições mecânicas para respirar e/ou se alimentar, em decorrência do acometimento tumoral, têm o seu estado nutricional comprometido39. Esses sintomas podem ser os maiores responsáveis pelo estado consuptivo da doença e podem interferir desfavoravelmente com o tratamento e com o prognóstico.
O tempo de evolução da doença que se passou entre os primeiros sinais e sintomas até a motivação do paciente a procurar por auxílio médico foi longo nesta casuística (delay's patient), em torno de 150 dias, mas também comparável aos resultados da literatura40. O tempo de evolução longo da doença (> três meses) se correlacionou com piora no estado nutricional e geral dos pacientes, de maneira semelhante ao encontrado por outros estudos, e estes pacientes devem receber maior atenção quanto ao suporte clínico e nutricional41,42.
CONCLUSÃO
Dentre os resultados, dois foram realmente marcantes, ao se considerar o CETADS como doença única: (1) não se identificaram sinais e sintomas estatisticamente significativos da fase inicial do CETADS e que (2) não houve correlação do tempo de evolução da doença com o seu estadiamento (delay's patient). Ficou assim demonstrado, e como conclusão mais importante, que os sintomas quando perceptíveis aos pacientes como indicativos de alguma anormalidade, na verdade já prenunciavam uma doença avançada, sugerindo uma rápida evolução da fase inicial da doença para as fases mais avançadas.
O longo tempo de evolução do CETADS - superior a três meses, pode ser considerado como um preditor de piora no estado geral e nutricional dos pacientes. De forma semelhante e especificamente, os sintomas "dispneia e disfagia" se associaram ao comprometimento global dos pacientes.
CONFLITO DE INTERESSES
Os autores declaram não haver conflitos de interesses.
REFERÊNCIAS
1. Curado MP. S35 The Brazilian experience on mass screening. Oral Oncol Supp. 2007;2(1):123.
2. Boyle P, Levin B. World Cancer Report 2008. Lyon: World Health Organization; 2009. p.13-5.
3. Instituto Nacional do Câncer: Incidência de Câncer no Brasil: Estimativas 2012. [Acesso em 20 Dezembro de 2012]. Disponível em: http://www.inca.gov.br/estimativa/2012.
4. Barbosa MM. Diagnóstico e tratamento dos tumores de cabeça e pescoço. 1a ed. São Paulo: Atheneu; 2001. p.491-5.
5. Biazevic MGH, Castellanos RA, Antunes JLF, Michel-Crosato E. Tendências de mortalidade por câncer de boca e orofaringe no Município de São Paulo, Brasil, 1980/2002. Cad Saúde Pública. 2006;22(10):8-15.
6. Santos RA, Portugal FB, Felix JD, Santos PMO, Siqueira MM. Avaliação epidemiológica de pacientes com câncer no trato aerodigestivo superior: relevância dos fatores de risco álcool e tabaco. Rev Bras Cancerol. 2012;58(1):21-9.
7. Avi ALRO, Tanimoto HM, Queiroz CDS, Gerim LR, Zuza EP, Trevisani DM, et al. Neoplasia de boca e orofaringe: um estudo transversal na Fundação Pio XII - Hospital do Câncer de Barretos. Rev Odontol UNESP. 2012;41(4):273-80.
8. Siu LL. Preface: head and neck cancer. Hematol Oncol Clin North Am. 2008;22(6):XIII-XV.
9. Gervásio OL, Dutra RA, Tartaglia SM, Vasconcellos WA, Barbosa AA, Aguiar MC. Oral squamous cell carcinoma: a retrospective study of 740 cases in a Brazilian population. Braz Dent J. 2001;12(1):57-61.
10. Onizawa K, Nishihara K, Yamagata K, Yusa H, Yanagawa T, Yoshida H. Factors associated with diagnostic delay of oral squamous cell carcinoma. Oral Oncol. 2003;39(8):781-8. PMID: 13679201 DOI: http://dx.doi.org/10.1016/S1368-8375(03)00075-7
11. Kowalski LP. Causes of diagnostic delay of oral cancer. Oral Oncol Supp. 2007;2(1):123-3.
12. Tromp DM, Brouha XD, Hordijk GJ, Winnubst JA, de Leeuw RJ. Patient and tumour factors associated with advanced carcinomas of the head and neck. Oral Oncol. 2005;41(3):313-9. PMID: 15743694 DOI: http://dx.doi.org/10.1016/j.oraloncology.2004.09.008
13. Guidry JJ, Greisinger A, Aday LA, Winn RJ, Vernon S, Throckmorton TA. Barriers to cancer treatment: a review of published research. Oncol Nurs Forum. 1996;23(9):1393-8. PMID: 8899755
14. Antunes JLF, Toporcov TN, Wünsch-Filho V. Resolutividade da campanha de prevenção e diagnóstico precoce do câncer bucal em São Paulo, Brasil. Rev Panam Salud Pública. 2007;21(1):30-6. DOI: http://dx.doi.org/10.1590/S1020-49892007000100004
15. Franco EL, Kowalski LP, Oliveira BV, Curado MP, Pereira RN, Silva ME, et al. Risk factors for oral cancer in Brazil: a case-control study. Int J Cancer. 1989;43(6):992-1000. PMID: 2732011 DOI: http://dx.doi.org/10.1002/ijc.2910430607
16. Noce CW, Rebelo MS. Avaliação da relação entre tamanho do tumor e características sociais em pacientes com carcinoma de células escamosas bucal. Rev Bras Cancerol. 2008;54(2):123-9.
17. Jitomirski F. Câncer bucal. In: Pinto VG, org. Saúde bucal coletiva. 4ª ed. São Paulo: Editora Santos; 2000. p.445-56.
18. Koivunen P, Rantala N, Hyrynkangas K, Jokinen K, Alho OP. The impact of patient and professional diagnostic delays on survival in pharyngeal cancer. Cancer. 2001;92(11):2885-91. PMID: 11753962 DOI: http://dx.doi.org/10.1002/1097-0142(20011201)92:11<2885::AID-CNCR10119>3.0.CO;2-G
19. Morelatto RA, Herrera MC, Fernández EN, Corball AG, López de Blanc SA. Diagnostic delay of oral squamous cell carcinoma in two diagnosis centers in Córdoba Argentina. J Oral Pathol Med. 2007;36:405-8. PMID: 17617833 DOI: http://dx.doi.org/10.1111/j.1600-0714.2007.00547.X
20. Teixeira CM. O consumo de bebidas alcoólicas como lazer [Tese de doutorado]. Vila Real: Universidade de Trás-os-Montes Alto Douro; 2008.
21. Ramos C, Carvalho JEC, Mangiacavalli MASC. Impacto e (i)mobilização: um estudo sobre campanhas de prevenção ao câncer. Ciênc Saúde Coletiva. 2007;12(5):1387-96. DOI: http://dx.doi.org/10.1590/S1413-81232007000500036
22. Sankaranarayanan R, Masuyer E, Swaminathan R, Ferlay J, Whelan S. Head and neck cancer: a global perspective on epidemiology and prognosis. Anticancer Res. 1998;18(6B):4779-86. PMID: 9891557
23. Sciubba JJ. Improving detection of precancerous and cancerous oral lesions. Computer-assisted analysis of the oral brush biopsy. U.S. Collaborative OralCDx Study Group. J Am Dent Assoc. 1999;130(10):1445-57.
24. Myers EN. Otorrinolaringologia cirúrgica - Cirurgia de cabeça e pescoço. 2a ed. Rio de Janeiro: Dilivros; 2011. p.305-32.
25. Franceschi S, Bidoli E, Herrero R, Muñoz N. Comparison of cancers of the oral cavity and pharynx worldwide: etiological clues. Oral Oncol. 2000;36(1):106-15. DOI: http://dx.doi.org/10.1016/S13688375(99)00070-6
26. Dhooge IJ, Albers FW, van Cauwenberge PB. Clinical characteristics and diagnostic delay of head and neck cancer: results from a prospective study in Belgium. Eur J Surg Oncol. 1996;22(4):354-8. PMID: 8783651 DOI: http://dx.doi.org/10.1016/S0748-7983(96)90220-6
27. Fritz A, Percy C, Jack A, Shanmugaratnam K, Sobin LH, Parkin MD, eds. International classification of diseases for oncology (ICD-O). 3rd ed. Geneva: World Health Organization; 2000.
28. Sobin LH, Wittekind Ch. Classification of Malignant Tumours. 6a ed. New Jersey: John Wiley & Sons; 2004. p. 1-44.
29. Detsky AS, McLaughlin JR, Baker JP, Johnston N, Whittaker S, Mendelson RA, et al. What is subjective global assessment of nutritional status? JPEN J Parenter Enteral Nutr. 1987;11(1):8-13. PMID: 3820522 DOI: http://dx.doi.org/10.1177/014860718701100108
30. Detsky AS, Smalley PS, Chang J. The rational clinical examination. Is this patient malnourished? JAMA. 1994;271(1):54-8. PMID: 8258889 DOI: http://dx.doi.org/10.1001/jama.1994.03510250070038
31. Ecog/WHO. Eastern Cooperative Oncology Group/World Health Organization. WHO; 2008.
32. Hashibe M, Brennan P, Benhamou S, Castellsague X, Chen C, Curado MP, et al. Alcohol drinking in never users of tobacco, cigarette smoking in never drinkers, and the risk of head and neck cancer: pooled analysis in the International Head and Neck Cancer Epidemiology Consortium. J Natl Cancer Inst. 2007;99(10):777-89. PMID: 17505073 DOI: http://dx.doi.org/10.1093/jnci/djk179
33. Wünsch-Filho V. The epidemiology of oral and pharynx cancer in Brazil. Oral Oncol. 2002;38(8):737-46. PMID: 12570051 DOI: http://dx.doi.org/10.1016/S1368-8375(02)00066-0
34. Abdo EN, Garrocho AA, Aguiar MCF. Perfil do paciente portador de carcinoma epidermóide da cavidade bucal, em tratamento no Hospital Mário Penna em Belo Horizonte. Rev Bras Cancerol. 2002;48(3):357-62.
35. Gouvea AS, Nogueira MX, Oliveira ZFL, Podestá JRV, Zeidler SVV. Aspectos clínicos e epidemiológicos do câncer bucal em um hospital oncológico: predomínio de doença localmente avançada. Rev Bras Cir Cabeça Pescoço. 2010;39(4):261-5.
36. Farah CS, Ford PJ, Allen K, Vu A, McCullough MJ. Oral Cancer and Potentially Cancerous Lesions - Early Detection and Diagnosis, Oral Cancer. [Acesso em: 2012] Disponível em: http://www.intechopen.com/books/oral-cancer/oral-cancer-and-potentiallycancerous-lesions-early-detection-and-diagnosis
37. IARC - International Agency for Research on Cancer: 2009. Oral cancer/First evidence from a randomized trial that screening reduces oral cancer mortality: The trivandrum oral cancer screening study (TOCS). Kerala, India. [Acesso em: 2011] Disponível em: http://screening.iarc.fr/study_booklptrivandrum.php
38. IARC - International Agency for Research on Cancer: Cervix Cancer Screening. Lyon: IARC Working Group; 2005. p.59-201.
39. Bispo dos Santos AL, Marinho RC, Lima PNM, Fortes RC. Avaliação nutricional subjetiva proposta pelo paciente versus outros métodos de avaliação do estado nutricional em pacientes oncológicos. Rev Bras Nutr Clín. 2012;27(4):243-9.
40. Cuffari L, Tesseroli de Siqueira JT, Nemr K, Rapaport A. Pain complaint as the first symptom of oral cancer: a descriptive study. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2006;102(1):56-61. PMID: 16831673 DOI: http://dx.doi.org/10.1016/j.tripleo.2005.10.041
41. Abdo EN, Garrocho Ade A, Barbosa AA, Oliveira EL, Franca-Filho L, Negri SL, et al. Time elapsed between the first symptoms, diagnosis and treatment of oral cancer patients in Belo Horizonte, Brazil. Med Oral Patol Oral Cir Bucal. 2007;12(7):469-73.
42. Campos JLG, Chagas JFS, Magna LA. Fatores de atraso no diagnóstico do câncer de cabeça e pescoço e sua relação com sobrevida e qualidade de vida. Rev Bras Cir Cabeça Pescoço. 2007;36(2):65-8.
1. Mestre pela UTAD, Portugal. Cirurgião de Cabeça e Pescoço, docente do curso médico da UNIMONTES
2. Doutor. Professor catedrático da UTAD - Portugal
3. Mestre e doutoranda pela UNIFESP (Médica e Docente da UNIMONTES). Universidade Estadual de Montes Claros (UNIMONTES)
Endereço para correspondência:
Francis Balduino Guimarães Santos
Rua São Pedro, nº 112. Todos os Santos
Montes Claros - MG. Brasil. CEP: 394000-123
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) do BJORL em 16 de fevereiro de 2013. cod. 10773.
Artigo aceito em 31 de julho de 2013.