Ano: 2003 Vol. 69 Ed. 5 - Setembro - Outubro - (10º)
Seção: Artigo Original
Páginas: 649 a 655
Miringoplastia com a utilização de um novo material biossintético
Myringoplasty using a new biomaterial allograft
Autor(es):
José Antonio Apparecido de Oliveira1,
Miguel Angelo Hyppolito2,
Joaquim Coutinho Netto3,
Fátima Mrué4
Palavras-chave: miringoplastia, membrana timpânica, material biossintético, fatores de crescimento
Keywords: myringoplasty, tympanic, membrane, biossintetic allografts, growth factors
Resumo:
A miringoplastia é uma cirurgia com a finalidade de controlar a infecção no ouvido médio, reconstruir o mecanismo de transmissão sonora para a janela oval e proteger a janela redonda. São descritos diversos materiais para reconstruir a membrana timpânica, destacando-se a fáscia do músculo temporal, pericôndrio do tragus, cartilagem, dura-máter, tecido placentário, entre outros. Objetivo: Este trabalho tem objetivo de demonstrar o efeito de um novo biomaterial, a membrana de látex natural com polilisina, desenvolvida no laboratório de Neuroquímica do Departamento de Bioquímica da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo - USP. Forma de estudo: Coorte Longitudinal. Material e método: O biomaterial utilizado é estimulante da neovascularização e crescimento tecidual organizado em diferentes órgãos e tecidos, sendo um material inócuo e não rejeitado pelo organismo. Foi usada a biomembrana de látex com polilisina como um implante transitório para o fechamento da perfuração da membrana timpânica. A membrana foi colocada na face externa dos bordos da membrana timpânica e a fáscia temporal na face interna da mesma. Foram estudadas 238 orelhas com perfuração de membrana timpânica por seqüela de otite média crônica, submetidas a miringoplastia com enxerto de fáscia de músculo temporal e a membrana de látex natural, com idades de 7 a 76 anos. Apresentavam uma ou mais miringoplastias anteriores sem sucesso 41 dos casos. Resultado: Como ressaltamos preliminarmente, verificamos pega do enxerto em 90,5% das orelhas (181), sendo fechamento de perfuração amplas, 96; médias, 73 e 12 pequenas. Verificamos intensa vascularização em 100% dos enxertos, o que não é habitual quando não se usa a membrana de látex natural. Conclusão: Conclue-se que o biomaterial usado merece nossa atenção quanto ao seu uso como implante transitório em miringoplastias, melhorando o processo de revascularização da membrana timpânica remanescente.
Abstract:
Myringosplaty is a surgery that is performed to control infections in middle ear, to reconstruct the sound conducting mechanism for the oval window and protection of the round window. Some materials are used to reconstruct the tympanic membrane like autologous temporalis fascia, cartilage-perichondium graft taken from the tragus, cartilage only, dura mater human placental graft. It is important the vascular support to the graft with well-vascularized flap in wide perforations. Aim: The main goal of this work is shown the use of a new biomaterial, the natural latex membrane with polylysin. Study design: Longitudinal Cohort. Material and method: This material was developed from Department of Biochemistry from Faculdade de Medicina de Ribeirão Preto Universidade de São Paulo. The natural latex membrane is used stimulating neovessels and organized tecidual growing in different parts and tissues of the human body. This material promotes any allergic reaction and is innocuous to the human tissue. The 238 ears with tympanic membrane perforation resulted from chronic middle ear infection and thek was going through myringoplasty with autologous temporalis fascia and natural latex membrane. The ages were 7 to 76 years. Results: The first results show 181 (90,5%) healing tympanic membrane perforation, 96 healing of wide perforation 73 medium perforation and 12 small one. Neovessels could be seen in all grafts and remaining tympanic membrane. This is not a habitual funding when the natural latex membrane is not used. Conclusion: According to these results we can conclude that the natural latex membrane can be used as a temporary implant in myringoplasty, improving the well vascularized of remaining tympanic membrane.
![]()
Introdução
A membrana timpânica normal é um órgão simples que apresenta duas funções básicas: a transmissão da pressão sonora à janela oval e a proteção sonora da janela redonda, além de importante proteção do ouvido médio contra infecção1. A diferença nas dimensões entre a superfície da membrana timpânica e a palatina do estribo aumenta, por princípios hidráulicos, o nível auditivo em 27dB1,2.
Histologicamente, a membrana timpânica apresenta 3 camadas: uma camada epitelial, composta por duas fileiras de células epiteliais; uma intermediária fina de constituição fibrosa, com fibras de natureza colágena, fibroblastos e células endoteliais e uma média de natureza mucosa, que se continua com a mucosa do ouvido médio3-7.
A membrana timpânica pode ter sua estrutura anatômica comprometida, levando à perfuração, que pode ser permanente ou temporária. Pode ser lesada por patologias da orelha média, associada com perfuração como nas otites médias agudas e crônicas, tecidos de granulação e traumas, incluindo-se a miringotomia com perfuração após a retirada do tubo de ventilação8. Vários estudos relatam como fator importante para a manutenção de alteração anatômica definitiva da membrana timpânica o comprometimento da camada intermediária, com alteração da organização da arquitetura das fibras colágenas. Outros fazem referência à alteração epitelial como sendo o fator mais importante, afirmando que a reconstituição epitelial é o suporte para a reparação da camada colágena intermediária5-7,9-11.
Diferentes métodos são descritos por se tratar de perfuração da membrana timpânica, incluindo-se as técnicas de miringoplastia e timpanoplastia clássicas, com o uso de enxertos confeccionados com fáscia de músculo temporal, pericôndrio do trágus, tecido endotelial, dura-máter e biomateriais compatíveis, como filme colágeno placentário humano ou bovino, todos utilizando as técnicas clássicas de microcirurgia para a plástica da membrana timpânica2,12-18.
Há uma tendência atual em simplificar os procedimentos atuais microcirúrgicos para reconstrução da membrana timpânica e melhorar a sua eficácia2,19,-22.
Tem sido descrito o uso de fatores de crescimento epitelial e de fibroblastos, estudados com sucesso no processo de cicatrização em diferentes tecidos e, mais recentemente, em perfurações de membranas timpânicas, envolvendo técnicas simples. A aquisição desses fatores de crescimento é possível por técnica de DNA recombinante que é complexa21-32.
Os resultados positivos de estudos experimentais em animais utilizando fatores de crescimento no fechamento de perfurações de membranas timpânicas têm incentivado o seu uso em estudos clínicos em pacientes acometidos por otite média crônica. Estudo realizado por Hamsay (1995) utilizando o fator de crescimento epidérmico em perfurações de membranas timpânicas em humanos não mostrou eficiência satisfatória quanto ao fechamento das mesmas23,24,26-35.
Alguns estudos demonstram a atuação de lisados de culturas de queratinócitos na cicatrização de diferentes tecidos e, mais recentemente, sua atuação na cicatrização e fechamento de perfurações de membranas timpânicas em modelos animais. Em estudos clínicos realizados em pacientes que foram submetidos às técnicas clássicas de miringoplastia com o uso de enxerto de fáscia de músculo temporal e cultura de queratinócitos, houve considerável redução no tempo de fechamento das perfurações timpânicas, sendo ainda incerta qual a sua forma da atuação e sugerindo-se seu efeito relacionado com a atividade mitótica primária através de fatores de crescimento e citocinas27,36-38. Também tem sido tentado o uso de ácido hialurônico, que se distribui na matriz extracelular de tecido conjuntivo no homem e em outros animais, apresentando resultados positivos em perfurações de membrana timpânica, principalmente perfurações pequenas e traumáticas, na ausência de infecção crônica da orelha média propondo-se seu uso como substituto para as técnicas clássicas de microcirurgia para a reconstrução da membrana timpânica nestes casos20,-22,39,40.
Um novo material biocompatível, a base de látex natural polimerizado (látex natural extraído da seringueira Haevea brasiliensis) com polilisina 0,1% foi desenvolvido por um método de polimerização a frio pelo setor de neuroquímica do Departamento de Bioquímica da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo. Foi usado a princípio como material indutor da cicatrização de paredes esofágicas lesadas. Observou-se no esôfago neoformado de cães (área de 4-6 cm) um marcante aumento da vascularização (angiogênese), epitelização (epitélio pseudo estratificado), neoformação glandular submucosa e fibras musculares neoformadas25,41,42. O material não promove reação alérgica e não é rejeitado pelo organismo do cão e do homem. Em outras áreas da medicina vem sendo estudado e utilizado com sucesso no processo de cicatrização de úlceras flebopáticas, arteriais e diabéticas e em áreas da superfície corpórea queimadas.
Motivados por buscar um método simples, prático e para melhora dos resultados de miringoplastias, tentamos utilizar a membrana natural de látex com polilisina 0,1% como coadjuvante no fechamento de perfurações timpânicas por infecção da orelha média, sem colesteatoma, buscando um material que possa dar suporte para o processo natural de regeneração da membrana timpânica remanescente. As técnicas clássicas de miringoplastia utilizando como enxerto a fáscia muscular temporal mostram insucessos, que variam de 10% a 30%, dependendo do tamanho da perfuração e da técnica utilizada, sendo que as perfurações amplas são as que mais apresentam índices de insucessos, com perfuração residual principalmente por insuficiência de vascularização do enxerto livre43-47. Baseados no fato de a biomembrana de látex favorecer sobretudo a neovascularização, propusemos a princípio estudar o seu efeito na eficácia da vascularização do enxerto de fáscia temporal a partir da membrana remanescente, seguindo as técnicas convencionais de miringoplastia, na busca de melhora dos resultados desta cirurgia.
Objetivos
Os objetivos do trabalho foram: observar a interação da biomembrana de látex com o tecido timpânico humano; observar a biocompatibilidade da biomembrana de látex, a toxicidade do biomaterial, a presença de reações alérgicas, a possibilidade do uso da membrana natural de látex como implante transitório em miringoplastias; o efeito desta estimulação no sucesso de miringoplastia; e observar a neovascularização induzida pelo biomaterial.
Material e Método
Foram selecionados aleatoriamente 238 pacientes registrados e seguidos em ambulatório de otorrinolaringologia, com perfuração crônica da membrana timpânica e história clínica de otite média crônica simples, com um tempo de evolução de otorréias crônicas intermitentes maior que um ano. Nenhum dos pacientes apresentava história de ruptura traumática da membrana timpânica.
O tamanho da perfurações foi dividido em: ampla (> que um quadrante da membrana timpânica), média (de meio a um quadrante da membrana timpânica) e pequena (menor que meio quadrante da membrana timpânica) avaliados subjetivamente. As orelhas selecionadas não apresentavam sinais de infecção, nem otorréia (200). As perfurações foram filmadas e fotografadas no pré operatório com otoendoscópio (Richards 235210-2.7mm-0º).
Foram eliminadas 38 orelhas das 238 iniciais pelos critérios de exclusão:
- infecção pós-operatória - 10
- presença de Glue ear - 1
- presença de colesteatoma - 1
- pólipo - 3
- mal posicionamento do látex - 23
TOTAL = 38
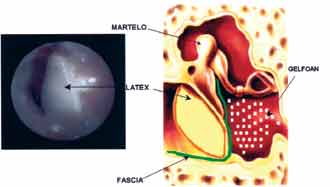
Os pacientes foram submetidos às técnicas clássicas de Miringoplastia, realizadas por uma equipe de cirurgiões do serviço e médicos residentes, sob anestesia geral e com a utilização do enxerto livre de fáscia do músculo temporal, apoiado sobre gel foam colocado na orelha média e sob os bordos da perfuração escarificados. Posteriormente, foi colocada a membrana natural de látex externamente, apoiada na face externa dos bordos da membrana timpânica remanescente e em contato com a fáscia temporal. A placa foi apoiada por gel foam e pomada otológica contendo polimixina e bacitracina (Figura 1).
Os pacientes receberam alta hospitalar no primeiro dia de pós-operatório após avaliação otomicroscópica para o diagnóstico precoce de infecção (presença de otorréia). Não foram utilizadas gotas otológicas contendo antibiótico nestes pacientes rotineiramente, somente utilizadas nos casos em que havia sinais de infecção.
No sétimo dia de pós-operatório, os pacientes foram submetidos a uma segunda avaliação com exame otomicroscópio do ouvido operado, verificando a ocorrência de infecção (otorréia), presença da pomada no conduto auditivo externo e posicionamento da biomembrana de látex. Neste período, se a biomembrana de látex estivesse solta era reposicionada, e se houvesse presença de otorréia, a mesma era tratada com gotas otológicas tópicas de ciprofloxacin, sendo tais ouvidos descartados da avaliação final (critérios de exclusão).
Posteriormente, os pacientes foram avaliados com trinta dias de pós-operatório, onde foram verificados os mesmos itens acima. Neste período, a biomembrana de látex era removida, e o aspecto do enxerto era avaliado e documentado através de otoendoscopia, bem como o sucesso do fechamento da perfuração timpânica.
Figura 1. Foto mostrando a biomembrana de látex com polilisina.
Figura 2. Esquema do posicionamento da fáscia do músculo temporal e da membrana de látex junto a membrana timpânica.
Resultados
A Tabela I mostra o número de orelhas e a faixa etária consideradas no trabalho.
Das cirurgias consideradas como sucesso, pega total do enxerto de fáscia temporal, descrevemos na Tabela II as características deste grupo quanto ao sexo, lado acometido pela perfuração, localização e tamanho da perfuração na membrana timpânica comprometida e número de timpanoplastias sem sucesso, anteriores a utilização da membrana biossintética de látex.
- Resultados positivos pega total do enxerto - 181 orelhas - 90,5%
- Resultados negativos - 19 orelhas - 9,5%
- Equipe cirúrgica - Docentes e Residentes
- Vascularização exuberante e hiperemia do enxerto e da membrana timpânica remanescente
- Tempo médio de confirmação da pega do enxerto - 28 diasTabela I. Descrição do grupo de estudo.
Orelhas: 238 consideradas no estudo
38 excluídas pelos critérios de exclusão
200 consideradas para a avaliação final
181 consideradas como sucesso da cirurgia
19 consideradas como insucesso da cirurgia
Idade: 7 - 76 anos (média 24 anos)
Tabela II. Caracterização do grupo de estudo em que os resultados foram positivos, com pega total do enxerto.
Perfuração - Localização
Central - 118
Centro anterior - 17
Centro inferior - 4
Centro - Superior - 3
Póstero-superior - 9
Póstero-inferior - 10
Ântero-inferior - 20
Total - 181
Tamanho da Perfuração
Pequena - 12
Média - 73
Ampla - 96
Total - 181
Cirurgias anteriores com insucesso
1ª Cirurgia - 32
2ª Cirurgia - 6
3ª Cirurgia - 3
Total - 41
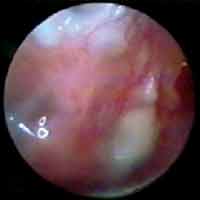
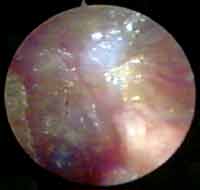
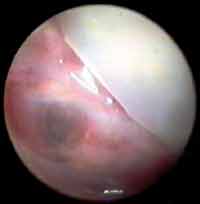
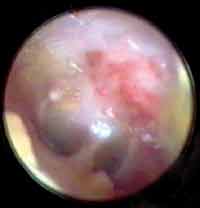
O primeiro aspecto observado foi o estado do enxerto, ressaltando a exuberante vascularização e hiperemia do mesmo e da membrana timpânica remanescente (Figuras 3, 4 e 5). Tal fato não é observado nos ouvidos que são submetidos a miringoplastias sem a colocação da membrana natural de látex, onde o enxerto mostra-se pálido e pouco vascularizado.
O segundo aspecto avaliado foi o sucesso do fechamento da perfuração, o que foi verificado em 90,5% (181 casos) dos pacientes, ressaltando-se que 32 das orelhas já haviam sido submetidas a uma cirurgia, 6 das orelhas a 2 cirurgias e 3 orelhas à 3ª cirurgia de miringoplastia sem sucesso. Verificamos ainda fechamento completo de 96 dos ouvidos onde as perfurações eram amplas.
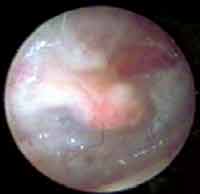
O tempo médio de fechamento das perfurações foi de 28 dias. Com dois meses as membranas timpânicas já se mostravam de aspecto normal (Figuras 6 e 7).
Figura 3. Otoendoscopia de paciente no 45º dia de pós-operatório, mostrando intensa hiperemia e vascularização do enxerto de fáscia de músculo temporal, incorporado a membrana timpânica remanescente.
Figura 4. Otoendoscopia de paciente no 25º dia de pós operatório, mostrando os vasos neoformados a partir da membrana timpânica remanescente.
Figura 5. Otoendoscopia de paciente no ouvido com 2 semanas de pós operatório, mostrando a vascularização do enxerto logo após retirada da membrana de látex.
Figura 6. Otoendoscopia de paciente ouvido com 10 dias de pós operatório, mostrando perfuração fechada (apenas com o uso da membrana) e membrana de látex.
Figura 7. Otoendoscopia de paciente com dois meses de pós-operatório, mostrando o aspecto normal da membrana timpânica (pós fechamento de perfuração média).
Discussão
Os processos envolvidos no mecanismo de fechamento de perfurações da membrana timpânica ainda são pouco compreendidos9-11,27,31,48. Estudos realizados nas duas últimas décadas apontam a importância de fatores de crescimento próprios da membrana timpânica normal e a expressão destes fatores ocorrendo de forma diferente em membranas timpânicas perfuradas23-35.
Tais estudos fortalecem as expectativas de se esclarecer os fatores que atuam na cicatrização e fechamento de membranas timpânicas lesadas e que determinam seu comportamento de cicatrização diferente do de outros tecidos9-11,27,31.
Os estudos experimentais em animais mostram-se favoráveis ao uso de fatores de crescimento epitelial e de fibroblastos, estimulando o crescimento celular e promovendo vasodilatação, com aumento do suprimento sangüíneo para a membrana timpânica, favorecendo assim o fechamento de perfurações49. No entanto, seu uso a longo prazo, em experimentos com animais, demonstrou a possibilidade de desenvolvimento de colesteatoma e não foi verificado sucesso no fechamento de perfurações crônicas, em estudos em seres humanos28,29,35,36,38.
A tendência em se procurar simplificar as técnicas tradicionais para a correção de perfurações da membrana timpânica, reduzindo seus custos e operacionalidade e tornando-as totalmente efetivas, estimula a busca de alternativas para novos enxertos e para a melhora dos que são disponíveis atualmente, principalmente o de fáscia de músculo temporal que é o mais utilizado e com sucesso que varia de 70% a 90%43-47.
A membrana natural de látex acrescida com polilisina mostrou neste trabalho eficiente alternativa na cicatrização de tecidos com possível atuação no complexo mecanismo de reparação da membrana timpânica. É material de baixo custo e de fácil aquisição, não promovendo reação alérgica ou rejeição pelo organismo humano. Por ser um material vegetal não existe a preocupação com possível transmissão de vírus patogênicos para o homem como os das hepatites B e C e HIV, o que não ocorre quando da obtenção dos fatores de crescimento e lisados de queratinócitos que necessitam de "células doadoras humanas".
Estudos preliminares mostram a presença de um possível fator de crescimento vascular vegetal presente na seringueira (Hevea brasiliensis) e com atuação em tecidos humanos, possibilitando através da sua capacidade de indução de angiogênese, melhorar a vascularização de enxertos de fáscia do músculo temporal, a partir da membrana timpânica remanescente, o que ocorreu neste trabalho50.
Conclusões
A membrana natural de látex confeccionada a partir de seringueira (Hevea brasiliensis) mostrou excelente interação com os tecidos da membrana timpânica humana, excelente biocompatibilidade, nenhuma toxicidade e ausência manifestações alérgicas.
A eficiência na regeneração das membranas timpânicas perfuradas ocorre principalmente devido ao processo intenso de revascularização da membrana timpânica remanescente.
Outro fato interessante observado no estudo é que o sucesso no fechamento da perfuração timpânica com a membrana biossintética de látex como coadjuvante ocorreu de uma forma significativa também quando a cirurgia foi realizada por médicos residentes em Otorrinolaringologia do 2º ano que será oportunamente comparado aos resultados cirúrgicos dos residentes do 2º ano anterior ao uso da membrana biossintética de látex.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Wullstein H. Theory and Practice of Tympanoplasty. Laryngoscope 1956; 66:1076-95.
2. Briggs RJ, Luxford WM. Chronic Ear Surgery: A Historical Review. Am J Otol 1994; 15:558-67.
3. Amoils CP, Jackler RK, Milczuk H, Kelly KE, Cao K. An Animal Model of Chronic Tympanic Membrane Perforation. Otolaryngol Head Neck Surg 1992; 106:47-55.
4. Johnson A, Hawke M. The Function of Migratory Epidermis in the Healing of Tympanic Membrane Perforations in Guinea Pig. Acta Otolaryngol (Stockh) 1987; 103:81-6.
5. Litton WB. Epidermal Migration in the Ear:The Location and Characteristics of the Generation Center Revealed by Utilizing a Radioactive Desoxyribose Nucleic Acid Precursor. Acta Otolaryngologica (Suppl.) 1969; 240:5-39.
6. Reijnen CJH, Kuijpers W. The Healing Pattern of the Drum Membrane. Acta Otolaryngologica (Suppl.) 1971; 287:1-74.
7. Taylor M, McMinn RMH. Cytology of Repair in Experimental Perforations of the Tympanic Membrane and its Relationship to Chronic Perforations in Man. TR Am Acad Ophth Otol 1967; 71:802-12.
8. Jackson CG, Schall DG, Glasscock ME 3rd, Macias JD, Widick MH, Touma BJ. A surgical Solution for the Difficult Chronic Ear. Am J Otol 1996; 17:7-14.
9. Spandow O, Hellstrom S, Dahlstrom M. Structural Characterization of Persistent Tympanic Membrane Perforations in Man. Laryngoscope 1996; 106:346-52.
10. Gladstone HB, Jackler RK, Varav K. Tympanic Membrane Wound Healing. An Overview. Otolaryngol Clin North Am 1995 Oct; 28:913-32.
11. Koba R. Epidermal Cell Migration and Healing of the Tympanic Membrane:An Immunohistochemical Study of Cell Proliferation Using Bromodeoxyuridine Labeling. Ann Otol Rhinol Laryngol 1995; 104:218-25.
12. Carrat X, Bozon N, Rabaud M, Deminiere C, Bebear JP. Development of Artificial Collagen-elastin Conjunctive Matrix for Tympanoplasty. Concept and 1st Results of Animal Experiments. Ann Otolaryngol Chir Cervicofac 1995; 112:52-7.
13. Ensari S, Selampinar F, Akalin Y, Kara CO, Dagli S, Ergin A, Ozdem C. The Use of Molded Tympanic Heterograft (Lamb Peritoneum). Ear Nose Throat J 1995 Jul; 74:487-9.
14. Grote JJ, Bakker D, Hesseling SC, Van Blitterswijk CA. New Alloplastic Tympanic Membrane Material. AM J Otol 1991; 12:329-35.
15. Hartwein J, Leuwer R. "Crown-cork tympanoplasty": A Method for Complete Reconstruction of the Tympanic ¨Membrane Laryngorhinootologie. 1992; 71:102-5.
16. Klotz G, Flesch J, Bilger P. Use of New Materials in Tympanic Reconstruction. Rev Laryngol Otol Rhinol (Bord) 1988; 109:67-9.
17. Truy E, Disant F, Morgon A. Experimental Study in Dogs of a Human Reticulated Placental IV Collagen Film for Myringoplasty. Rev Laryngol Otol Rhinol (Bord) 1990; 111:79-82.
18. Truy E, Disant F, Tardy M, Tayot JL, Eloy R, Morgon A. Use of Human Placental Type IV Collagen in Tympanoplasty. Results of Initial Animal Experimentation. Ann Otolaryngol Chir Cervicofac 1990; 107:209-13.
19. Kohn FE, Feijen J, Feenstra L. New Perspectives in Myringoplasty. Int J Artif Organs 1984; 7:151-62.
20. Laurent C, Soederberg O, Aniko M, Hartwig S. Repair of Chronic Tympanic Membrane Perforations Using Applications of Hyaluronan or Rice Paper Prosthesis ORL J Otorhinolaryngol (Relat. Spec.) 1991; 53:37-40.
21. Stenfors LE. Repair of Traumatically Ruptured Tympanic Membrane Using Hyaluronan. Acta Otolaryngol 1987 (Stockh) (Suppl) 442:88-91.
22. Stenfors LE. Treatment of Tympanic Membrane Perforations With Hyaluronan in an Open Pilot Study of Unselected Patients. Acta Otolaryngol (Stockh) 1987 Suppl; 442:81-7.
23. Fina M, Bresnick S, Baird A, Ryan A. Improved Healing of Tympanic Membrane Perforations with Basic Fibroblast Growth Factor. Grow Factors 1991; 5:265-72.
24. Mondain M, Saffiedine S, Uziel A. Fibroblast Growth Factor Improves the Healing of Experimental Tympanic Membrane Perforations. Acta Otolaryngol (Stockh) 1991; 111:37-341.
25. Mrue F, Thomazinni JA, Tambeliini H, Coutinho Netto J, Ceneviva R, Lachat JJ, Zborowski AC. Latex Membrane from Hevea brasiliensis as a biomaterial-A New Concept for an Old Material. J Biomaterials - In Press.
26. O'Daniel TG, Ptitjean M, Jones SC et al. Epidermal Growth Factor Binding and Action on Tympanic Membranes. Ann. Otol Rhinol Laryngol 1990; 99:80-4.
27. Somers T, Goovaerts G, Schelfhout L, Peeters S, Govaerts PJ, Offeciers E. Growth Factors in Tympanic Membrane Perforations. Am J Otol 1998; 19:428-34.
28. Dvorak DW, Abbas G, Ali T, Stevenson S, Welling DB. Repair of Chronic Tympanic Membrane Perforations With Long-Term Epidermal Growth Factor. Laryngoscope 1995; 105:1300-4.
29. Hom DB. Growth Factors in Wound Healing. Otolaryngol Clin North Am 1995 Oct; 28:933-53.
30. Vrabec JT, Schwaber MK, Davidson JM, Clymer MA. Evaluation of Basic Fibroblast Growth Factor in Tympanic Membrane Repair. Laryngoscope 1994; 104:1059-64.
31. Koba R, Kawabata I. Immunohistochemical Study of Transforming Growth Factor- Expression in Normal and Perforated Tympanic Membrane. Ann Otol Rhinol Laryngol 1995; 104:793-7.
32. Friedman N, Wrigth CG, Pawlowiski KS, Meyerhoff WL. Effect of Basic Fibrolast Growth Factor on Perforated Chinchilla Tympanic Membranes. ENT-Ear, Nose & Throat Journal 1997; 76:559-64.
33. Mondain M, Ryan A. Epidermal Growth Factor and Fibroblast Growth Factor Are Induced in Guinea-pig Tympanic Membrane Following Traumatic Perforation. Acta Otolaryngol (Stockh) 1995; 115:50-4.
34. Mondain M, Ryan A. Histological Study of the Healing of Traumatic Tympanic Membrane Perforation After Basic Fibroblast Growth Factor Application. Laryngoscope 1993; 103: 312-8.
35. Ramsay HA, Heikkonen EJ, Laurila PK. Effect of Epidermal Growth Factor on Tympanic Membranes With Chronic Perforations: a Clinical Trial. Otolaryngol Head Neck Surg 1995; 113:375-9.
36. Somers T, Duinslaeger L, Delaey B, Verbeken G, Vanhalle S, Boedts D, Govaerts PJ, Offeciers E. Stimulation of Epithelial Healing in Chronic Postoperative Otorrhea Using Lyophilized Cultured Keratinocyte Lysates. Am J Otol 1997; 18:702-6.
37. Clymer MA, Schwaber MK, Davidson JM. The Effects of Keratinocyte Growth Factor on Healing of Tympanic Membrane Perforations. Laryngoscope 1996; 106:280-5.
38. Somers T, Verbeken G, Vanhalle S, Delaey B, Duinslaeger L, Govaerts P, Offeciers E.Lysates From Cultured Allogeneic Keratinocytes Stimulate Wound Healing After Tympanoplasty. Acta Otolaryngol (Stockh) 1996; 116:589-93.
39. Amoils CP, Jackler RK, Lustig LR. Repair of Chronic Tympanic Membrane Perforations Using Epidermal Growth Factor. Otolaryngology Head and Neck Surgery 1992; 107:669-83.
40. Hellstromp S, Laurent C. Hyaluronan and Healing of Tympanic Membrane Perforations. An Experimental Study. Acta Otolaryngol (Stockh) 1987 Suppl; 442:54-61.
41. Mrue F, Coutinho Netto J, Ceneviva R, Zucolotto S, Lachat JJ, Zborowski AC. Esophageal Replacement by a New Kind of Esophageal Prosthesis. XXX World Congress of the International College of Surgeons. Kyoto, Japan November 1996; 247-52.
42. Mrue F. Substituição do Esôfago Cervical por Prótese Biossintética de Látex - Estudo Experimental em Cães. Tese de Mestrado. Faculdade de Medicina de Ribeirão Preto-USP-1996.
43. Chandrasekhar SS, House JW, Devgan U. Pediatric Tympanoplasty. A 10-year Experience. Arch Otolaryngol Head Neck Surg 1995; 121:873-8.
44. Halik JJ, Smyth GD. Long-Term Results of Tympanic Membrane Repair. Otolaryngol Head Neck Surg 1988; 98:162-9.
45. Perrin A, Mendoza R, Baril C, Receveur M, Roulleau P. Long-term anatomic results of tympanic homografts. Apropos of 170 cases. Ann Otolaryngol Chir Cervicofac 1987; 104:535-9.
46. Podoshin L, Fradis M, Malatskey S, Ben-David J. Tympanoplasty in Adults: A Five-year Survey. Ear Nose Throat J 1996; 75:149-52, 155-6.
47. Podoshin L, Fradis M, Malatskey S, Ben-David J. Type I Tympanoplasty in Children. Am J Otol 1996; 17:293-6.
48. Stenfors LE, Carlsöö B,Winbland B. Repair of Experimental Tympanic Membrane Perforations. Acta Otolaryngol 1980; 90:332-41.
49. Mondain M, Ryan A. Effect of Basic Fibroblast Growth Factor on Normal Tympanic Membrane. Am J Otolaryngol 1994; 15:344-50.
50. Oliveira, JAA, Bernal TMO. Fatores neurotróficos de crescimento. In: Campos CAH, Costa HOO. Tratado de Otorrinolaringologia. 1ª Edição. São Paulo: Editora Roca; 2003. v. 1, p. 138-55.
1 Professor Titular do Departamento de Oftalmologia, Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da Faculdade de Medicina de Ribeirão Preto - USP.
2 Médico Assistente do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto - USP.
3 Professor Associado do Departamento de Bioquímica e Imunologia da Faculdade de Medicina de Ribeirão Preto - USP.
4 Aluno de Pós-Graduação do Departamento de Cirurgia da Faculdade de Medicina de Ribeirão Preto - SP.
Departamento de Oftalmologia, Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da Faculdade de Medicina de Ribeirão Preto - USP - Área Otorrinolaringologia (Otologia) - Hospital das Clínicas de Ribeirão Preto.
Artigo recebido em 14 de abril de 2003. Artigo aceito em 24 de julho de 2003.