Ano: 2011 Vol. 77 Ed. 4 - Julho - Agosto - (14º)
Seção: Artigo Original
Páginas: 499 a 503
Betaistina no tratamento do zumbido em pacientes com distúrbios vestibulares
Betahistine in the treatment of tinnitus in patients with vestibular disorders
Autor(es): Maurício Malavasi Ganança1; Heloisa Helena Caovilla2; Juliana Maria Gazzola3; Cristina Freitas Ganança4; Fernando Freitas Ganança5
Palavras-chave: conduta do tratamento medicamentoso, tontura, vertigem, zumbido.
Keywords: dizziness, medication therapy management, tinnitus, vertigo.
Resumo:
A betaistina é um medicamento utilizado no tratamento de distúrbios da função vestibular, que também tem sido utilizado para tratar o zumbido. Objetivo: Avaliar o efeito da betaistina sobre o zumbido de pacientes com distúrbios vestibulares. Material e Método: Foram coletados dados retrospectivos de pacientes com vestibulopatia e zumbido. Os pacientes incluídos receberam 48 mg/dia de betaistina ao dia e os resultados clínicos foram comparados com os de um grupo controle, que incluiu indivíduos impossibilitados de receber betaistina devido à gastrite, úlceras, gravidez, asma ou hipersensibilidade ao medicamento. Os pacientes realizaram controle de fatores agravantes e exercícios de reabilitação vestibular, como tratamento de base para a vestibulopatia. A intensidade, frequência e duração do zumbido foram avaliadas no primeiro dia e após 120 dias de tratamento. A melhora clínica foi definida pela redução total ou parcial do zumbido após o tratamento. Resultados: Observou-se melhora clínica do zumbido em 80/262 (30,5%) dos pacientes tratados com a betaistina e em 43/252 (17,1%) pacientes do grupo controle. A betaistina melhorou significativamente (p<0.0001) o zumbido nos indivíduos tratados. Conclusão: A dose de 48 mg/dia de betaistina durante 120 dias consecutivos é útil na redução ou eliminação do zumbido de pacientes com distúrbios vestibulares.
Abstract:
Betahistine is a medicine used to treat vestibular disorders that has also been used to treat tinnitus. Aim: To assess the effects of betahistine on tinnitus in patients with vestibular disorders. Material and method: Retrospective data were collected from patient records for individuals presenting with vestibular dysfunction and tinnitus. Patients included had received betahistine 48 mg/day and clinical outcomes were compared with a control group comprising individuals who were unable to receive betahistine due to gastritis, ulcers, pregnancy, asthma or hypersensitivity to the drug. Patients underwent control of any aggravating factors and also standard vestibular exercises as a basis for treatment. The intensity, frequency and duration of tinnitus were assessed on the first day of dosing and after 120 days of treatment. Clinical improvement was defined as a total or partial reduction of tinnitus after treatment. Results: Clinical improvement was observed in 80/262 (30.5%) of patients treated with betahistine and 43/252 (17.1%) of control patients. Betahistine significantly (p<0.0001) improved tinnitus in treated individuals. Conclusion: The daily dosage of 48 mg of betahistine during 120 consecutive days is useful to reduce or eliminate tinnitus in patients with vestibular disorders.
![]()
INTRODUÇÃO
O zumbido, a percepção de som na ausência de um estímulo acústico aparente, é uma preocupação de saúde crescente em todas as camadas da população. As estimativas indicam que 10%-15% da população podem apresentar zumbido. Adultos e crianças podem ser afetados, a prevalência de zumbido aumenta com a idade e existe uma alta incidência associada tanto com a exposição ao ruído como com a perda de audição relacionada com a idade. Apesar de sua fisiopatologia ainda precisar ser elucidada, o zumbido poderia ser resultado de uma atividade neural espontânea e aberrante em qualquer nível do sistema auditivo1.
Aproximadamente 8% dos indivíduos com zumbido são gravemente debilitados pelo sintoma angustiante; em 2.800 pacientes com zumbido, ocorreu uma associação significante (p<0,05) entre o sintoma e a redução da qualidade de vida2. Não há influência de gênero, idade e perda auditiva no incômodo gerado pelo zumbido3.
O zumbido subjetivo é um sintoma comum com muitas causas4. Um estudo epidemiológico mostrou que a causa mais comum do zumbido foi a perda da audição induzida pelo ruído (37,8% dos casos); entretanto, muitos casos podem estar correlacionados com diversos outros distúrbios, tais como dor, ansiedade, depressão e dores de cabeça causadas por migrânea5. Distúrbios otológicos, especialmente os que cursam com perda auditiva neurossensorial ou condutiva, como exposição excessiva a ruídos intensos, presbiacusia, doenças metabólicas, ototóxicos, doença de Ménière, schwannoma vestibular, desordens psicológicas, são fatores causais frequentes6. O zumbido também pode ocorrer em pacientes com audiometria normal; os pacientes com zumbido e audição normal apresentaram características clínicas semelhantes às dos pacientes com perda auditiva; no entanto, a faixa etária acometida e a interferência sobre a concentração e o equilíbrio emocional foram significantemente menores7. Em pacientes idosos em que o achado principal à audiometria foi a presbiacusia, não foi encontrada correlação entre o grau da perda auditiva e o grau de insatisfação do paciente com o zumbido8. O zumbido é um dos quatro sintomas clássicos da doença de Ménière, uma condição associada ao prejuízo substancial da qualidade de vida do paciente9.
A terapia do zumbido é tão diversificada quanto a origem da condição. Quando há uma causa aparente, ela deve ser tratada. O controle da causa pode não ser suficiente para reduzir ou eliminar o zumbido. Com graus variáveis de sucesso, foram propostos diferentes tratamentos para zumbido, tais como terapia de retreinamento, mascaramento sonoro, utilização de prótese auditiva, acupuntura e terapia farmacológica.
Diversas opções farmacêuticas têm sido investigadas10-12, com diferentes graus de benefício sintomático e melhora da qualidade de vida1-2,13. Foram experimentados estabilizadores de membrana (cloridrato de lidocaína), anticonvulsivantes (carbamazepina, gabapentina), antidepressivos (cloridrato de fluoxetina, cloridrato de sertralina), ansiolíticos (clonazepam, alprazolam), extrato 761 de Ginkgo biloba, vasomoduladores (flunarizina, cinarizina e betaistina); o tempo de uso de cada medicação e o critério de escolha depende da característica clínica de cada paciente14.
Há estudos mostrando que a betaistina pode oferecer alívio sintomático do zumbido15-18. A betaistina é um heterorreceptor antagonista H3 e um receptor agonista H1 que melhora a microcirculação no ouvido interno19, promovendo e facilitando a compensação vestibular central20-22. É atualmente indicada para o tratamento dos sintomas de diversos distúrbios vestibulares23-24, incluindo o zumbido. Os possíveis eventos adversos da betaistina incluem dor de cabeça e desconforto epigástrico. A betaistina é contraindicada em pacientes com úlcera gastrointestinal, asma, feocromocitoma e hipersensibilidade ao medicamento23.
O objetivo deste estudo foi avaliar o efeito da betaistina sobre o zumbido de pacientes com distúrbios da função vestibular.
MÉTODO
Este foi um estudo de controle de caso, retrospectivo e experimental, realizado em uma instituição universitária. Foram coletados os dados retrospectivos de 865 pacientes com idade acima de 18 anos que apresentavam disfunção vestibular periférica e zumbido. O estudo foi aprovado pelo Comitê de Ética em Pesquisa da universidade onde o estudo foi realizado, sob o protocolo de número 0117/08.
Os pacientes foram submetidos a uma avaliação otoneurológica que incluiu história clínica, exame de ouvido, nariz e garganta, avaliação audiológica e vestibular. A avaliação da audição foi realizada por meio de audiometria tonal, testes de reconhecimento da fala e medida de imitância acústica. Avaliação do processamento auditivo, audiometria de tronco encefálico e/ou eletrococleografia foram eventualmente realizadas. A avaliação de equilíbrio corporal incluiu testes de Romberg e Unterberger-Fukuda, pesquisa de nistagmo posicional e de posicionamento e eletronistagmografia.
Foram incluídos pacientes com diagnóstico de distúrbios vestibulares periféricos. Foram excluídos os pacientes com distúrbios do sistema nervoso central e os que não completaram o período de tratamento ou que utilizaram outras medicações antivertiginosas ou zumbidogênicas. Os pacientes que podiam utilizar betaistina formaram o grupo de estudo, enquanto que o grupo controle compreendeu pacientes impossibilitados de receber a medicação por diversos motivos, incluindo gastrite grave, úlcera, gravidez, asma e hipersensibilidade ao medicamento.
Os pacientes do grupo de estudo receberam 48 mg/dia de dicloridrato de betaistina em 2 ou 3 administrações ao dia, durante 120 dias. Todos os pacientes realizaram controle dos fatores agravantes e exercícios de reabilitação vestibular como tratamento de base. Com o objetivo de poder comparar de modo homogêneo os resultados clínicos entre os grupos de tratamento e de controle, uma amostra randômica de pacientes do grupo de estudo foi selecionada para fornecer um número semelhante de indivíduos em cada grupo para análise estatística.
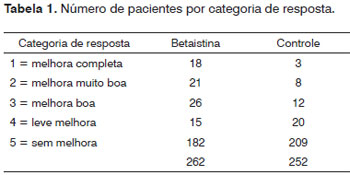
Os pacientes foram observados no início e após quatro meses de terapia. A impressão global do paciente foi utilizada como variável para avaliar a eficácia do tratamento. A efetividade foi avaliada de acordo com a resposta subjetiva ao final do período de tratamento. A avaliação da eficácia foi realizada utilizando-se a classificação a seguir: 1 = melhora completa (paciente livre de sintomas), 2 = melhora muito boa, 3 = melhora boa, 4 = leve melhora e 5 = sem melhora. Os pacientes com melhora muito boa, melhora boa, e melhora leve foram incluídos na categoria de melhora (melhora parcial). A tolerabilidade foi julgada pelos investigadores e pelo paciente no fim do tratamento. O teste de chi-quadrado foi utilizado para comparar estatisticamente a melhora clínica do zumbido entre os grupos de tratamento e controle. O nível de significância foi de 5% (α= 0,05). As análises estatísticas foram realizadas utilizando SPSS 10.0 para Windows (Pacote Estatístico para Ciências Sociais, versão 10.0, 1999).
RESULTADOS
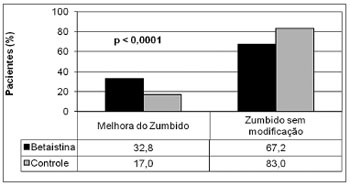
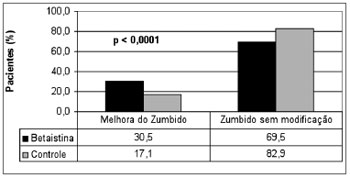
Um total de 613 pacientes do grupo de estudo (70,9%) e 252 do grupo de controle (29,1%) foram incluídos. A melhora clínica foi observada em 202 (32,8%) pacientes do grupo de estudo e em 43 (17%) casos do grupo de controle, como mostra a Figura 1. Com o objetivo de comparar os resultados clínicos do zumbido entre os grupos, uma amostra randômica de 42,7% pacientes do grupo de estudo (n=262) foi selecionada para fornecer um número semelhante de indivíduos do estudo e do controle para análise (Figura 2). Um total de 514 pacientes constituiu a casuística desta pesquisa. O grupo experimental foi constituído por 262 pacientes (51,0%), com idade variando de 19 a 76 anos (média de 54,5 anos), sendo 160 do gênero feminino (61,1%) e 102 (39,9%) do gênero masculino e o grupo controle foi formado por 252 pacientes (49,0%), com idade variando de 22 a 79 anos (média de 56,0 anos), sendo 156 do gênero feminino (62,4%) e 90 (37,6%) do masculino. Não foi observada diferença entre os grupos de estudo e de controle quanto ao número de casos tratados, a idade e o gênero. Observou-se melhora clínica em 80/262 (30,5%) pacientes tratados com a betaistina e em 43/252 (17,1%) casos do grupo controle (Tabela 1). Houve diferença estatisticamente significativamente (p<0,0001) entre os resultados do grupo de estudo e o grupo controle, quanto à porcentagem de casos melhorados, demonstrando a eficácia da betaistina na remissão ou eliminação do zumbido nos pacientes com disfunção vestibular.
Figura 1. Comparação da melhora clínica do zumbido entre os pacientes do grupo de estudo e do grupo de controle.
Figura 2. Comparação da melhora clínica do zumbido entre uma amostra randômica do estudo e os pacientes do grupo de controle.
O tratamento com betaistina foi bem tolerado, com uma baixa incidência de eventos adversos leves e transitórios, como dor de cabeça, desconforto epigástrico e dispepsia. Não foi necessário interromper o uso do medicamento em nenhum dos casos que apresentaram estes eventos adversos.
DISCUSSÃO
A betaistina é atualmente utilizada no tratamento de diversos distúrbios vestibulares24. Em uma revisão sobre os efeitos da betaistina em pacientes com doença de Ménière, alguns estudos mostraram resultados considerados favoráveis quanto à redução da vertigem e do zumbido e um estudo mostrou que a betaistina não causava efeito sobre o zumbido em comparação com o placebo15. As pesquisas clínicas mais recentes têm demonstrado que a betaistina é eficiente no tratamento dos sintomas da doença de Ménière9,25-26. Os achados do presente estudo também evidenciaram a atividade da betaistina na redução do zumbido em pacientes com distúrbios vestibulares. Observou-se melhora clínica significante (p<0,0001) em 30,5% pacientes tratados com a betaistina, em comparação com 17,1% casos melhorados no grupo controle.
A melhora do zumbido com o uso da betaistina também tem sido relatada em outros estudos. Em pacientes com doença de Ménière, foi observada redução do zumbido tanto com dimesilato de betaistina (36 mg/dia), como com uma combinação de 20 mg de cinarizina e 40 mg de dimenidrinato, não havendo diferença significante entre os dois grupos de tratamento27. Em outro estudo, o uso durante 5 semanas de uma combinação de mesilato de betaistina, complexo B vitamínico e diazepam reduziu de modo significante o zumbido28. Não é possível estabelecer comparação entre estes achados, pois a presente investigação foi efetuada com dicloridrato de betaistina e com diferente formulação e dosagem.
A betaistina não foi diretamente comparada com outras abordagens farmacológicas no tratamento do zumbido, sendo difícil, portanto, estimar a sua eficácia em relação a outras alternativas. Os antidepressivos são comumente prescritos para zumbido. Existem relatos de casos com o uso de fluoxetina e paroxetina, revisões retrospectivas para imipramina e inibidores seletivos de recaptação da serotonina; estudos com amitriptilina e pesquisas duplo-cegas com trimipramina, nortriptilina, paroxetina e sertralina, em comparação com placebo. Por outro lado, a literatura também menciona que o zumbido pode ser um efeito adverso de medicamentos antidepressivos, tais como fenelzina, amitriptilina, protriptilina, doxepina, imipramina, fluoxetina, trazadone, bupropiona, venlafaxina. O zumbido também pode ser associado com a suspensão dos antidepressivos venlafaxina e sertralina29-31.
A evidência para as abordagens farmacológicas do tratamento do zumbido está sendo construída. Os dados deste estudo sugerem que a betaistina pode ser uma opção terapêutica útil e bem tolerada a ser considerada. Não encontramos outros estudos para comparação pertinente com os nossos achados em pacientes com zumbido e síndromes vestibulares periféricas. São necessários estudos prospectivos controlados para confirmar os presentes resultados.
CONCLUSÃO
A dose de 48 mg/dia de betaistina durante 120 dias consecutivos é útil na redução ou eliminação do zumbido de pacientes com distúrbios vestibulares.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Henry JA, Dennis KC, Schechter MA. General review of tinnitus: prevalence, mechanisms, effects, and management. J Speech Lang Hear Res. 2005;48:1204-3.
2. Nondahl DM, Cruickshanks KJ, Dalton DS, Klein BE, Klein R, Schubert CR, et al. The impact of tinnitus on quality of life in older adults. J Am Acad Audiol. 2007;18:257-66.
3. Pinto PCL, Sanchez TG, Tomita S. Avaliação da relação entre severidade do zumbido e perda auditiva, sexo e idade do paciente. Braz J Otorhinolaryngol. 2010;76(1):18-24.
4. Fornaro M, Martino M. Tinnitus psychopharmacology: A comprehensive review of its pathomechanisms and management. Neuropsychiatr Dis Treat. 2010;6:209-18.
5. Axelsson A. Tinnitus epidemiology. In: Reich GF, Vernon JA, eds. Fifth international tinnitus seminar; 1995; Portland, Oregon. Proceedings. Portland, Oregon: American Tinnitus Association. 1995;12-15.p.249-53.
6. Crummer RW, Hassan GA. Diagnostic Approach to Tinnitus. Am Fam Physician. 2004;69:120-6,127-8.
7. Sanchez TG, Medeiros ÍRT, Levy CP, Ramalho JRO, Bento F. Zumbido em pacientes com audiometria normal: caracterização clínica e repercussões. Braz J Otorhinolaryngol. 2005;71(4):427-31.
8. Ferreira LMBM, Ramos Júnior AN, Mendes EP. Caracterização do zumbido em idosos e de possíveis transtornos relacionados. Braz J Otorhinolaryngol. 2009;75(2):249-55.
9. Lacour M, van de Heyning PH, Novotny M, Tighilet B. Betahistine in the treatment of Ménières disease. Neuropsych Dis Treat. 2007;3:1-12.
10. Patterson MB, Balough BJ. Review of pharmacological therapy for tinnitus. Int Tinnitus J. 2006;12(2):149-59.
11. Elgoyhen AB, Langguth B. Pharmacological approaches to the treatment of tinnitus. Drug Discov Today. 2010;15(7-8):300-5.
12. Seidman MD, Standring RT, Dornhoffer JL. Tinnitus: current understanding and contemporary management. Curr Opin Otolaryngol Head Neck Surg. 2010;18(5):363-8.
13. Møller AR. Tinnitus: presence and future. Prog Brain Res. 2007;166:3-16.
14. Onishi E, Kasse C, Rodrigues C, Oliveira MHP, Aprile MR, Bataglia PUR, Karsch UM. Como diagnosticar e tratar zumbido. Rev Bras Med. 2008;65:32-7.
15. James AL, Burton MJ. Betahistine for Ménières disease or syndrome. Cochrane Database Syst Rev. 2001;(1):CD001873.
16. Ma FR, Xin Y, Zhao YM, Lü JQ. Efficacy of Betahistine Mesilate combined with Flunarizine Hydrochloride for treating tinnitus. Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2006;41:269-73.
17. Gryczyńska D, Drobik-Wasiewicz K, Malicka M, Kotecki M. Therapy of tinnitus in children. Otolaryngol Pol. 2007;61:784-8.
18. Frew IJC, Menon GN. Betahistine hydrochloride in Ménières disease. Postgrad Med J. 1976;52:501-3.
19. Dziadziola JK, Laurikainen EL, Rachel JD, Quirk WS. Betahistine increases vestibular blood flow. Otolaryngol Head Neck Surg. 1999;120:400-5.
20. Dutia MB. Betahistine, vestibular function and compensation: in vitro studies of vestibular function and plasticity. Acta Otolaryngol Suppl. 2000;544:11-4.
21. Lacour M, Tighilet B. Vestibular compensation in the cat: the role of the histaminergic system. Acta Otolaryngol Suppl. 2000;544:15-8.
22. Lacour M, Sterkers O. Histamine and betahistine in the treatment of vertigo: elucidadtion of mechanisms of action. CNS Drugs. 2001;15:853-70.
23. Ganança MM, Munhoz MSL, Caovilla HH, Silva MLG. Managing vertigo. Hannover: Solvay; 2006. p.112.
24. Ganança MM, Caovilla HH, Munhoz MSL, Ganança CF, Silva MLG, Serafini F, et al. Optimizing the pharmacological component of integrated balance therapy. Braz J Otorhinolaringol. 2007;73:12-8.
25. Strupp M, Hupert D, Frenzel C, Wagner J, Hahn A, Jahn K, et al. Long-term prophylactic treatment of attacks of vertigo in Ménière's disease: comparison of a high with a low dosage of betahistine in an open trial. Acta Otolaryngol. 2008;128(5):520-4.
26. Ganança MM, Caovilla HH, Ganança FF. Comparable efficacy and tolerability between twice daily and three times daily betahistine for Ménières disease. Acta Otolaryngol. 2009;129(5):487-92.
27. Novotný M, Kostrica R. Fixed combination of cinnarizine and dimenhydrinate versus betahistine dimesylate in the treatment of Ménières disease: a randomized, double-blind, parallel group clinical study. Int Tinnitus J. 2002;8:115-23.
28. Ohsaki K, Ueno M, Zheng HX, Wang QC, Nishizaki K, Nobuto Y, et al. Evaluation of tinnitus patients by peroral multi-drug treatment. Auris Nasus Larynx. 1998;25:149-54.
29. Robinson SK, Viirre ES, Bailey KA, Gerke MA, Harris JP, Stein MB. Randomized placebo-controlled trial of a selective serotonin reuptake inhibitor in the treatment of nondepressed tinnitus subjects. Psychosom Med. 2005;67:981-8.
30. Robinson S. Antidepressants for treatment of tinnitus. Prog Brain Res. 2007;166:263-71.
31. Robinson SK, Viirre ES, Stein MB. Antidepressant therapy in tinnitus. Hear Res. 2007;226:221-31.
1. Professor Titular de Otorrinolaringologia da Universidade Federal de São Paulo - Escola Paulista de Medicina. Docente do Programa de Mestrado Profissional em Reabilitação do Equilíbrio Corporal e Inclusão Social da Universidade Bandeirante de São Paulo.
2. Livre-Docente em Otoneurologia. Professor Associado, da Disciplina de Otologia e Otoneurologia da Universidade Federal de São Paulo - Escola Paulista de Medicina. Professor Associado, da Disciplina de Otologia e Otoneurologia da Universidade Federal de São Paulo - Escola Paulista de Medicina.
3. Doutora em Ciências pelo Curso de Pós-Graduação em Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da Universidade Federal de São Paulo - Escola Paulista de Medicina. Docente do Programa de Mestrado Profissional em Reabilitação do Equilíbrio Corporal e Inclusão Social da Universidade Bandeirante de São Paulo.
4. Doutora em Ciências pelo Programa Distúrbios da Comunicação Humana pelo Departamento Fonoaudiologia da Universidade Federal de São Paulo - Escola Paulista de Medicina., Doutora em Ciências pelo Programa Distúrbios da Comunicação Humana pelo Departamento Fonoaudiologia da Universidade Federal de São Paulo - Escola Paulista de Medicina.
5. Médico Otorrinolaringologista, Pós-Doutorado pela UNIFESP - EPM. Professor Adjunto, Chefe da Disciplina de Otologia e Otoneurologia da UNIFESP - EPM, Professor Adjunto, Chefe da Disciplina de Otologia e Otoneurologia da UNIFESP - EPM.
Universidade Federal de São Paulo.
Endereço para correspondência:
Maurício Malavasi Ganança
Rua Dr. Eduardo de Souza Aranha, 99 cj. 62
São Paulo - SP. CEP: 04543-120
E-mail: mauricio.gananca@globo.com
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da BJORL em 9 de agosto de 2010. cod. 7255
Artigo aceito em 1 de dezembro de 2010.