Ano: 2003 Vol. 69 Ed. 2 - Março - Abril - (12º)
Seção: Artigo Original
Páginas: 222 a 225
Emissões otoacústicas x Cisplatina: detecção precoce da ototoxicidade em pacientes oncológicos
Otoacoustic emissions x Cisplatin: precocious detection of ototoxicity in oncologic patients
Autor(es):
Ruysdael Zocoli[1],
Sandro Laércio Reichow[2],
Ângela Maria Fontana Zocoli[3]
Palavras-chave: audição, emissão otoacústica evocada, ototoxicidade e cisplatina.
Keywords: hearing, otoacoustic emissions, ototoxicity, cisplatin.
Resumo:
Introdução: Estudos mostram que existem numerosas substâncias reconhecidas como potencialmente ototóxicas e entre as principais, na classe dos medicamentos, destacam-se os quimioterápicos. Objetivo: o objetivo deste trabalho foi realizar um estudo da ototoxicidade através das emissões otoacústicas evocadas - produto de distorção (EOA-PD), pré e pós-aplicação do quimioterápico Cisplatina, em indivíduos adultos, moradores da cidade de Blumenau/SC. Forma de Estudo: Prospectivo clínico. Material e Método: Foram estudados 11 indivíduos com patologia oncológica, idade variando entre 29 e 73 anos, através das emissões otoacústicas evocadas - produto de distorção, prévia e posteriormente à aplicação da Cisplatina, utilizando-se o equipamento Madsen Cappela acoplado ao Notebook Toshiba Satélite. Resultados: Os resultados não mostraram mudanças significativas nas respostas das EOA-PD nas freqüências de 2, 3 e 4 kHz, porém, em 1 e 6 kHz, ocorreram alterações na sensibilidade auditiva, após a aplicação da Cisplatina.
Abstract:
Introduction: Studies show that there are numerous substances known as potentially ototoxic and among the main ones in the medicine classes, stands out the chemotherapeutics. Objective: The objective of this work was to achieve a study of the ototoxicity through otoacoustic emissions - product of distortion (EOA - PD), pre and post-application of the chemotherapeutic Cisplatin, in adults individuals, residents of the city of Blumenau/SC. Study Form: Clinic prospective. Material and Method: There were 11 individuals studied with oncologic pathology, age between 29 and 73 years old, through the otoacoustic emissions - product of distortion, previous and subsequently to the Cisplatin application, using the Madsen Cappela equipment coupled to the notebook Toshiba satellite computer. Results: The results didn't show significant changes on the answers of the EOA - PD on the frequencies of 2, 3 and 4 kHz, however, in 1 and 6 kHz, alterations occurred on the hearing sensitivity after the Cisplatin application.
![]()
Introdução
Desde tempos imemoriais sabe-se que diversas substâncias possuem ação tóxica, podendo afetar um órgão específico ou todo o organismo. Devido à sua sensibilidade e função, as células ciliadas externas são as primeiras estruturas da orelha interna a serem lesadas por agentes externos. Estudos revelam que numerosas substâncias são reconhecidas como potencialmente ototóxicas, sendo em sua grande maioria lesivas à cóclea e em menor proporção ao vestíbulo. A ototoxicidade é definida como a perda parcial ou total da função vestibular e/ou coclear em decorrência do uso de drogas, geralmente com finalidades terapêuticas ou por exposição a substâncias tóxicas e o grau de severidade depende da predisposição individual, dose, duração do tratamento, via de administração, idade, tendência familiar e/ou de eventual dano prévio à orelha interna1-12.
A realização de um estudo genérico em pacientes tratados com drogas ototóxicas mostrou-se amplo, devido à grande variedade das mesmas na classe de medicamentos. Optou-se, então, por estudar, através das emissões otoacústicas, alguns dos efeitos colaterais causados em usuários do quimioterápico Cisplatina.
A Cisplatina (cis-diaminodicloroplatina) é um metal pesado complexo, com um átomo central de platina, cercado por dois átomos de cloro e duas moléculas de amônia na posição cis. É apresentado na fórmula de um pó branco liofilizado, com fórmula molecular PtCl2H6N2, solúvel em água ou salina na concentração de 1mg/ml e em dimetilformamida na concentração de 24mg/ml. (Observação: agulhas ou conjuntos intravenosos, contendo partes de alumínio que possam entrar em contato com Cisplatina não devem ser usados na apresentação ou administração, pois reagem causando formação de precipitado e perda de potência).
Inúmeras são as técnicas que podem ser utilizadas para monitorar a função auditiva durante a administração de drogas ototóxicas. As emissões otoacústicas, como representantes das condições de funcionamento das células ciliadas externas, podem detectar sinais iniciais de danos cocleares e, dessa forma, atuar no monitoramento e prevenção de danos por agentes ototóxicos.12,13 São testes de aplicação clínica recente e vêm assumindo importância significativa na identificação de alterações cocleares, principalmente por se tratar de um exame objetivo, não invasivo e de fácil aplicação. Mesmo não determinando o limiar auditivo e não substituindo a audiometria tonal, a imitanciometria ou a audiometria de tronco encefálico informa dados que nenhum outro método consegue fornecer.14
As emissões otoacústicas evocadas - produto de distorção - são definidas como energia acústica medida no canal auditivo, originada pela interação não-linear de dois tons puros simultâneos aplicados dentro da cóclea.15 Os dois tons puros apresentam-se com duas freqüências diferentes (F1 e F2), que são chamadas de freqüências primárias. Em humanos a mais ampla EOA-PD ocorre na freqüência equivalente a 2F1 - F2 onde F1 > F2.
O objetivo deste estudo foi monitorar através das emissões otoacústicas evocadas, de forma prévia e posterior ao uso da Cisplatina, as condições de funcionamento das células ciliadas externas, buscando detectar sinais de alterações cocleares após o uso da medicação, podendo assim, reavaliar dosagens e atuar na prevenção de outros danos, evitando maiores comprometimentos auditivos.
Material e Método
Trabalho realizado em conjunto pela Clínica de Otorrinolaringologia Blumenau Ltda. - CLIOB, Setor de Oncologia da Policlínica Lindolf Bell e Centro Onco-Hematológico do Hospital Santa Catarina, no período de fevereiro a agosto de 2002. Participaram do estudo 11 indivíduos portadores de patologia oncológica, com e sem queixas auditivas, de ambos sexos e idade variando de 29 a 73 anos.
Utilizou-se, como critério para a seleção, pacientes em início de tratamento quimioterápico, que fizesse uso de Cisplatina. Realizou-se anamnese dirigida, visando conhecer a história audiológica pregressa ao tratamento. Todos os pacientes assinaram o termo de consentimento após serem informados sobre a realização dos testes e a inclusão dos dados no trabalho, conforme comunicado enviado ao CRM-SC.
As testagens das emissões otoacústicas evocadas (produto de distorção) foram realizadas durante o período de hidratação (antes da aplicação da medicação) em todos os pacientes, imediatamente após a aplicação em alguns e com intervalo de uma hora após, nos demais. O protocolo de uso da droga é de quatro aplicações, com intervalo de 21 dias, salvo os casos em que os pacientes apresentam alterações hematológicas. Utilizou-se o equipamento Madsen Cappela acoplado ao Notebook Toshiba Satélite.
Os exames foram realizados na instituição onde o paciente realizava as sessões de quimioterapia. Nem sempre o ambiente encontrava-se acusticamente protegido; procurou-se realizar em local com menor ruído ambiental, levando-se em conta o fato que quanto maior a redução do ruído de fundo, melhores as condições para se medir as EOA. Foram tomados cuidados na adaptação da sonda no meato acústico externo, para que não ocorresse contaminação por ruído ou produção de artefatos. Os pacientes foram testados bilateralmente, avaliando-se as freqüências de 1, 2, 3, 4 e 6 kHz, com intensidade do estímulo sonoro de 65 dB.
Resultados
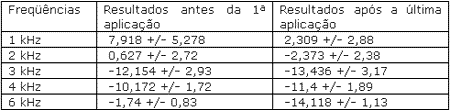
Ao comparar as EOAs pré e pós-aplicação da Cisplatina, constatou-se que as freqüências de 2, 3 e 4 kHz apresentaram menores diferenças nas respostas. No entanto, nas freqüências extremas testadas de 1 e 6 kHz, ocorreram mudanças significativas na sensibilidade auditiva após o uso do quimioterápico.
Foram testados 11 pacientes, 6 durante quatros ciclos de aplicação da Cisplatina (3 com intervalo de vinte e um dias e 3 em sessões semanais), 4 realizaram três ciclos e 1 foi a óbito logo após a primeira sessão.
Dos pacientes testados, 5 referiram presença de zumbido a partir da segunda aplicação da medicação. De acordo com a literatura, a ototoxicidade da Cisplatina manifesta-se primariamente através de tinnitus ou hearing loss, acontecendo em até 31% dos pacientes, sendo seus efeitos cumulativos e irreversíveis.12
Tabela 1. Exame prévio à primeira aplicação da Cisplatina e exame posterior à última aplicação da Cisplatina: médias nas variações das respostas EOA-PD.
Nos exames prévios à aplicação da Cisplatina, 9 pacientes apresentaram alteração nas respostas das EOA-PD. A média de idade foi de aproximadamente 54 anos ±17, tratando-se de uma população adulta e em sua maioria entrando na terceira idade.
A realização do exame imediatamente após ou 1 hora após a aplicação do quimioterápico, ocorreu com o intuito de observar-se à ocorrência de pico máximo de ototoxicidade, o que não se confirmou neste estudo.
Discussão
As drogas ototóxicas podem potencialmente alterar a biomecânica coclear afetando a audição.16 As emissões otoacústicas são testes de grande valia clínica, por mapear a função das células ciliadas externas ao longo do órgão de Córti, possibilitando a identificação do local onde estas se encontram lesadas. É um teste bastante útil para monitorar os estados de riscos para a audição.14
Muitos autores têm pesquisado sobre a ototoxicidade da Cisplatina nos últimos anos; os primeiros relatos constam de 1972. Sua incidência ainda é muito variável na literatura e está relacionada à dose e forma de administração.17 Recentemente foi realizado estudo sobre a ototoxicidade da cisplatina com um grupo de crianças e constatado que as freqüências de 6 e 8 kHz foram as mais afetadas, vindo de encontro aos dados encontrados na presente pesquisa (esta, por sua vez, tem como fator agravante a idade dos pacientes estudados), com ressalva que neste estudo observou-se maior alteração nas freqüências de 1 e 6 kHz. Outros pesquisadores, em estudos realizados com Amicacina, relatam que as freqüências afetadas também foram em 6 e 8 kHz, o que mostra que há concordância com os achados descritos na literatura.18
Um fator considerado significativo foi o índice de presença de zumbido. Alguns autores12 referem que são de ocorrência comum as queixas de zumbidos intensos nos quadros de ototoxicoses e descrevem o acometimento de 31% dos pacientes. Neste estudo foi observado que 46% dos pacientes testados apresentaram zumbido após a segunda aplicação da Cisplatina, permanecendo até o final do tratamento, com poucas queixas de alterações de intensidade ou de freqüência.
Conclusão
Após a análise dos resultados pode-se verificar que os tratamentos realizados com a Cisplatina podem causar alterações no funcionamento das células ciliadas externas. Observaram-se quedas nas respostas, principalmente nas freqüências extremas 1 e 6 kHz, o que faz com que se acredite na importância do monitoramento efetivo com EOA-PD na detecção precoce da ototoxicidade e se pense em readaptações de doses (sem perda da eficiência quimioterápica) mas com menores efeitos sobre o órgão auditivo.
Agradecimentos
Agradecemos aos pacientes que mesmo diante da fragilidade do momento em que se encontravam, permitiram a realização desse estudo, e às equipes de enfermagem das instituições, que se mostraram bastantes solícitas ao bom andamento do trabalho.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Ayala-Martinez L. et al. Correlaciones morfofuncionales de la acion protectora del coenzima A en la ototoxia por cisplatino (II). Acta Otorrinolaringol Esp 1997;48(4):265-7.
2. Cevette MJ et al. Cisplatin ototoxicity, increased DPOEA amplitudes, and magnesium deficiency. Distortion product otoacustic emission. J Am Acad Audiol 2000;11(6):323-9.
3. Kaltenbach JA et al. Comparison of five agents in protecting the cochlea against the ototoxiceffects of cisplatin in the hamster. Otolarygol-Head-Neck-Surg 1997;117(5):493-500.
4. Laurell G et al. Blood-perilymph barrier and ototoxicity: an in vivo study in the rat. Acta Otolaryngol 2000;120(7):796-803.
5. Li L. Experimental study on cisplatinum ototoxicity. Zhonghua er bi yan hou ke za ahi 1990;25(4):205-7, 254.
6. Lou WH et al. Effect of sodium thiosulfate on cisplatin-induced ototoxicity. Zhonghua er bi yan hou ke za ahi 1990;25(4):208-10, 255.
7. Macdonald MR et al. Ototoxicity of carboplatin: comparing animal and clinical models at the Hospital for Sick Children. Otolaryngol 1994;23(3):151-9.
8. Moroso MJ & Blair RL. A review of cis-platinum ototoxicity. J Otolaryngol 1983;12(6):365-9.
9. Ozturan O et al. Monitoring of cisplatin ototoxicity by distortion-product otoacustic emissions. Auris-Nasus-Larinx 1996;23147-51.
10. Schaefer SD et al. Ototoxicity of low and moderate-dose cisplatin. Cancer 1985;56(8):1934-9.
11. Schroder M et al. Cisplatin ototoxicity. A Clinical study. Larynglo Rhinol Otol (Stuttg) 1986;65(2):86-9.
12. Silva MLG, Munhoz MSL, Ganança MM & Caovilla HH. Ototoxicoses. In: Quadros clínicos mais comuns. Vol. III. Cap. 14. Série Otoneurológica. São Paulo: Ateneu; 2000. p. 119-130.
13. Lopes Filho O & Carlos RC. Produto de distorção das emissões otoacústicas. Rev Bras de Otorrinolaringol 1996;5:224-237.
14. Munhoz MSL, Caovilla HH, Silva MLG & Ganança MM. Otoemissões acústicas. In: Audiologia Clínica. Vol. II. Cap. 9. Série Otoneurológica. São Paulo: Ateneu; 2000. p.121-148.
15. Kemp DT. Stimulates acoustic emissions from within the human auditory system. J Acoust Soc Am 1978;64:1386-91.
16. Oliveira JAA, Canedo DM & Rossato M. Otoproteção das células ciliadas auditivas contra a ototoxicidade da amicacina. Rev Bras de Otorrinolaringol 2002;68:7-14.
17. Borges GC, Borges RHM, Baraúna GN & Lopes Filho O. Ototoxicidade causada pela cisplatina em crianças - Estudo retrospectivo. Rev Bras de Otorrinolaringol 2001;67:292-296.
18. Valejjo JC et al. Detecção precoce de ototoxicidade usando emissões otoacústicas produtivas de distorção. Rev Bras de Otorrinolaringol 2001;67:845-851.
19. Boheim K & Bichler E. Cisplatin-induced ototoxicity: audiometric findings and experimental cochlear pathology. Arch-Otorhinolaryngol 1985;242(1):1-6.
20. Lopes Filho O, Carlos RC. Emissões otoacústicas. In: Tratado de Fonoaudiologia. Cap. X. São Paulo: Rocca;1996. p.221-237.
21. Martinez-Martinez MJ et al. Correlaciones morfofuncionales de la acción protectora del ácido pantotenico en la ototoxia por cisplatino (I). Acta Otorrinolaringol Esp 1997;48(4):261-4.
22. Smoorenburg GF et al. Protection and spontaneous recovery from cisplatin-induced hearing loss. Ann-N.Y-Acad-Sci 1999;28:884192-210.
23. Standnicki SW et al. Cis-dichlorodiammineplatinum (II) (NSC-119875): hearing loss and other toxic effects in rhesus monkeys. Cancer chemother 1975; Rep. 59:467-80.
24. Strauss M et al. Cis-platinum ototoxicity: clinical experience and temporal bone histopathology. Laryngoscope 1983;93:1554-9.
25. Taudy M et al. Carboplatin and cisplatin ototoxicity in guinea pigs. Audiology 1992;31(5):293-9.
26. Wright CG & Schaefer SD. Inner ear histopathology in patients treated with cis-platinum. Laryngoscope 1982; 92:1408-13.
[1] Médico Otorrinolaringologista - CLIOB Ltda.
[2] Médico Oncologista (Setor de Oncologia da Policlínica Lindolf Bell e Centro Onco-Hematológico do Hospital Santa Catarina)
[3] Fonoaudióloga - CLIOB Ltda.
Endereço para Correspondência: CLIOB Ltda. - Rua Prefeito Frederico Busch Jr., 255 sala 407 (CELP) Bairro Garcia Blumenau SC 89020-400 - Fone/Fax (0xx47) 322-0302 - E-mail ruysdael@cliob.med.br