INTRODUÇÃONo tratamento do câncer de laringe não avançado, as laringectomias parciais são utilizadas para se preservar algumas das funções vitais da laringe: manutenção da via aérea natural e proteção das vias aéreas inferiores, além de preservar a habilidade vocal. A alteração estrutural na via aérea superior decorrente das laringectomias parciais pode predispor à Apneia Obstrutiva do Sono (AOS), acometendo 81% a 91% destes pacientes
1.
As laringectomias parciais podem ser divididas em laringectomias horizontais (LH) e laringectomias verticais (LV). Nas LH, como na laringectomia supraglótica, toda a supraglote, incluindo epiglote, pregas vestibulares, ventrículos de Morgagni e osso hioide, é removida. Na laringectomia supracricoide, também horizontal, é feita a remoção de toda a supraglote, pregas vocais, região pré-epiglótica e paraglótica e cartilagem tireoide. Pelo menos uma aritenoide deve ser preservada, a fim de preservar a fonação e a função enfincteriana
2. A cricoide é preservada e suturada no hioide. A neoglote passa a se localizar na cricoide. Nestes casos, a região da cartilagem cricoide e aritenoide remanescente é suspensa e fixada à epiglote, reconstrução chamada cricohioidoepiglotopexia (CHEP). Se a epiglote é removida, esta reconstrução se dá pela sutura da cricoide e aritenoides com o hioide, chamada cricohioidopexia (CHP). Já nas LV, a prega vocal, o ventrículo laríngeo, a prega vestibular e a lâmina da cartilagem tireoide do lado da lesão são ressecados, preservando-se pelo menos uma porção da cartilagem tireoide, a fim de preservar a sustentação laríngea. Parte da prega vocal contralateral também pode ser removida e uma das aritenoides pode ser ressecada total ou parcialmente. O pericôndrio externo da cartilagem tireoide ressecada é usado na reconstrução da região removida, formando uma nova parede na laringe
3.
Um estudo notou que a incidência e a gravidade da AOS após LH e LV são semelhantes, apesar da abertura da neoglote ser maior nos pacientes submetidos a LV
1.
A espirometria é utilizada na avaliação da função pulmonar
4,5. Nas curvas fluxo-volume da espirometria, os pacientes com AOS geralmente não apresentam o padrão de obstrução extratorácica da via aérea superior
6 e a doença pulmonar obstrutiva não é um fator de risco independente para AOS
7. Entretanto, este exame detecta anormalidades funcionais quando o diâmetro da faringe ou laringe está reduzido a menos de 8 mm
8-10. Nestes casos, a curva fluxo-volume expiratória pode parecer normal, mas a porção inspiratória da curva mostra-se tipicamente achatada, demonstrando obstrução extratorácica alta.
Uma vez que o tamanho da menor área da laringe parece se correlacionar com a AOS nas laringectomias parciais
1, é possível que a presença de obstrução extratorácica alta à espirometria possa identificar os pacientes laringectomizados parciais que desenvolvem AOS. A prevalência da AOS nesta população de laringectomizados será comparada à prevalência da população geral. Objetivou-se, ainda, comparar a presença e a gravidade da AOS entre os grupos de pacientes submetidos a laringectomias verticais e horizontais e avaliar o papel da espirometria na detecção dos laringectomizados parciais que apresentam AOS.
MÉTODOEste estudo foi aprovado pelo Comitê de Ética em Pesquisa de nossa instituição, com o número de protocolo 001/10. Termo de Consentimento Livre e Esclarecido foi obtido de todos os participantes da pesquisa.
Nós revisamos os prontuários e recrutamos os pacientes submetidos a laringectomias parciais (LH ou LV) no período de 2000 a 2008 no Serviço de Otorrinolaringologia da nossa instituição. Incluímos no estudo pacientes com idade atual acima de 18 anos, submetidos a uma única cirurgia de laringectomia parcial para tratamento de câncer de laringe, com remoção de parte do arcabouço laríngeo e manutenção de via aérea natural na época do estudo. Pacientes que tenham realizado traqueostomia temporária e que mantenham a via aérea natural na época do estudo foram incluídos. Também foram incluídos aqueles que realizaram outros tratamentos para o câncer de laringe, como esvaziamento cervical, radioterapia e/ou quimioterapia.
Excluímos do estudo os pacientes com presença de traqueostomia, mesmo que ocluída, pacientes submetidos exclusivamente à cordectomia, aqueles que apresentaram recidiva local ou regional ou metástase tumoral, aqueles em uso de drogas que alterem o controle neuromuscular, presença de insuficiência cardíaca congestiva (ICC) ou de doença pulmonar com necessidade de oxigenioterapia. Dos 40 pacientes identificados pela revisão de prontuários, seis foram excluídos por apresentar recidiva tumoral, três faleceram por motivos não relacionados ao tumor, quatro apresentavam doença pulmonar obstrutiva crônica com necessidade de oxigenoterapia e dois apresentavam ICC. Três não concordaram em participar do estudo. Um paciente foi excluído pela impossibilidade de decanulação da traqueostomia no pós-operatório. Não conseguimos entrar em contato com sete pacientes. Assim, 14 pacientes participaram deste estudo.
Tratamento utilizado:
Sete pacientes do estudo foram submetidos a laringectomias horizontais e sete a laringectomias verticais.
No grupo LH, quatro pacientes apresentavam-se ao diagnóstico com tumor em estágio T2 e três em estágio T1. Seis foram tratados por meio da laringectomia supracricoide. Um paciente foi tratado com laringectomia supraglótica. Neste grupo, três pacientes receberam radioterapia pós-operatória. Três pacientes receberam esvaziamento cervical eletivo bilateral e quatro, unilateral. Nenhum paciente recebeu quimioterapia pós-operatória. Dos seis pacientes submetidos a laringectomias supracricoides, quatro pacientes foram reconstruídos por meio de CHP e dois por CHEP.
No grupo LV, quatro pacientes foram diagnosticados com tumor em estágio T2 e três em estágio T1. Quatro pacientes submeteram-se à laringectomia frontolateral e três à hemilaringectomia. Dois receberam radioterapia pós-operatória. Três pacientes foram submetidos a esvaziamento cervical eletivo unilateral. Nenhum paciente recebeu quimioterapia pós-operatória. Em três pacientes, foi necessária reconstrução da via aérea com retalho miocutâneo de platisma.
O tempo médio de seguimento desde a finalização do tratamento do câncer de laringe até a avaliação por polissonografia foi de 54 meses, variando de 6 a 84 meses.
Avaliação clínicaAvaliamos o tipo de cirurgia realizada (LH ou LV), as queixas de roncos, a relação temporal entre os roncos e a cirurgia (se prévios, posteriores ou se pioraram após as cirurgias), a circunferência cervical e o índice de massa corporal (kg/m
2). A sonolência diurna foi avaliada pela escala de Epworth, considerando valores superiores a 10 como indicativos da presença de sonolência excessiva. Todos os pacientes foram submetidos à nasofibroscopia para avaliação de recidivas tumorais e tamanho da via aérea laríngea. Nenhum paciente apresentou sinais de recidiva e nem queixas de dispneia. O tamanho da via aérea laríngea foi considerado seguro para manutenção da via aérea natural em todos os casos.
Avaliação polissonográficaTodos os pacientes foram submetidos à polissonografia noturna completa em laboratório do sono. Neste exame, foram monitorados os seguintes parâmetros: eletroencefalograma, eletro-oculograma, eletrocardiograma, eletromiograma de queixo e pernas, fluxo respiratório oronasal através de cânula e termistor, esforço respiratório usando cintas torácicas e abdominais, saturação de oxigênio por oxímetro digital, sensor de ronco e sensor de posição. Os exames foram estagiados segundo os critérios da AASM de 2005
11, utilizando o critério recomendado para detecção das hipopneias.
Analisamos nestes exames o índice de apneia-hipopneia (IAH) e a saturação basal, mínima e média de oxi-hemoglobina.
Avaliação espirométricaOs pacientes foram submetidos à espirometria, com o intuito de pesquisar a presença de obstrução extratorácica alta por meio da demonstração do achatamento típico da curva fluxo-volume inspiratória sempre utilizando-se manobra inspiratória forçada ao final da manobra expiratória
4. Foram obtidas pelo menos três manobras aceitáveis de cada um dos pacientes para garantir a reprodutibilidade do teste. A manobra foi considerada aceitável quando o pico de fluxo expiratório encontrava-se em 10% ou 500 ml do maior pico de fluxo obtido em manobras prévias.
Análise estatísticaUtilizamos testes estatísticos não paramétricos para comparar as duas cirurgias, devido ao pequeno número de casos estudados e também porque a maioria das variáveis analisadas não apresentou distribuição normal. Por coerência com esta análise, a medida de tendência central adotada foi a mediana, seguida pelo respectivo intervalo interquartil. Para efeito de comparação com outros estudos, alguns resultados foram também apresentados pelos valores das médias das variáveis. As comparações entre os dois grupos foram feitas utilizando-se o teste não paramétrico de Mann Whitney. Para a avaliação da influência de outras variáveis nas diferenças obtidas no IAH, foi calculado o coeficiente de correlação não paramétrico Spearman R entre as variáveis de interesse. Adotou-se um nível de significância igual ou inferior a 0,05. As diferenças estatisticamente significantes foram assinaladas, nas tabelas, com um asterisco (*).
RESULTADOSA casuística foi formada por 13 homens e uma mulher. A mediana da idade no momento da avaliação foi de 67,5 anos (interquartil 11 anos), com média de 64,9 anos, variando entre 41 e 81 anos. O IMC mediano foi de 27,3 kg/m
2 (interquartil 5,4 kg/m
2), com média de 25,7 kg/m
2, variando de 19,4 a 29,4 kg/m
2. A circunferência cervical mediana foi de 38,5 cm, variando de 32 a 49 cm, com média de 39,6 cm.
A paciente mulher e 12 homens (92,9%) apresentavam roncos noturnos habituais socialmente incômodos e nove relataram que os roncos tiveram início ou pioraram significativamente após a laringectomia parcial. As avaliações foram realizadas, em média, 67,2 meses após as cirurgias (variando de 9 a 102 meses). Sonolência excessiva (
Epworth > 10) foi observada em quatro pacientes (28%).
O IAH variou de 3,9 a 72,3 com média de 24,0. Treze pacientes (92,9%) apresentaram AOS à polissonografia (IAH > 5). 42,9% apresentaram AOS leve (5 >< iahIAH < 30) e 21,4% AOS grave (IAH > 30). Houve correlação significante do IAH com o IMC (s = 0,76,
p = 0,002), com a CC (s = 0,61,
p = 0,02) e com a pontuação na escala de sonolência de
Epworth (s = 0,77,
p = 0,001). A média da saturação basal, mínima e média da oxi-hemoglobina nestes exames foi de 94%, 89% e 93%, respectivamente.
No exame nasofibroscópico em 12 dos pacientes estudados, foi observado edema em região interaritenoídea com diminuição da luz laríngea. Cinco pacientes pertenciam ao grupo LH e sete ao grupo LV, não sendo esta diferença estatisticamente significativa. No grupo LV, pode-se notar ainda prolapso da estrutura laríngea do lado operado para dentro da luz laríngea em cinco pacientes durante manobra de inspiração forçada.
A espirometria demonstrou obstrução extratorácica alta em 13 dos 14 pacientes. Destes, sete do grupo LV e seis do grupo LH. O paciente com espirometria normal apresentava IAH < 5 (3,9).
Os dados antropométricos, clínicos e polissonográficos dos grupos LH e LV encontram-se na Tabela 1. O IAH do grupo LV foi significantemente maior do que o do grupo LH (
p = 0,004), conforme demonstrado no Gráfico 1. Além disto, o grupo LV teve uma saturação mínima de oxi-hemoglobina significantemente pior e pontuou significantemente mais na escala de Epworth. A CC mostrou-se maior no grupo sujeito a LV, mas não houve diferença estatisticamente significativa. Não houve diferença entre os grupos em relação ao gênero dos pacientes e em relação aos outros parâmetros avaliados.
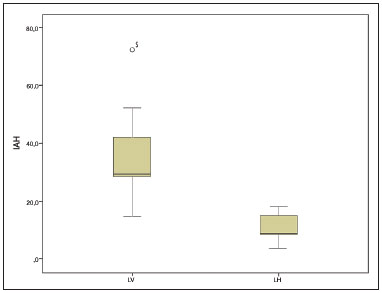
Gráfico 1. IAH: índice de apneia/hipopneia; LV: laringectomias verticais; LH: laringectomias horizontais.
Ao se comparar os pacientes submetidos à radioterapia e aqueles não submetidos, não houve diferença estatisticamente significativa em relação à presença ou à gravidade da AOS. Ao se avaliar o IAH dos pacientes submetidos à radioterapia, os cinco apresentavam IAH maior do que 5, média de 25,1. Entre os nove pacientes não submetidos à radioterapia, 88% apresentavam IAH maior do que 5, com média de 27.01 (
p = 0,06).
DISCUSSÃOApesar dos pacientes submetidos a laringectomias parciais com manutenção da via aérea natural não referirem dispneia durante o dia, o impacto destas cirurgias na respiração durante o sono ainda não é conhecido. Neste estudo, demonstramos que 92,9% dos pacientes submetidos a laringectomias parciais apresentam AOS e que aqueles submetidos à LV possuem AOS significantemente mais grave do que os submetidos a LH. A espirometria detectou obstrução extratorácica na via aérea superior em 92,3% dos casos e o único paciente com espirometria normal não tinha AOS.
Um estudo epidemiológico que avaliou a presença AOS na mesma região, com faixa etária similar aos pacientes de nosso estudo, encontrou prevalência de 34,5%, bem inferior à prevalência no grupo de pacientes laringectomizados por nós avaliados
12.
A associação entre AOS e o tratamento do câncer de cabeça e pescoço tem sido estudada por vários autores. Um estudo
13 encontrou prevalência de 91,7% de casos com IAH > 15 entre 24 pacientes tratados por vários tumores de cabeça e pescoço. Em nosso estudo, a prevalência de IAH maior do que 15 foi de 50%. Esta diferença pode ser atribuída à inclusão de pacientes tratados por tumores de base de língua e faringe naquele estudo, as quais são regiões desprovidas de um arcabouço laríngeo duro e, portanto, mais vulneráveis ao colapso durante o sono.
Como poderíamos explicar a maior gravidade da AOS encontrada no grupo LV em relação ao grupo LH? Exames de tomografia computadorizada da laringe no pós-operatório tardio de laringectomias horizontais demonstram que as dimensões do anel da cartilagem cricoide permanecem inalteradas
14. Há pouca densidade de partes moles no lúmen do anel cricoide após uma LH
15. Além disto, a neoglote encontra-se em posição mais cranial do que a da laringe normal, devido à diminuição do eixo vertical da laringe
13. Esta subida da laringe em direção à hipofaringe, possivelmente, reduz a vulnerabilidade da via aérea à AOS, por encurtar a faringe
16 Já nas LV, há um aumento de partes moles na região pré-epiglótica do lado operado. O maior eixo da glote deixa de ser anteroposterior e gira em direção ao lado ressecado, podendo estreitar a neoglote
17. A neoglote formada nas LV, apesar de apresentar maior espaço aéreo do que nas LH
1, perde metade de sua sustentação pela remoção de uma asa da cartilagem tireoide. Desta forma, a tendência ao colabamento local diante da redução do tônus muscular durante o sono nos parece aumentada nas LV.
Evidentemente, nosso estudo apresenta uma série de limitações. Trata-se de um estudo retrospectivo com uma casuística pequena. Apesar de não termos realizado polissonografias pré-operatórias, 64,3% dos casos referiram início ou piora significativa dos roncos após as cirurgias, indicando uma provável relação de causa e efeito. Para se estabelecer a real correlação entre espirometria e AOS nestes casos, seriam necessários mais casos com espirometria normal, o que nos parece raro devido ao estreitamento da via aérea provocado por uma laringectomia parcial. Devido à faixa etária dos casos tratados e à prevalência de tabagismo nesta população, a incidência de mortes por outras causas, como as cardiovasculares, é frequente, o que, junto com a falta de disposição de alguns pacientes ou familiares em participar do estudo, restringiu a nossa casuística.
Matyja et al.
18 avaliaram a via aérea de 39 pacientes submetidos a LH e 25 submetidos à LV com o uso de espirometria. Notou-se que a maioria, 85% no grupo LH e 72% no grupo LV, apresentava achatamento da curva fluxo-volume sugestivo de obstrução extratorácica alta. Esse achado também foi prevalente na maioria dos pacientes de nosso estudo. Talvez haja um papel para a espirometria na triagem de casos suspeitos de AOS após laringectomias parciais, uma vez que nosso único caso sem AOS foi o único a apresentar espirometria normal. Este exame representa uma maneira simples para se avaliar o impacto funcional do estreitamento cirúrgico da via aérea superior.
CONCLUSÃOObservamos incidência mais alta de AOS entre os pacientes submetidos a laringectomias parciais quando comparados à população geral da mesma faixa etária. A gravidade é maior nos pacientes submetidos a laringectomias verticais do que nos pacientes submetidos a laringectomias horizontais. Mais dados a respeito da espirometria na triagem de casos suspeitos de AOS neste grupo de pacientes devem ser obtidos.
REFERÊNCIAS1. Israel Y, Cervantes O, Abrahão M, Ceccon FP, Marques Filho MF, Nascimento LA, et al. Obstructive sleep apnea in patients undergoing supracricoid horizontal or frontolateral vertical partial laryngectomy. Otolaryngol Head Neck Surg. 2006;135(6):911-6. PMID: 17141083 DOI:
http://dx.doi.org/10.1016/j.otohns.2006.02.0302. Cocek A. The history and current status of surgery in the treatment of laryngeal cancer. Acta Medica (Hradec Kralove). 2008;51(3):157-63.
3. Chawla S, Carney AS. Organ preservation surgery for laryngeal cancer. Head Neck Oncol. 2009;1:12. DOI:
http://dx.doi.org/10.1186/17583284-1-124. Lung function testing: selection of reference values and interpretative strategies. American Thoracic Society. Am Rev Respir Dis. 1991;144(5):1202-18. PMID: 1952453
5. Harber P. Interpretation of lung function tests. In: Simmons DH, ed.. Current Pulmonology. St Louis: Mosby; 1991. p.261-96.
6. Katz I, Zamel N, Slutsky AS, Rebuck AS, Hoffstein V. An evaluation of flow-volume curves as a screening test for obstructive sleep apnea. Chest. 1990;98(2):337-40. DOI:
http://dx.doi.org/10.1378/chest.98.2.3377. Sharma B, Feinsilver S, Owens RL, Malhotra A, McSharry D, Karbowitz S. Obstructive airway disease and obstructive sleep apnea: effect of pulmonary function. Lung. 2011;189(1):37-41. PMID: 21132554 DOI:
http://dx.doi.org/10.1007/s00408-010-9270-38. Lobato JE, Ruocco HH, Oliveira RB, Batista RM. Obstrução fixa das vias aéreas superiores - estudo simulado. J Pneumol. 1981;7:223-6.
9. Lobato JE, Rezende AG, Ruocco HH, Oliveira RB, Batista RM. Curva fluxo volume na obstrução das vias aéreas superiores - relato de 2 casos. J Pneumol. 1990;16(3):149-54.
10. Miller RD, Hyatt RE. Obstructing lesions of the larynx and trachea: clinical and physiologic characteristics. Mayo Clin Proc. 1969;44(3):145-61.
11. Sleep-related breathing disorders in adults: recommendations for syndrome definition and measurement techniques in clinical research. The Report of an American Academy of Sleep Medicine Task Force. Sleep. 1999;22(5):667-89. PMID: 10450601
12. Tufik S, Santos-Silva R, Taddei JA, Bittencourt LR. Obstructive sleep apnea syndrome in the Sao Paulo Epidemiologic Sleep Study. Sleep Med. 2010;11(5):441-6. DOI:
http://dx.doi.org/10.1016/j.sleep.2009.10.00513. Friedman M, Landsberg R, Pryor S, Syed Z, Ibrahim H, Caldarelli DD. The occurrence of sleep-disordered breathing among patients with head and neck câncer. Laryngoscope. 2001;111(11 Pt 1):1917-9. PMID: 11801969
14. Bruno E, Napolitano B, Sciuto F, Giordani E, Garaci FG, Floris R, et al. Variations of neck structures after supracricoid partial laryngectomy: a multislice computed tomography evaluation. ORL J Otorhinolaryngol Relat Spec. 2007;69(5):265-70.
15. Bely-Toueg N, Halimi P, Laccourreye O, Laskri F, Brasnu D, Frija G. Normal laryngeal CT findings after supracricoid partial laryngectomy. AJNR Am J Neuroradiol. 2001;22(10):1872-80.
16. Malhotra A, Huang Y, Fogel RB, Pillar G, Edwards JK, Kikinis R, et al. The male predisposition to pharyngeal collapse: importance of airway length. Am J Respir Crit Care Med. 2002;166(10):1388-95. PMID: 12421747 DOI: http://dx.doi.org/10.1164/rccm.2112072
17. DiSantis DJ, Balfe DM, Hayden R, Sessions D, Sagel SS. The neck after vertical hemilaryngectomy: computed tomographic study. Radiology. 1984;151(3):683-7. PMID: 6718727
18. Matyja G, Zietek E, Kawczyński M, Firlit K, Tarnowska C. Objective assessment of the respiratory function of the larynx after fronto-lateral laryngectomy with epiglottoplasty and after supracricoid laryngectomy with CHP or CHEP. Otolaryngol Pol. 2006;60(3):369-76.
1. Médica (Mestranda Hospital do Servidor Público Estadual de São Paulo)
2. Doutor (Médico Assistente do Hospital do Servidor Público Estadual de São Paulo Médico Assistente do Hospital das Clínicas da Universidade de São Paulo)
Hospital do Servidor Público Estadual de São Paulo.
Endereço para correspondência:
Raquel Chartuni Pereira Teixeira
ca 5, bloco f, torre 4, apto 209. Lago Norte
Brasília - DF. Brasil. CEP: 71503-505
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) do BJORL em 8 de dezembro de 2012. cod. 10651.
Artigo aceito em 18 de julho de 2013.


