INTRODUÇÃOA otosclerose é uma doença limitada à cápsula ótica, que resulta de uma alteração do metabolismo ósseo e se caracteriza pela presença de vários focos de reabsorção e reposição óssea1-3, numa estrutura que, em condições normais, não tem atividade osteoclástica ou osteoblástica1,4,5. Foi descrita pela primeira vez em 1741 por Valsalva, que se deparou com uma anquilose do estribo na autópsia de um doente surdo, e, em 1894, Politzer define a otosclerose como uma entidade clínica1,4. Apesar dos inúmeros trabalhos de investigação desenvolvidos nesta área, a etiologia da otosclerose permanece por esclarecer. A maioria dos autores a considera uma doença multifatorial4. Parece haver predisposição genética com transmissão autossômica dominante, penetrância incompleta (40%) e expressividade variável4, ou surgir de forma esporádica (40%-50%)6.
Os fatores desencadeantes mais frequentemente referidos são o vírus do sarampo, as alterações hormonais (gravidez, metabolismo fosfocálcico, por exemplo) e a autoimunidade4. Aproximadamente 10% da população caucasiana tem características histológicas de otosclerose, mas apenas 10% destes apresentam manifestações clínicas1,4. A localização mais frequente das placas de otosclerose é na região anterior à janela oval (80%-95%)7 e quando a atingem condicionam a uma fixação da platina e consequente hipoacusia de transmissão. Atualmente, o tratamento preconizado é preferencialmente cirúrgico e consiste na estapedectomia ou na estapedotomia2,8, sendo esta última a mais utilizada9 por parecer ter menos complicações associadas10-13, nomeadamente menor agravamento dos limiares ósseos das altas frequências1. Para as duas técnicas estão documentados bons resultados imediatos, mas os resultados a longo prazo são frequentemente questionados. Alguns estudos relatam um limiar ósseo estável após cirurgia, mas outros demonstram perda neurossensorial de vários graus ao longo dos anos9. Na maioria dos casos, esta perda foi interpretada como sendo relacionada com a idade14-17, mas pode resultar do envolvimento do endósteo da cóclea pela própria doença (otosclerose coclear)5,9.
A prótese auditiva convencional é uma alternativa segura e com resultados comparáveis à cirurgia nos doentes com hipoacusia de transmissão pura1,5, embora não se possa dizer o mesmo quando estamos perante uma hipoacusia mista6. A prótese pode ser necessária como tratamento de resgate alguns anos (13 a 30 anos) após a cirurgia18,19. Outra opção são as próteses auditivas osteointegradas, que não implicam fenestração da platina, excluindo-se o risco de cofose1,6. Este trabalho teve como objetivo avaliar os resultados audiométricos pelo menos 10 anos após cirurgia da otosclerose com sucesso imediato documentado.
MATERIAL E MÉTODOSFoi realizado um estudo retrospectivo, no qual foram incluídos os doentes submetidos à estapedotomia/estapedectomia parcial no nosso Serviço, entre novembro de 1998 e janeiro de 2002, com o diagnóstico de otosclerose confirmado na cirurgia e melhoria da audição pós-operatória comprovada por audiograma tonal. Foram excluídas cirurgias de revisão e complicações. Os doentes selecionados foram convocados para reavaliação audiométrica e exame otológico. Foram levantados os dados pessoais, da afecção e da cirurgia efetuada nos respectivos processos clínicos.
Compararam-se os valores obtidos (limiares 500, 1000, 2000, 4000 e 8000 Hz) com os prévios à cirurgia e do pós-operatório imediato. Foi calculada a diferença aéreo-óssea (DAO) para as frequências 500, 1000, 2000 e 4000 Hz e a sua média, e o PTA (
Pure Tone Average) para os limiares aéreos e ósseos das mesmas frequências. Não foi possível cumprir as
Guidelines do
Committee on Hearing and Equilibrium20 no que se refere ao PTA para quatro frequências porque os 3000 Hz não foram incluídos nos audiogramas pré e pós-operatório imediato.
Compararam-se, também, os limiares aéreos e ósseos dos dois ouvidos de doentes com otosclerose bilateral e cirurgia estapédica unilateral após correção do efeito de Carhart (5 dB nos 500 Hz, 10 dB nos 1000 Hz, 15 dB nos 2000 Hz e 5 dB nos 4000 Hz)21 no ouvido não operado. Considerou-se que o ouvido contralateral tinha otosclerose se a otoscopia fosse normal e houvesse hipoacusia de transmissão ou mista com pelo menos 10 dB de DAO em duas ou mais frequências ou 15 dB numa frequência.
Os dados obtidos foram tratados estatisticamente em Excel 2007 e SPSS 17.0. Para comparação estatística dos valores audiométricos pré, pós-operatório imediato (pós-operatório 1) e tardio (pós-operatório 2) foi usado o teste
t Student para amostras emparelhadas ou o teste de
Wilcoxon quando a distribuição da variável não era normal. Para comparação de dois ouvidos do mesmo doente, usou-se o teste
t Student para amostras independentes ou o teste de
Mann-Whitney. Foi considerado um nível de significância estatística de 0,01 (α = 0,01).
A estapedotomia/estapedectomia parcial, no Serviço, é realizada sob anestesia geral por via transcanalar ou endaural. Faz-se uma incisão horizontal na pele do canal a 5-6 mm do ânulus e outras duas verticais às 12 e 6 horas e confecciona-se um retalho tímpanomeatal que permite aceder à caixa do tímpano. Para garantir melhor controle da janela oval, é feita a curetagem da parede posterosuperior do canal, poupando a corda do tímpano. Após confirmação da fixação do estribo, faz-se a platinotomia de segurança, desarticulação incudoestapédica, secção do músculo do estribo, fratura da supraestrutura, alargamento da platinotomia/platinectomia e colocação de uma prótese de politetrafluoretileno (Teflon
®) tipo Causse, com 0,4 a 0,6 mm de espessura e 4,5 a 5,5 mm de comprimento. Consideramos indicação para cirurgia estapédica DAO maior ou igual a 30 dB, com Rinne negativo (512 Hz).
RESULTADOSDos doentes operados no período mencionado, 54 preenchiam os critérios estabelecidos e foram convocados para reavaliação audiométrica. Compareceram 41 doentes (47 ouvidos), 77% (36/47) do sexo feminino, todos de raça caucasiana. A idade média à data do diagnóstico, da cirurgia e da reavaliação foi de 40,4 ± 8,3 (78,7% entre os 30-50 anos), 43,8 ± 9,2 e 55,2 ± 9,1 anos. O sintoma de apresentação mais frequente foi a hipoacusia bilateral (61,7%), isolada (29,8%) ou acompanhada de acufeno (31,9%). A duração mediana dos sintomas foi de 72 meses (1-300 meses). A cirurgia realizada na maioria dos casos foi a estapedotomia (72,3%) por uma equipe cirúrgica constituída por um especialista como cirurgião principal em 65,9% e utilizou-se uma prótese com comprimento de 4,5 mm em 69,2% dos casos. Quarenta e dois por cento (17/41 doentes; 23/47 ouvidos) dos doentes realizaram cirurgia do ouvido contralateral. Dos 24 ouvidos contralaterais que não foram operados, 10 tinham otosclerose, o que perfaz 65,9% (27/41 doentes; 33/47 ouvidos) dos doentes com otosclerose bilateral. Havia história familiar de hipoacusia (presumivelmente otosclerose) em 42,6% dos doentes.
Limiar aéreoO seguimento por audiograma, pós-operatório imediato e tardio foram realizados em mediana aos 4 meses (1-19 meses) e 11 anos (10-14 anos), respectivamente. Encontramos otoscopia normal, após remoção de eventual rolhão de cerúmen, em todos os ouvidos reavaliados. Não havia nenhum doente com adaptação protésica no ouvido operado. Apenas 14,6% (6/41) dos doentes notaram um agravamento subjetivo da audição no seguimento tardio.
Nos limiares aéreos pré-operatórios, verificamos que as frequências mais atingidas são os 500 e 1000 Hz, um sinal típico da otosclerose. Há melhoria dos limiares em todas as frequências no pós-operatório imediato (
p < 0,01). Quando comparamos os limiares pós-operatórios imediatos e tardios verifica-se um agravamento (
p < 0,01) que não alcança os valores pré-operatórios (
p < 0,01), exceto nos 8000 Hz (
p > 0,01) (Figura 1).
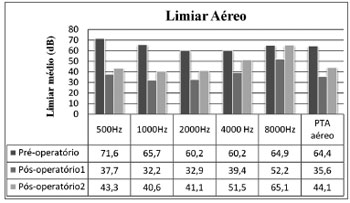
Figura 1. Limares aéreos médios para cada frequência auditiva e PTA aéreo médio.
Os valores médios do PTA aéreo pré, pós e pós-operatório tardios foram 64,4 ± 15,1 dB, 35,6 ± 11,8 dB e 44,1 ± 14,1 dB, respectivamente. Estes valores representam um ganho médio de 28,8 dB do pré para o pós-operatório imediato (
p < 0,01) e um declínio pós-operatório global de 8,5 dB (
p < 0,01). Por fim, verificamos que o valor de PTA aéreo pós-operatório tardio é inferior ao valor pré-operatório (
p < 0,01).
Limiar ósseoNos limiares ósseos pré-operatórios, podemos verificar um maior atingimento das frequências 2000 e 4000 Hz (escotoma de Carhart). Quando comparamos os limiares pré e pós-operatório imediato, assistimos a uma melhoria dos limiares (correção do efeito de Carhart) e apenas não há significância estatística nos 4000 Hz. Verifica-se agravamento de todos os limiares ósseos no pós-operatório tardio (
p < 0,01), sendo este valor pior do que o pré-operatório para todas as frequências (
p > 0,01).
Os valores médios do PTA ósseo, pré, pós e pós-operatório tardios foram 27,0 ± 15,2 dB, 22,3 ± 11,3 dB e 29,6 ± 12,5 dB, respectivamente, o que representa um ganho de 4,7 dB (
p < 0,01) do pré para o pós-operatório imediato, seguido de um declínio global de 7,3 dB (
p < 0,01). Por fim, verificamos que o PTA ósseo pós-operatório tardio é superior ao pré-operatório (
p > 0,01) (Figura 2).
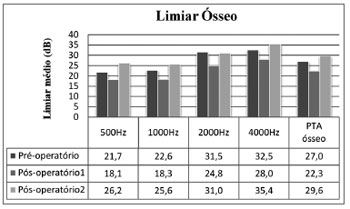
Figura 2. Limares ósseos médios para cada frequência auditiva e PTA ósseo médio.
Verificou-se uma melhoria da DAO em todas as frequências no pós-operatório imediato (
p < 0,01). Esta DAO também se alterou ao longo do tempo, com tendência a aumentar nos 1000, 2000 e 4000 Hz, embora sem significado estatístico, exceto nos 4000 Hz. A DAO média pré, pós e pós-operatória tardia foi de 37,4 ± 9,3, 13,3 ± 5,7 e 14,6 ± 5,6 dB, respectivamente, o que representa uma ganho pós-operatório médio de 24,1 dB (
p < 0,01) e um aumento total no seguimento tardio de 1,3 dB (
p > 0,01). A DAO média pós-operatória tardia não alcança o valor pré-operatório (
p < 0,01) (Figura 3).
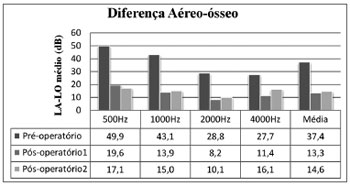
Figura 3. Diferença aéreo-óssea para as frequências e valor médio da sua média. LA: Limiar Aéreo; LO: Limiar Ósseo.
Nos limiares aéreos (LA), constatamos declínio médio anual (LA pós-operatório tardio - LA pós-operatório imediato/anos de
follow-up) após cirurgia de 0,47, 0,74, 0,70, 1,06 e 1,10 dB nas frequências 500, 1000, 2000, 4000 e 8000 Hz.
Em relação aos limiares ósseos (LO), houve declínio médio anual (LO pós-operatório tardio - LO pós-operatório imediato/anos de
follow-up) após cirurgia de 0,4, 0,64, 0,53 e 0,65 nas frequências 500, 1000, 2000 e 4000 Hz.
O declínio anual do PTA, aéreo e ósseo, foi de 0,75 e 0,63 dB, respectivamente. O aumento da DAO médio anual (DAO médio pós-operatório imediato - tardio/anos de
follow-up) foi de 0,12 dB (Figura 4).
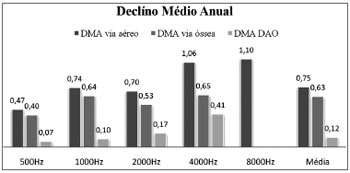
Figura 4. Declínio médio anual (DMA) dos limiares da via aérea, via óssea e diferença aéreo-óssea (DAO) por frequência. A média corresponde ao declínio dos valores médios do PTA aéreo e ósseo e DAO médio.
Verificou-se melhoria do grau de hipoacusia no pós-operatório imediato (
p < 0,01) que reduziu ao longo dos anos sem alcançar os valores pré-operatórios (
p < 0,01). No
follow-up tardio, 49% dos doentes tinham audição normal ou grau de hipoacusia ligeiro (normal (0-25 dB) 4,3% e ligeira (26-40 dB) 44,7%) (Figura 5).
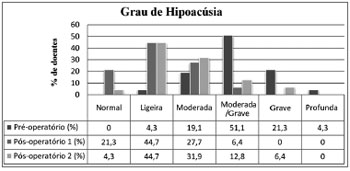
Figura 5. Grau de hipoacusia pré-operatória e pós-operatória imediata (1) e tardia (2).
O PTA aéreo médio dos ouvidos operados e não operados com otosclerose no seguimento tardio foi de 40,8 ± 14,1 e 67,3 ± 16,0 dB, respectivamente, com diferença estatisticamente significativa. Os PTA ósseos médios foram 30,4 ± 11,5 e 35,1 ± 12,4 dB (26,0 ± 12,7 dB após correção de Carhart) nos ouvidos operados e não operados sem diferença significativa (Figura 6).
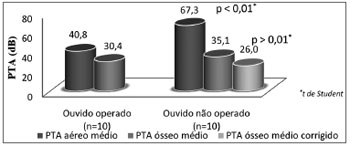
Figura 6. Comparação do PTA aéreo e ósseo dos doentes com otosclerose bilateral e cirurgia estapédica unilateral.
Não se verificou diferença nos resultados pós-operatórios entre os dois sexos, a presença ou não de história familiar, a exposição ou não ao ruído, o tipo de cirurgia, na constituição da equipe cirúrgica (especialista/não especialista) e no comprimento da prótese. O encerramento da DAO é superior (
p > 0,01) nos doentes com mais de 40 anos, mas o PTA aéreo é pior (
p > 0,01).
DISCUSSÃOA maior incidência no sexo feminino, os sintomas de apresentação, a idade à data do diagnóstico e da cirurgia, o atingimento bilateral em 65,9% dos casos e a história familiar em 42,6% dos doentes são sobreponíveis à literatura consultada1,2,4,6,8,9.
A comparação dos valores pré e pós-operatórios imediatos sai do âmbito deste trabalho, uma vez que os doentes selecionados tinham de ter melhoria audiométrica documentada, o que constitui logo de partida um viés de amostragem.
Ao longo dos anos, assiste-se à degradação dos limiares aéreos em todas as frequências, mas mais intensa nas frequências altas (4000 e 8000 Hz), tal como já foi descrito em estudos anteriores2,8, o que pode traduzir o trauma acústico durante a própria cirurgia por aspiração da endolinfa8 ou o resultado do envelhecimento da cóclea. Estes valores não alcançam os valores pré-operatórios. Os limiares ósseos e a DAO também agravam ao longo dos anos. Os limiares ósseos alcançam e ultrapassam os valores pré-operatórios, mas sem significado estatístico, ao contrário da DAO, que se mantém muito inferior à pré-operatória.
O declínio anual do PTA aéreo descrito em estudos anteriores varia entre 0,6 e 2,1 dB6,22. O nosso é de 0,75 dB/ano e deve-se, em grande parte, ao declínio ósseo (0,63 dB/ano) e não à DAO (0,12 dB/ano), compatível com aquilo que seria de esperar para a idade (perda de 1 dB/ano23), como defendem alguns autores4,15,16,17, embora seja tema de grande controvérsia. Para o afirmarmos, teríamos de comparar este grupo com um grupo controle, sem afecção otológica ou fatores de risco, com a mesma distribuição no que diz respeito à idade e sexo.
No final do seguimento, 49% dos doentes tinham audição normal ou um grau de hipoacusia ligeiro e por isso, em princípio, não tinham necessidade de prótese auditiva. Apenas 14,6% notaram agravamento subjetivo da audição, mas nenhum doente tinha adaptação protésica no ouvido operado.
Quando comparamos os ouvidos dos 10 doentes com otosclerose bilateral submetidos à cirurgia em apenas um ouvido, concluímos que, 11 anos após, o PTA aéreo do ouvido operado (aquele que, em regra, terá sido considerado pior inicialmente) é significativamente melhor do que o do ouvido contralateral. O PTA ósseo é pior quando se faz a correção de Carhart, mas sem significado estatístico, ao contrário do que defendem alguns trabalhos, que concluem que a cirurgia condiciona uma progressão mais rápida da surdez neurossensorial9.
Assim, não esquecendo as complicações que podem resultar de uma cirurgia estapédica e que não foram levadas em conta neste trabalho, a cirurgia parece uma opção de tratamento com resultados pelo menos mais duradouros do que uma prótese auditiva que, em 10 anos, provavelmente, já teria tido necessidade de ser substituída pelo menos uma vez pela progressão da doença. Para comparar a eficácia dos dois tipos de tratamento, seria necessário fazer um estudo randomizado de comparação que até ao momento não existe6.
Na comparação de grupos, não obtivemos diferença estatística em nenhum dos grupos, fato que se explica pelo pequeno tamanho da amostra. Talvez por isso, não tenhamos obtido a diferença encontrada em estudos anteriores em relação à faixa etária, que se traduz por pior prognóstico para os indivíduos mais jovens2.
CONCLUSÕESA cirurgia da otosclerose, quando tem benefício pós-operatório imediato, este mantém-se ao longo dos anos. Apesar da queda dos limiares, principalmente nas frequências mais agudas, o grau de hipoacusia, 11 anos depois, é inferior ao pré-operatório. Obtivemos declínio médio anual pós-operatório de 0,75 dB (principalmente à custa da degradação da via óssea), valor semelhante ao calculado para a presbiacusia. A cirurgia melhorou a função auditiva a longo prazo dos ouvidos operados quando comparados com os ouvidos não operados, sendo, por isso, um tratamento a considerar em detrimento da prótese auditiva. De qualquer modo, a decisão cabe ao doente depois de devidamente esclarecido.
REFERÊNCIAS1. Thomas JP, Minovi A, Dazert S. Current aspects of etiology, diagnosis and therapy of otosclerosis. Otolaryngol Pol. 2011;65(3):162-70.
2. Merán Gil JL, Masgoret Palau E, Avilés Jurado FJ, Domènech Vadillo E, Flores Martín JC, Figuerola Massana E. Stapedotomy outcomes in the treatment of otosclerosis: our experience. Acta Otorrinolaringol Esp. 2008;59(9):448-54.
3. Chole RA, McKenna M. Pathophysiology of otosclerosis. Otol Neurotol. 2001;22(2):249-57.
4. Markou K, Goudakos J. An overview of the etiology of otosclerosis. Eur Arch Otorhinolaryngol. 2009;266(1):25-35.
5. Cureoglu S, Baylan MY, Paparella MM. Cochlear otosclerosis. Curr Opin Otolaryngol Head Neck Surg. 2010;18(5):357-62.
6. Merchant SN, McKenna M, Browning G, Rea PA, Tange RA. Otosclerosis. In: Gleeson MJ, Jones NS, Clarke R, Luxon L, Hibbert J, Watkinson J (Eds). Scott-Brown's Otorhinolaryngology, Head and Neck Surgery (7th Ed). London: Edward Arnold; 2008. p.3454-85.
7. Merchant SN, Incesulu A, Glynn RJ, Nadol JB Jr. Histologic studies of the posterior stapediovestibular joint in otosclerosis. Otol Neurotol. 2001;22(3):305-10.
8. Paz Cordovés A, Leyva Montero E, García de Hombre AM, Prieto Zelaya GM. Ear surgery outcomes in patients operated on for otosclerosis. Acta Otorrinolaringol Esp. 2007;58(3):79-82.
9. Redfors YD, Möller C. Otosclerosis: thirty-year follow-up after surgery. Ann Otol Rhinol Laryngol. 2011;120(9):608-14.
10. Kürsten R, Schneider B, Zrunek M. Long-term results after stapedectomy versus stapedotomy. Am J Otol. 1994;15(6):804-6.
11. Quaranta N, Besozzi G, Fallacara RA, Quaranta A. Air and bone conduction change after stapedotomy and partial stapedectomy for otosclerosis. Otolaryngol Head Neck Surg. 2005;133(1):116-20.
12. Levy R, Shvero J, Hadar T. Stapedotomy technique and results: ten years' experience and comparative study with stapedectomy. Laryngoscope. 1990;100(10 Pt 1):1097-9.
13. Fisch U. Stapedotomy versus stapedectomy. Otol Neurotol. 2009;30(8):1166-7.
14. Browning GG, Gatehouse S. Sensorineural hearing loss in stapedial otosclerosis. Ann Otol Rhinol Laryngol. 1984;93(1 Pt 1):13-6.
15. Ramsay HA, Linthicum FH Jr. Mixed hearing loss in otosclerosis: indication for long-term follow-up. Am J Otol. 1994;15(4):536-9.
16. Pirodda E, Modugno GC, Buccolieri M. The problem of the sensorineural component in otosclerotic hearing loss: a comparison between operated and non-operated ears. Acta Otolaryngol. 1995;115(3):427-32.
17. Soudry E, Sulkes J, Attias J, Nageris BI. Bone conduction in otosclerosis-operated versus non-operated ears. J Basic Clin Physiol Pharmacol. 2007;18(3):189-99.
18. Smyth GD, Hassard TH. Hearing aids poststapedectomy: incidence and timing. Laryngoscope. 1986;96(4):385-8.
19. Shea JJ Jr. Forty years of stapes surgery. Am J Otol. 1998;19(1):52-5.
20. Committee on Hearing and Equilibrium guidelines for the evaluation of results of treatment of conductive hearing loss. American Academy of Otolaryngology - Head and Neck Surgery Foundation, Inc. Otolaryngol Head Neck Surg. 1995;113(3):186-7.
21. Carhart R. Clinical application of bone conduction audiometry. Arch Otolaryngol. 1950;51(6):798-808.
22. Kürsten R, Schneider B, Zrunek M. Long-term results after stapedectomy versus stapedotomy. Am J Otol. 1994;15(6):804-6.
23. Langman AW, Jackler RK, Sooy FA. Stapedectomy: long-term hearing results. Laryngoscope.1991;101(8):810-4.
1. Dra. (Medicina/ORL) (Interno ORL - CHVNG/E.EPE).
2. Dra. (Audiologia) (Técnica de Audiologia - CHVNG/E.EPE).
3. Dr. (Medicina/ORL) (Assistente Graduado ORL - CHVNG/E. EPE).
4. Dr. (Medicina/ORL) (Chefe de Serviço ORL - CHVNG/E.EPE).
Centro Hospitalar de Vila Nova de Gaia/Espinho. EPE.
Endereço para correspondência:
Teresa Bernardo
Rua Conceição Fernandes. Vila Nova de Gaia
Portugal. CEP: 4434-502
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da BJORL em 9 de abril de 2012. cod. 9148.
Artigo aceito em 26 de abril de 2012.


