INTRODUÇÃOA saliva exerce papel muito importante na manutenção das funções orais. A perda ou diminuição do fluxo salivar podem dificultar o exercício de funções como mastigação, fala e deglutição e está associada com um impacto negativo na qualidade de vida do paciente. A habilidade das glândulas salivares em concentrar iodo as torna potenciais alvos durante e após a iodoterapia1.
Complicações agudas graves com a iodoterapia são extremamente raras. Entretanto, efeitos colaterais a médio e longo prazos são bem descritos na literatura como sialodenite, perda temporária do paladar, xerostomia e cáries1-3.
Xerostomia é a sensação de boca seca relatada pelo paciente4. A xerostomia pode ser causada por diversos fatores como doenças locais e sistêmicas, diversos medicamentos, radiação e quimioterapia. Alexander et al.2 e Caglar et al.5 relataram taxas de xerostomia associadas à iodoterapia tão altas quanto 42.9% e 54%, respectivamente, normalmente 1 ano após a terapia. Nossos estudos têm mostrado que 11.2% dos pacientes submetidos à iodoterapia têm persistido com queixas de xerostomia durante todo o dia (dados não publicados).
O tratamento da xerostomia é difícil e pode ser alcançado com o alívio sintomático pela administração de gomas de mascar sem açúcar, hidratação frequente, substitutos salivares e sialogogos. A pilocarpina é um agente parassimpatomimético com propriedades β-adrenérgicas que estimula os receptores colinérgicos na superfície das glândulas exócrinas, causando uma redução nos sintomas de xerostomia. Efeitos adversos graves são raros com o uso da pilocarpina, mas efeitos colaterais como sudorese, aumento da frequência urinária e rubor são comuns, com intensidade tipicamente média a moderada por um período curto de duração6.
O objetivo deste estudo piloto é descrever a eficácia e a viabilidade da pilocarpina no tratamento de xerostomia em pacientes submetidos à iodoterapia.
PACIENTES E MÉTODOSEste artigo é parte de um grande estudo transversal retrospectivo, com coleta prospectiva de alguns dados, que teve por critérios de inclusão: pacientes tratados por carcinoma bem-diferenciado de tireoide, submetidos ou não à iodoterapia adjuvante entre 1997 e 2006, em seguimento no ambulatório de Cirurgia de Cabeça e Pescoço do Hospital A. C. Camargo, para avaliação de possíveis efeitos colaterais da iodoterapia sobre a função das glândulas salivares. Quatrocentos pacientes, que preencheram os critérios de inclusão, foram convidados e destes, 184 pacientes aceitaram participar do estudo e assinaram o termo de consentimento aprovado pelo Comitê de Ética em Pesquisa da Instituição (processo n° 762/06). Cento e oitenta pacientes eram portadores de carcinoma papilífero e somente 4 pacientes eram portadores de carcinoma folicular. A média de idade dos pacientes foi de 49.9 anos e a idade mediana de 49 anos (25-89 anos). Cento e oito (58.7%) pacientes foram submetidos à iodoterapia adjuvante. Setenta e oito (42.4%) pacientes faziam uso de algum tipo de medicação xerostômica (anti-hipertensivo, anti-histamínico, antidepressivo). Todos os pacientes foram submetidos à sialometria e cintilografia de glândulas salivares.
Sialometria foi realizada como descrito por Koseki et al.7, e saliva total não estimulada foi coletada em tubo Falcon de 15 ml por 5 minutos e o volume total divido por 5 para se obter o fluxo em ml/min. Para o fluxo salivar total estimulado foi fornecido ao paciente uma pastilha de ácido cítrico (Cewin®, Sanofi-Synthelabo, Brasil), o mesmo foi orientado a não mastigar a pastilha, e a saliva coletada com a mesma técnica descrita anteriormente. Os parâmetros de normalidade adotados foram baseados nos dados publicados por Jensen et al. (fluxo não-estimulado > 0.3 ml/min; estimulado > 1.5 ml/min)4.
Para verificar a eficácia da pilocarpina no tratamento da xerostomia em pacientes submetidos à iodoterapia, adotaram-se os seguintes critérios de inclusão: pacientes submetidos à iodoterapia adjuvante apresentando ao mesmo tempo 1-queixa de xerostomia, 2-valores anormais de fluxo salivar à sialometria4 e 3-disfunção à cintilografia de glândulas salivares pela análise visual. Pacientes que apresentassem contraindicações para o uso da pilocarpina como asma, hipertensão, doenças cardíacas e glaucoma de ângulo fechado não participariam do estudo. Pressão arterial foi aferida antes do início do tratamento, o qual consistiu na administração de 5 mg de pilocarpina 3 vezes ao dia como recomendado pela literatura6, principalmente antes das refeições e a noite, durante 1 semana. Os pacientes preencheram um questionário controle sobre os efeitos colaterais e relataram todos os sintomas durante 7 dias.
RESULTADOSDos 108 pacientes submetidos à iodoterapia adjuvante, 65.4% (70 pacientes) relataram xerostomia pelo menos um período do dia e 11.2% (12 pacientes) durante todo o dia. Destes 70 pacientes, somente 9 pacientes preencheram os critérios de inclusão para o protocolo de tratamento com pilocarpina. A média de idade dos pacientes foi 52.1 anos e a idade mediana 56 anos (36-65 anos). A dose média de iodo recebida durante a iodoterapia foi de 150 mCi (100-450 mCi). Destes nove pacientes, quatro não foram incluídos no estudo. Um paciente não aceitou participar do protocolo, e três pacientes apresentaram hipertensão arterial não controlada. Os dados dos pacientes incluídos no protocolo de pilocarpina estão sumarizados na Tabela 1.
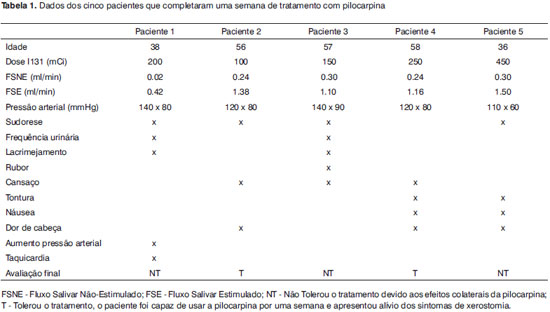
O efeito colateral mais comumente relatado pelos pacientes foi a sudorese, afetando 4 dos 5 pacientes. Cansaço e dor de cabeça foram relatados por 3 dos 5 pacientes. Aumento da frequência urinária, lacrimejamento, calafrios, tontura e náusea foram constatados em 2 dos 5 pacientes. Alterações na pressão arterial e taquicardia foram observados em um mesmo paciente. Avaliando o alívio da xerostomia após o uso da pilocarpina, dois pacientes relataram melhora significativa na sensação de boca seca, mas um deles apresentou diversos efeitos colaterais considerando o uso por longo período inaceitável.
DISCUSSÃODiferentemente da radioterapia externa, a iodoterapia com I131 não destrói completamente a habilidade das glândulas salivares em produzir saliva, preservando assim parênquima funcionante para responder a estímulos. Xerostomia é relatada estar presente em 11 a 54% dos pacientes submetidos à iodoterapia2,5. Como os tumores bem-diferenciados de tireoide apresentam um bom prognóstico, a redução dos efeitos colaterais tardios da iodoterapia é essencial para manter a qualidade de vida destes pacientes.
Ao contrário da radioterapia externa, a qual apresenta diversos estudos mostrando a eficácia da pilocarpina no estímulo das glândulas salivares8-15, faltam estudos na literatura mostrando a eficácia da pilocarpina para aliviar os sintomas de xerostomia associada à iodoterapia. Silberstein16 publicou resultados com o uso de 5 mg de pilocarpina de 8 em 8 horas em um estudo cego, controlado com 60 pacientes por uma semana logo após a iodoterapia na tentativa de prevenir a ocorrência de sialodenite associada ao I131. Este estudo mostrou que a pilocarpina não reduz a ocorrência de sialodenite causada pelo iodo radioativo. Estes resultados confirmam dados publicados por Alexander et al.2 dez anos atrás, o qual não observou diferença significativa entre pacientes que receberam pilocarpina durante a iodoterapia e aqueles que não receberam.
Objetivando mostrar uma outra aplicação da pilocarpina, Aframian et al.17 publicaram um estudo mostrando a eficácia de uma única dose de 5 mg de pilocarpina para aumentar fluxo salivar não-estimulado e estimulado em cinco pacientes portadores de câncer de tireoide submetidos à iodoterapia adjuvante há pelo menos 3 meses antes da realização do estudo. Os resultados mostraram significante aumento do fluxo salivar não-estimulado e estimulado em quatro pacientes, sem alterações significativas das pressões sistólica e diastólica, pulso e temperatura corporal. Até o momento, não há na literatura estudos utilizando a pilocarpina como tratamento a longo prazo para alívio da xerostomia associada à iodoterapia, nem avaliando a tolerabilidade deste medicamento nestes pacientes.
CONCLUSÕESO presente estudo mostra resultados não favoráveis ao uso da pilocarpina como tratamento de rotina para estes pacientes. Os efeitos colaterais com 3 doses de 5 mg ao dia por uma semana não foram bem tolerados por pacientes com câncer de tireoide e o uso desta medicação não deve ser recomendado, visto que os benefícios não sobrepujam os efeitos colaterais.
AGRADECIMENTOSFundação de Amparo à Pesquisa do Estado de São Paulo - FAPESP pelos financiamentos 05/60474-0 e 06/50061-2.
REFERÊNCIAS BIBLIOGRÁFICAS 1. Newkirk KA, Ringel MD, Wartofsky L, Burman KD. The role of radioactive iodine in salivary gland dysfunction. Ear Nose Throat J. 2000;79(6):460-8.
2. Alexander C, Bader JB, Schaefer A, Finke C, Kirsch CM. Intermediate and long-term side effects of high-dose radioiodine therapy for thyroid carcinoma. J Nucl Med. 1998;39(9):1551-4.
3. Bushnell DL, Boles MA, Kaufman GE, Wadas MA, Barnes E. Complications, sequela and dosimetry of iodine-131 therapy for thyroid carcinoma. J Nucl Med. 1992;33(12):2214-21.
4. Jensen SB, Pedersen AM, Reibel J, Nauntofte B. Xerostomia and hypofunction of the salivary glands in cancer therapy. Support Care Cancer. 2003;11(4):207-25.
5. Caglar M, Tuncel M, Alpar R. Scintigraphic evaluation of salivary gland dysfunction in patients with thyroid cancer after radioiodine treatment. Clin Nucl Med. 2002;27(11):767-71.
6. Koseki M, Maki Y, Matsukubo T, Ohashi Y, Tsubota K. Salivary flow and its relationship to oral signs and symptoms in patients with dry eyes. Oral Dis. 2004;10(2):75-80.
7. Fox PC. Salivary enhancement therapies. Caries Res. 2004;38(3):241-6.
8. LeVeque FG, Montgomery M, Potter D, Zimmer MB, Rieke JW, Steiger BW, et al. A multicenter, randomized, double-blind, placebo-controlled, dose-titration study of oral pilocarpine for treatment of radiation-induced xerostomia in head and neck cancer patients. J Clin Oncol. 1993;11(6):1124-31.
9. Hamlar DD, Schuller DE, Gahbauer RA, Buerki RA, Staubus AE, Hall J, et al. Determination of the efficacy of topical oral pilocarpine for postradiation xerostomia in patients with head and neck carcinoma. Laryngoscope. 1996;106(8):972-6.
10. Zimmerman RP, Mark RJ, Tran LM, Juillard GF. Concomitant pilocarpine during head and neck irradiation is associated with decreased posttreatment xerostomia. Int J Radiat Oncol Biol Phys. 1997;37(3):571-5.
11. Horiot JC, Lipinski F, Schraub S, Maulard-Durdux C, Bensadoun RJ, Ardiet M, et al. Post-radiation severe xerostomia relieved by pilocarpine: a prospective French cooperative study. Radiother Oncol. 2000;55(3):233-9.
12. Leek H, Albertsson M. Pilocarpine treatment of xerostomia in head and neck patients. Micron. 2002; 33(2): 153-5.
13. Haddad P, Karimi M. A randomized, double-blind, placebo-controlled trial of concomitant pilocarpine with head and neck irradiation for prevention of radiation-induced xerostomia. Radiother Oncol. 2002;64(1):29-32.
14. Gorsky M, Epstein JB, Parry J, Epstein MS, Le ND, Silverman S Jr. The efficacy of pilocarpine in cancer patients with hyposalivation following radiation therapy. Oral Surg Oral Med Oral Pathol. 2004;97(2):190-5.
15. Mosqueda-Taylor A, Luna-Ortiz K, Irigoyen-Camacho ME, Díaz-Franco MA, Coll-Muñoz AM. Efecto del clorhidrato de pilocarpina como estimulante de la producción salival en pacientes sometidos a radioterapia de cabeza y cuello. Med Oral. 2004;9(3):204-11.
16. Silberstein EB. Reducing the incidence of 131I-induced sialadenitis: the role of pilocarpine. J Nucl Med. 2008;49(4):546-9.
17. Aframian DJ, Helcer M, Livni D, Markitziu A. Pilocarpine for the treatment of salivary glands' impairment caused by radioiodine therapy for thyroid cancer. Oral Dis. 2006;12(3):297-300.
1. Doutora, Estomatologista.
2. Livre Docente, Diretor do Departamento de Cirurgia de Cabeça e Pescoço e Otorrinolaringologia, Hospital A. C. Camargo.
Hospital A. C. Camargo
Endereço para correspondência:
Luiz Paulo Kowalski
Hospital A.C. Camargo Departamento de Cirurgia de Cabeça e Pescoço e Otorrinolaringologia
Rua Professor Antônio Prudente, 211
São Paulo Brasil 01509-900
Tel: (55)(0xx11) 2189-5172 Fax: (55)(0xx11) 3341-0326
E-mail: lp_kowalski@uol.com.br
FAPESP - Fundação de Amparo à Pesquisa do Estado de São Paulo processos 05/60474-0 e 06/50061-2
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da BJORL em 9 de novembro de 2009. cod. 6777
Artigo aceito em 31 de janeiro de 2010


