INTRODUÇÃOO Hidrato de cloral (HC) é uma droga bem estabelecida como sedativa e hipnótica e usada em procedimentos pediátricos e odontológicos devido ao pouco efeito depressor sobre o sistema respiratório e cardíaco1. Apesar disso, casos de arritmias cardíacas e morte súbita em crianças, em especial nas com apneia obstrutiva, são descritos na literatura2, principalmente com o uso de altas doses, provavelmente pelo acúmulo de tricloroetanol sérico, um metabólito intermediário oriundo do metabolismo hepático da droga1. Uma possível ação carcinogênica, já observada em cobaias, também é citada3, apesar de não comprovada em humanos1.
Dentre as complicações menos graves estão a agitação paradoxal, náuseas e vômitos e a sonolência excessiva2.
O HC é uma das drogas de escolha para a sedação de crianças submetidas à captação dos Potenciais Elétricos Auditivos de Tronco Encefálico (PEATE), onde qualquer movimento ou contração muscular pode gerar artefatos interferindo na análise4.
Um sono profundo com duração média de uma hora é induzido rapidamente na dependência da dose usada não deixando sonolência residual após esse período, no entanto, não há um consenso na literatura sobre qual é a melhor dose, podendo esta variar de 40 a 100mg/kg2,4-7. Deste modo, desenvolvemos essa pesquisa com o objetivo de se avaliar a eficácia do HC como sedativo para captação do PEATE em crianças e sistematizar o seu emprego na prática diária.
MATERIAL E MÉTODOO projeto foi aprovado pela comissão de ética em pesquisa da instituição (protocolo 297/2008).
Foi realizado um estudo prospectivo transversal com 41 crianças, sem histórico de doença cardíaca e ou pulmonar grave, entre 01 e 11 anos; idade média de 3,75 anos e desvio padrão de ± 2,25 anos, sendo 46,34% do sexo feminino e 53,66% do sexo masculino, encaminhadas consecutivamente para a realização de PEATE sob sedação.
Foram incluídas somente crianças que não obtiveram sucesso na tentativa prévia de realizar o exame sob sono natural e com peso menor ou igual a 30kg. Foram excluídas crianças com doenças cardíacas e ou pulmonares graves que contraindicavam o uso do HC segundo o clínico responsável por cada paciente e crianças em uso de drogas com ação sobre o sistema nervoso central que não foram liberadas pelo neurologista e/ou psiquiatra.
Todos os participantes estavam de jejum há pelo menos 6 horas e com recomendação de privação de sono para facilitar o efeito da droga.
A dose inicial de HC a 10% foi de 50mg/kg com reforço de 6mg/kg administrado após 30 minutos nos casos onde não houve sedação. Os pacientes foram monitorados com oxímetro e a sala de procedimento equipada para atendimento de complicações respiratórias (cânula orofaríngea, bolsa valva-máscara com reservatório de oxigênio, máscara facial infantil, tubo endo-orotraqueal infantil, laringoscópio com lâminas retas e curvas, cânulas de aspiração, cateter nasal, material para acesso venoso, medicamentos para atendimento de parada respiratória).
A efetividade da droga foi determinada pela indução do sono até 1 hora após a administração da dose inicial. A ocorrência de sono foi correlacionada com as doses (50mg ou 56mg/kg), com as faixas etárias (< 2 anos, de 2 a 5 anos e > 5 anos), com as faixas de peso (<13Kg, de 13 a 19Kg e >19Kg) e com o sexo, utilizando-se os testes estatísticos pertinentes segundo a análise estatística (teste de Levene: teste de comparação de duas ou mais populações segundo a homogeneidade de variâncias, e qui-quadrado: teste para amostras com variáveis nominais em duas ou mais categorias) e aceito um nível de significância de 5%.
RESULTADOSTodas as 41 crianças que participaram do estudo tomaram 50mg/kg e 23 dormiram em 30 minutos. Duas crianças (4,88%) tiveram complicações respiratórias com dessaturação dos níveis de oxigênio sanguíneo (<90%) ainda em estado de sonolência mas acordadas. A dessaturação foi rapidamente revertida com aumento do suprimento de oxigênio por máscara facial e o protocolo foi suspenso. 16 crianças tomaram reforço de 6mg/kg (total de 56mg/kg) e 13 dormiram em mais 30 minutos. A dose de 50mg/kg seguida de 6mg/kg apresentou um efeito estatisticamente significante na indução do sono em relação à dose de 50mg/kg (p<0,05).
Não houve correlação significativa entre indução do sono e idade (p=0,170), entre indução do sono e peso (p=0,51) e entre indução de sono e sexo (p=0,142). Na Figura 1, vê-se um mapa perceptual onde se compara as variáveis relativas da amostra, ou seja, faixas etárias, faixas de peso, se foi dado o reforço de 6mg/kg ou não e se o efeito foi satisfatório (indução do sono) ou não. O resultado indica que não há uma visível associação entre as respectivas variáveis quando analisadas de forma combinada já que não se formam, no gráfico, conglomerados (clusters) entre as diversas marcações representativas de cada variável mencionada.
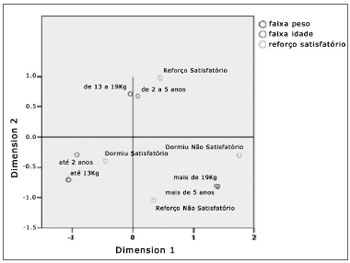
Figura 1. Mapa perceptual das variáveis relativas a faixas etárias, faixas de peso e se houve ou não reforço com efeito satisfatório ou não.
Apesar de o HC ser uma das drogas de escolha para sedação de crianças submetidas a procedimentos otorrinolaringológicos como Nasofibroscopia5 e PEATE, pouco se discute sobre a sua dose efetiva e sobre os seus efeitos colaterais. O HC é metabolizado em tricloroetanol e ácido tricloroacético que são responsáveis pela toxicidade aguda dessa droga. O tricloroetanol tem uma meia vida de 9 a 40 horas dependendo da idade do paciente e da maturidade de seu organismo, já o ácido tricloroacético é ainda detectado 6 dias após a administração de uma única dose de 50mg/kg3 . Portanto, nos casos de falha da sedação para a realização do exame ou da necessidade de se repetir o procedimento, não recomendamos que uma nova administração do HC seja feita em um intervalo menor que uma semana.
A grande vantagem do uso do HC é a indução relativamente rápida da sedação, principalmente se associada com privação de sono, e a ausência de sonolência residual após esse período, proporcionando que a criança seja rapidamente acordada somente aumentando os estímulos externos, diferentemente de outras drogas depressoras do Sistema Nervoso Central2. A literatura, no entanto, sugere que o HC seja eleito como droga sedativa para procedimentos em crianças somente até os 46 meses de idade e/ou peso entre 25 a 30kg, sendo que, além dessas faixas, outra droga deve ser escolhida visando bom efeito sedativo e segurança em relação aos efeitos tóxicos2.
Concordamos com a literatura em manter a faixa máxima de peso em 30kg mas, em função da impossibilidade de usarmos outras drogas depressoras do SNC em nosso serviço, temos administrado o HC para crianças mais velhas. Nossos resultados não mostram diferenças estatísticas comparando-se o efeito satisfatório, ou seja a indução de sono, com a idade dos pacientes, tanto para dose de 50mg/kg como para dose de 56mg/kg. Também não encontramos resultados significativos comparando-se a sedação com o sexo e o peso dos participantes, mas reforçamos novamente que não administramos HC na dose de 50mg/kg e/ou 56mg/kg para crianças com mais de 30kg.
A indução do sono com a dose total de 56mg/kg foi estatisticamente mais significativa em comparação com a dose de 50mg/kg, apesar da amostra com a dose menor ser maior e, mesmo com a literatura recomendando doses entre 40 a 100mg/kg2,4-7, acreditamos que a dose de 56mg/kg dentro do protocolo proposto de se administrar primeiramente 50mg/kg e se necessário um reforço de 6mg/kg, traz um bom resultado, não necessitando de doses maiores.
Duas crianças (4,88% da amostra) apresentaram depressão respiratória (<90% de saturação) com a dose de 50 mg/kg revertida com o uso de oxigênio administrado por máscara facial. Essa porcentagem está muito próxima à descrita na literatura (5,3%) mesmo com amostras maiores (854 pacientes)8 e com doses consideradas seguras (65± 13mg/kg). A grande maioria desse tipo de complicação se resolve com aumento do aporte de oxigênio por máscara ou cateter nasal, mas procedimentos mais invasivos podem ser necessários. Em função dessas possíveis intercorrências é mandatória uma sala de exame minimamente equipada para controle clínico do paciente e com material para atendimento de depressão respiratória, além de um médico treinado para atendimento inicial desse tipo de complicação8.
Em todos os casos de complicações respiratórias é altamente recomendada a suspensão do procedimento para maior controle do paciente e foi por isso que não demos seguimento ao protocolo com as duas crianças que apresentaram dessaturação. Vale ressaltar também que eventos respiratórios adversos podem ocorrer mesmo após o fim do procedimento8 e com a criança acordada na sala de recuperação. Deste modo, recomendamos o monitoramento da mesma por pelo menos 1 hora após ó término da sedação.
Complicações como agitação paradoxal e vômitos são descritas e presentes em cerca de 2% dos pacientes que recebem o HC, apesar de não termos registrado, nesta amostra específica, essas intercorrências. Outras complicações relacionadas com o uso do HC como hipotensão, bradicardia e taquicardia supraventricular são descritas nos casos de sedação para procedimentos invasivos como cateterização cardíaca e em crianças com alto risco anestésico (ASA III e IV)8.
CONCLUSÃOPodemos concluir que dentro do protocolo proposto a dose total de 56mg/kg (50mg/kg seguida de um reforço de 6mg/kg) mostrou-se mais efetiva na indução da sedação que somente a dose de 50mg/kg e que esse reforço deve ser considerado para os casos onde não ocorreu a sedação em 30 minutos após a administração do HC a 50mg/kg. Eventos adversos como complicações respiratórias podem ocorrer independentemente da dose usada, exigindo monitorização do paciente e material adequado para atendimento.
REFERÊNCIAS BIBLIOGRÁFICAS1. Merdink JL, Robison LM, Stevens DK, Hu M, Parker JC, Bull RJ. Kinectics of chloral hydrate and its metabolites in male human volunteers. Toxicology. 2008;245:130-40.
2. Malis DJ, Burton DM. Safe pediatric outpatient sedation: The chloral hydrate debate revisited. Otolaryngol Head Neck Surg. 1997;116(1):53-7.
3. American Academy of Pediatrics, Committee on Drugs and Committee on Environmental Health. Pediatrics. 1993;92(3):471-3.
4. Jerger J, Hayes D, Jordan C. Clinical experience with auditory brainstem response audiometry in pediatric assessment. Ear Hear. 1980;1(1)19-3.
5. Patrocínio JA, Patrocínio LG, Amaral PM, Aguiar ASF, Patrocínio TG. Avaliação da eficácia do hidrato de cloral na sedação de crianças para exame nasofibroscópico. Rev Bras Otorrinolaringol. 2001;67(5):22-7.
6. Costa LRRS, Costa PSS, Lima ARA. A randomized double-blinded trial of chloral hydrate with or without hydroxyzine versus placebo for pediatric dental sedation. Braz Dent J. 2007;18(4):334-40.
7. Reich DS, Wiatrak BJ. Methods of sedation for auditory brainstem response testing. Int J Pediatr Otorhinolaryngol. 1996;38:131-41.
8. Malviya S, Voepel-Lewis T, Tait AR. Adverse events and risk factors associated with the sedation of children by nonanesthesiologists. Anesth Analg. 1997;85:1207-13.
1. Doutora em Ciências pela Otorrinolaringologia pela FMUSP, Médica Otorrinolaringologista DERDIC/PUCSP e HSPM.
2. Especialista em Otorrinolaringologia pela ABORL-CCF, Médica Otorrinolaringologista DERDIC/PUCSP.
3. Especialista em Otorrinolaringologia pela ABORL-CCF, Médico Otorrinolaringologista.
4. Mestre em Distúrbios da Comunicação PUC/SP, Médico Foniatra-Diretor clínico, DERDIC/PUCSP.
5. Especialista em Foniatria PUC/SP, Médico Foniatra DERDIC/PUCSP.
Setor de Otorrinolaringologia e Foniatria da DERDIC/PUCSP
Endereço para correspondência:
Mariana Lopes Fávero - Rua Itapeva 378 conj. 112 Bela Vista
São Paulo SP 01332-000.
E-mail: lopessquare@ig.com.br
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da BJORL em 12 de agosto de 2009. cod. 6565
Artigo aceito em 20 de novembro de 2009


