INTRODUÇÃOAs lesões do tecido ósseo podem ser causadas por traumatismos, infecções, neoplasias ou decorrentes de deformidades congênitas. Os traumas crânio-maxilo-faciais são responsáveis por um número expressivo nos atendimentos de urgência e emergência e em alguns casos evoluir com sequelas e comprometimento estético e funcional, necessitando em algumas ocasiões de tratamento cirúrgico e da utilização de biomateriais.
Durante muito tempo a utilização desses materiais aconteceu de maneira empírica e esperava-se apenas que o material fosse biologicamente inerte e com resistência mecânica adequada para a recuperação ou reconstrução do órgão.
Os aspectos biológicos importantes dos enxertos autógenos foram descobertos na segunda metade do século XX como, por exemplo, a proteína morfogenética do osso1.
Os enxertos autógenos necessitam de uma área doadora, aumentando a morbidade e o risco do tratamento, e nem sempre é possível obter um volume suficiente para preencher o defeito ósseo existente, o que requer procedimentos adicionais de enxertia2.
Os biomateriais são uma substância ou combinação de duas ou mais substâncias farmacologicamente inertes, de natureza sintética ou natural, que são utilizadas para melhorar, aumentar ou substituir, parcial ou integralmente, tecidos e órgãos3.
Entre os vários biomateriais, a poliuretana derivada do óleo de mamona apresenta uma fórmula molecular com aspectos favoráveis de processabilidade; flexibilidade de formulação; ausência de emissão de vapores tóxicos; bom poder de adesão; não libera radicais tóxicos quando implantada, e tem baixo custo4.
Ohara et al.5 não observaram reações tóxicas nos rins, fígado ou baço, após a implantação do polímero de mamona intraósseo e intra-articular em coelhos.
Vilarinho et al.6 verificaram que a resina da poliuretana derivada da mamona foi bem tolerada quando implantada na câmara anterior do olho de camundongo, desencadeando reações inflamatórias inicial, que diminui com o passar do tempo.
Figueiredo et al.7 realizaram um estudo comparativo entre os implantes de osso bovino desvitalizado, hidroxiapatita porosa de coral, polímero de mamona e enxerto ósseo autógeno como preenchimento de defeito ósseo no fêmur de coelhos. Os autores concluíram que o polímero de mamona mostrou propriedades de osteocondutividade e menor reação inflamatória que o osso bovino desvitalizado, com invasão de seus poros e preenchimento das cavidades císticas por tecido ósseo, mostrando-se eficaz como arcabouço para reparação tecidual guiada.
Porter8 considera o autoenxerto cartilaginoso como o material padrão para os enxertos nasais. Enumerou as seguintes razões: a baixa taxa de rejeição ou infecção e de reabsorção ou extrusão; facilidade de manipulação e obtenção, e a considerável quantidade que pode ser obtida do septo nasal ou da concha auricular.
Recentemente diferentes tipos de materiais são utilizados em rinoplastias, como os politetrafluoroetileno, sendo o mais comum o GoreTex; o silicone, tais como o Silastic; o polietileno, como o Medpore e Plastipore; e poliéster, como o Dacron, Mersilene e Supramid8-10.
De acordo com Rodrigues11, a mamona (Ricinus comunis) constitui um vegetal conhecido no Brasil e no mundo pelos sinônimos de palma Christi, carrapateira, rícino, tartago, "castor oil", "castor bean"; é originário provavelmente da Índia e constitui um vegetal típico de clima tropical. A mamona possui um grande potencial oleoquímico, sendo que o óleo de rícino, obtido das sementes, apresenta, além de seu emprego medicinal e cosmético, diversas utilidades para as necessidades humanas, em destaque a de ser biocombustível. A poliuretana é derivada do poliol poliéster, obtida a partir de ácido graxo vegetal retirado da mamona, o difenilmetanodiisocianato.
Costa, Schall12 avaliaram o emprego do polímero em próteses urológicas em 27 pacientes no período nove meses submetidos a orquiectomia bilateral por câncer da próstata. Os autores observaram que não houve infecção, reação do tipo corpo estranho, quebra da prótese ou extrusão. Concluíram que a progressão de uma cápsula fibrótica pode demorar mais de um ano para evoluir, portanto, são necessários no mínimo dois anos para se ter uma avaliação mais acurada e uma casuística maior para que o estudo estatístico das complicações seja satisfatório.
Suguimoto13 avaliou a reação do tecido ósseo na presença do implante de polímero da mamona em macacos (Cebus apella). No experimento foram utilizados oito macacos que receberam sobre o mento implantes pré-confeccionados, autoclavados e fixados com parafusos de titânio. Os autores concluíram, através da análise histológica, que o polímero da mamona foi biocompatível e não induziu à neoformação óssea nas áreas marginais e no seu interior.
Puricelli et al.14 analisaram o comportamento do polímero de mamona implantado no leito subperiosteal em ângulo da mandíbula em ratos. Os autores observaram estabilidade do implante, ausência significativa de reação inflamatória, formação de cápsula fibrosa circunjacente ao implante e neoformação óssea.
Garcia Junior15 apresentou um estudo comparativo entre os implantes de polietileno poroso (Medpor), polímero da mamona e matriz óssea bovina. O experimento foi realizado em oito macacos (Cebus apella) e teve como finalidade avaliar o processo de reparo ósseo em defeitos cirúrgicos realizados na parede anterior do seio maxilar. Após 145 dias de implantação, nas análises histológicas e histométricas foi observado que o melhor comportamento histomorfológico foi da matriz óssea bovina, seguida do polietileno poroso de alta densidade (Medpore) e do polímero da mamona (Ricinus communis), o qual respondeu com intensa fibrose e moderado infiltrado inflamatório crônico tardio.
Souza et al.16 avaliaram os resultados da utilização do polímero da mamona nas reconstruções de grandes falhas ósseas decorrentes da ressecção de tumores benignos agressivos e tumores malignos em 20 pacientes, e após seguimento mínimo de 26 e máximo de 147 semanas, obteve-se 7 (35%) de resultados excelentes, quatro (20%) bons, quatro (20%) regulares e 5 (25%) de falhas. Os autores notaram em alguns pacientes a neoformação óssea visível após três meses de pós-operatório.
O polímero da mamona foi considerado nesse estudo como uma alternativa viável, apresentando como vantagens: disponibilidade, baixo custo, ser biocompatível e osteointegrável.
Cavalieri17 realizou estudo das respostas teciduais em defeitos ósseos confeccionados nas tíbias de coelhos após implantação de polímero de mamona, cimento ósseo e resina acrílica. O autor concluiu que os três materiais foram bem tolerados pelos tecidos dos hospedeiros e relataram que o polímero da mamona permitiu o crescimento de tecido conjuntivo osteogênico no interior dos seus poros e fendas, bem como se incorporou ao tecido ósseo, promovendo a sua estabilidade no local de implantação.
Jacques18 realizou um estudo comparativo entre o enxerto ósseo autógeno e a poliuretana de mamona em coelhos submetidos a defeito padrão condilar femoral e implantação de enxerto ósseo autógeno em um dos lados e poliuretana de mamona no outro lado, de forma aleatória. Na análise macroscópica em 100% dos enxertos autógenos houve presença de cicatrização cortical, enquanto no grupo que recebeu o implante de polímero da mamona esta cicatrização estava ausente. A análise histológica mostrou a tecido ósseo maduro na zona de transição entre o implante e o osso receptor em todos os animais que receberam enxerto ósseo autógeno e em nenhum dos que receberam a poliuretana de mamona, sendo constatada presença de tecido ósseo imaturo. O autor concluiu que o implante de poliuretana da mamona integra-se no osso receptor de modo mais lento e incompleto que o enxerto ósseo autógeno.
OBJETIVOO presente trabalho teve como objetivo avaliar histologicamente a biocompatibilidade do implante do polímero derivado da mamona em macacos-pregos da espécie Cebus appella.
MATERIAL E MÉTODOEste projeto foi previamente analisado e autorizado pela Comissão de ética em experimentação animal, sob o protocolo no. 84. Para realização deste estudo foram utilizados quatro macacos adultos da espécie Cebus apella.
Os animais apresentavam um peso médio de 2kg e idade entre 7 e 8 anos; a preparação e o procedimento anestésico foram de acordo com o protocolo da Instituição.
Na anestesia os animais foram submetidos à inalação com éter dietilsulfúrico e, em seguida, foi aplicada injeção intraperitoneal de tiopental sódico, na concentração de 30 mg/Kg de peso corporal. Durante o período de pós-operatório os animais foram mantidos em condições controladas de iluminação e umidade de 60 a 80% e temperatura ambiente; receberam água e alimentação balanceada.
A avaliação radiológica foi realizada (Spectro II DabiAtlante - Ribeirão Preto) na regulagem habitual de 50 KV e 10 mA, na posição látero-lateral do perfil esquerdo da face no pré-operatório (Figura 1).
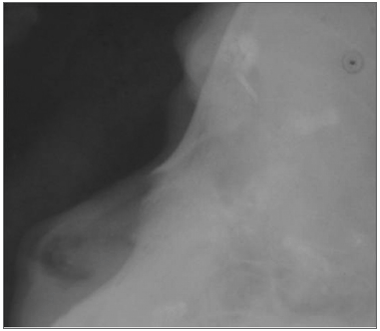
Figura 1. Radiografia lateral esquerda do nariz pré-operatório.
O procedimento cirúrgico obedeceu todos os critérios de antissepsia para a realização de defeito dos ossos nasais com luxação dos mesmos (Figura 2). O implante do polímero de mamona foi colocado sobre o defeito ósseo (Figura 3) e fixado com fio de poliglactina (polyvycril 4.0). Realizou-se o controle radiológico ao término do procedimento (Figura 4). Após o período de 270 dias os animais foram sacrificados e o material foi encaminhado para a análise morfológica, seguindo a metodologia de rotina do laboratório de histologia. As lâminas foram coradas pela Hematoxilina e Eosina (HE) para análise morfológica, em Tricrômico de Masson (TM) a fim de evidenciar a neoformação óssea ao polímero de mamona e em Picro Sirius (PS) para análise do grau de amadurecimento do colágeno por microscopia de polarização.
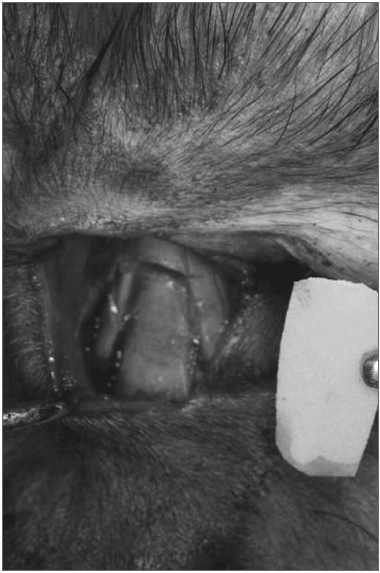
Figura 2. Aspecto do transoperatório mostrando fratura dos ossos nasais.
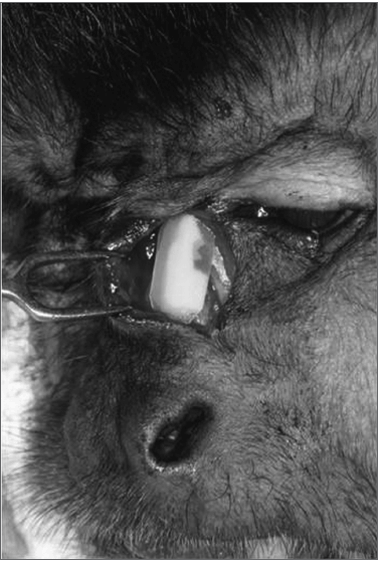
Figura 3. Aspecto do transoperatório mostrando o implante do polímero de mamona sobre o defeito ósseo.
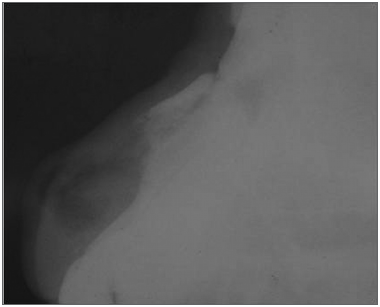
Figura 4. Radiografia lateral do nariz pós-operatório imediato.
Após o período de 270 dias, clinicamente não foi verificado degrau ou irregularidade na topografia dos ossos nasais ou retração cicatricial na ferida operatória. A cicatriz da incisão cirúrgica estava praticamente imperceptível em todos os animais estudados e os resultados radiológicos, na posição lateral da face, evidenciaram a integridade dos ossos nasais (Figura 5).
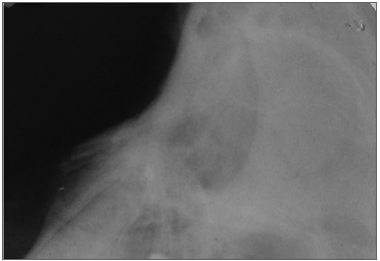
Figura 5. Radiografia lateral do nariz após 270 dias.
A análise histológica do presente estudo demonstrou que após o período de 270 dias o osso sofreu grande remodelação caracterizada pela riqueza celular com abundante número de células osteogênicas. Não foram observadas células inflamatórias ou mesmo características de reação do tipo corpo estranho. A presença de fragmentos do polímero de mamona em meio ao tecido ósseo neoformado (Figura 6) e diferentes graus de mineralização e fibras colágenas que se encontram amadurecidas demonstradas pelo alto grau de birrefringência observado na coloração próximo ao local de inserção do polímero de mamona que não foi absorvido (Figura 7).
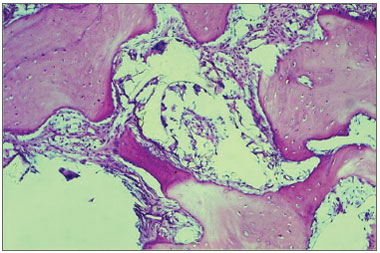
Figura 6. Fotomicrografia mostrando fragmentos da membrana do polímero de mamona no interior do tecido conjuntivo frouxo. Coloração Hematoxilina Eosina. Aumento 156 X.
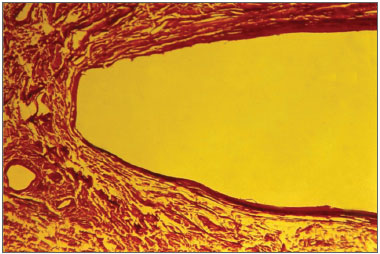
Figura 7. Local de inserção do polímero de mamona. Coloração Picro sirius. Aumento de 160 X.
Os materiais de baixo custo e abundantes na natureza seriam ideais para substituir, com vantagem, os materiais de custo mais elevado ou aqueles que necessitam de mais de uma intervenção cirúrgica, como nos casos dos enxertos autógenos. Nesse sentido, o polímero de mamona vem merecendo rigorosa investigação como material viável para enxertos.
Os estudos de Vilarinho et al.6, Suguimoto13, Souza et al.16, Cavalieri17 utilizaram o polímero de mamona nas mais diversas situações e modelos animais como camundongos, coelhos, cães e macacos em períodos de observação de 10 dias até 147 semanas, não sendo constatados nesses estudos sinais de infecção ou extrusão do material. A observação da literatura coincide com os achados clínicos desse estudo onde foi evidenciada a presença do polímero de mamona sobre o dorso nasal após 270 dias e este se encontrava fixo e recoberto por osso.
Contudo, o fato de um implante não sofrer extrusão no período observado pode não corresponder ao resultado final, uma vez que na prática clínica existem vários relatos de extrusão de implantes em períodos de dois meses até 19 anos de pós-operatório8-10.
Costa e Shall12 empregaram o polímero de mamona como próteses urológicas e não constataram sinais de infecção, reação tipo corpo estranho ou extrusão. Esses autores referem que a progressão para uma cápsula fibrótica demora no mínimo dois anos para se ter uma avaliação mais acurada.
A presença de porosidade permite o crescimento tecidual para dentro do material, fato este que dificultaria a possibilidade de movimento e que pode causar a migração e extrusão do implante8-10. Quando nos referimos à porosidade do polímero de mamona notamos relatos controversos; a maioria dos estudos refere-se à utilização do polímero associado ao carbonato de cálcio, resultando numa massa porosa quando comparada com a membrana do polímero de mamona.
Os experimentos tanto de Suguimoto13 quanto de Garcia Junior15 utilizaram o mesmo modelo animal do nosso estudo, mas aplicando o polímero associado ao carbonato de cálcio. Em nosso estudo utilizamos a membrana do polímero de mamona. Nestes experimentos não foi observada aos cortes histológicos a invasão de tecido osteogênico dentro dos poros do implante. Os resultados foram discordantes dos achados de Cavalieri17; concluíram que a presença de porosidade na arquitetura interna do implante permite a incorporação do material aos tecidos vivos e favorece a regeneração dos defeitos ósseos.
Considerando os achados da literatura pesquisada, notamos resultados conflitantes, o que reflete basicamente o perfil metodológico diferenciado em cada estudo, em virtude das múltiplas variáveis, como o modelo animal, e no mesmo tipo de animal a região estudada, o período de avaliação, o tipo de polímero de mamona utilizado e a finalidade da pesquisa. Contudo, na maioria dos relatos observamos que não foram demonstrados relatos de infecção ou extrusão do implante. Os casos que envolviam defeito ósseo ocorreu neoformação óssea com osso imaturo com tendência à organização e osso maturo na superfície do polímero, além da formação de fibras colágenas na superfície do implante de polímero da mamona. Não podemos afirmar que o polímero da mamona induziu à osteogênese; esta deveu-se provavelmente ao estímulo do próprio trauma cirúrgico no broto ósseo remanescente e periósteo do osso nasal.
CONCLUSÃODe acordo com a metodologia empregada e considerando os resultados obtidos podemos concluir que: o polímero de mamona foi biocompatível, houve persistência do biomaterial após 270 dias do procedimento cirúrgico e o implante de não induziu à neoformação óssea.
REFERÊNCIAS BIBLIOGRÁFICAS1. Citardi MJ, Friedman CD. Nonvascularized autogenous bone grafts for craniofacial skeletal augmentation and replacement. Otolaryngol Clin North Am. 1994;27:891910.
2. Cook AD, Hrkach JS, Gao NN, Johnson IM, Pajvani UB, Cannizaro Sm, Langer R. Characterization and development of RGDpeptidemodified poly(lactic acidcolysinc) as an interactive resorbable biomaterial. J Biomed Mater Res. 1997;35:51323.
3. Ignácio H, Mazzer N, Barbieri Chierice GO. Uso da poliuretana derivada do óleo de mamona para preencher defeitos ósseos diafisários segmentares do rádio. Estudo experimental em coelhos. Rev Bras Ortop. 1997; 32(10):81521.
4. Ohara GH, Kojima KE, Rossi JC, Salomão C. Estudo experimental da biocompatibilidade do polímero poliuretano da mamona implantada intraóssea e intra-articular em coelhos. Acta Ortop Bras. 1995;3(2):6268.
5. Vilarinho RH, Hetem S, Ramalho LTO. Implante de resina de poliuretana vegetal na câmara anterior do olho de camundongo. Odonto 2000 Odontologia do Século XXI, Araraquara. 1996;1(0):2529.
6. Figueiredo ASD, Fagundes DJ, Novo NF, Inouye CM, Takita LC, Sassioto MCP. Osteointegração de osso bovino desvitalizado, hidroxiapatita de coral, poliuretana de mamona e enxerto ósseo autógeno em coelhos. Acta Cir Bras. 2004;19(4):37082.
7. Porter JP. Grafts in rhinoplasty: alloplastic vs autogenous. Archives of Otolaryngology Head & Neck Surgery. 2000;126(4):55861.
8. Vuyk HD, Adamson, PA. Biomaterials in rhinoplasty. Clin Otolaryngol. 1998;23(3):20917.
9. Fanous N, Samatha M, Yoskovitch A. Dacron implants in rhinoplasty: a review of 136 cases of tip and dorsum implants. Arch Facial Plast Surg. 2002;4(3):14956.
10. Rodrigues RFO. As folhas de Palma ChristiRicinus communis L. Euphoorbiaceae Jussieu. Revista Lecta. 2002;20(2):183194.
11. Costa RP, Schall CH. Resultados preliminares da aplicação do polímero poliuretana vegetal em próteses e órteses. Hospital Amaral de Carvalho. 1993;3543.
12. Suguimoto RM. Implante de polímero de mamona (Ricinus communis) sobre o mento.Estudo histológico em macacos. Tese (Mestrado). Araçatuba: Universidade Estadual Paulista; 1997.
13. Puricelli E, Baraldi CE, Ponzoni D, Peschke. Estudo histológico do polímero poliuretano da mamona implantado no ângulo mandibular de ratos. Rev Fac Odontol Porto Alegre. 1999; 40(1):3841.
14. Garcia Junior IR. Utilização dos implantes de Polietileno Medpor, Poliuretana de Mamona e Matriz Óssea bovina em defeitos ósseos maxilares. Análise histológica e histométrica em macacos. Tese (Doutorado). Araçatuba: Universidade Estadual Paulista; 2000.
15. Souza AM, Brandt CT, Lima JA. Biopolímero da mamona na reconstrução de falhas ósseas após ressecção de tumores no esqueleto apendicular. An Fac Med Univ Fed Pernambuco. 2002;47(2):11623. Odontol Bras. 2003;6(3):1925.
16. Cavalieri, I. Estudo do processo de reparação óssea entre os implantes de polímero de mamona, resina acrílica termicamente ativada e cimento ósseo, em tíbia de coelhos. Tese (Mestrado). São José dos Campos: Universidade Estadual Paulista; 2000.
17. Jacques JW. Estudo comparativo entre enxerto ósseo autógeno e poliuretana de mamona, em coelhos. Tese (Mestrado). São Paulo: Escola Paulista de Medicina; 2001.
1 Mestre em Otorrinolaringologia e Cirurgia de Cabeça e Pescoço pela Universidade Federal de São Paulo - Felow em Cirurgia Craniomaxilofacial pelo Hospital de Clinicas de Porto Alegre - Universidade Federal do Rio Grande do Sul Pós-Graduando (Doutorado) pela Faculdade de Ciências Médicas da Santa Casa de São Paulo
2 Professor Doutor da Disciplina de Otorrinolaringologia da Faculdade de Ciências Médicas da Santa Casa de São Paulo
3 Doutora - Professora Doutora do Departamento de Morfologia da Faculdade de Odontologia de Araraquara - UNESP
4 Professor Doutor responsável pelo Núcleo de Procriação de Macacos -Prego do Departamento de Ciências Básicas da Faculdade de Odontologia do Campus de Araçatuba - UNESP
5 Mestre em Odontologia pela Faculdade de Odontologia de Araraquara - UNESP - Pós- Graduando (Doutorado) pela Faculdade de Odontologia de Araraquara - UNESP
Endereço para correspondência: Rua Marechal Floriano Peixoto 1520, ap 1703 - Duque de Caxias - Cuiabá /MT.
E-mail: pcjdias@ig.com.br Telefone: (0xx65) 3051 35 86
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da BJORL em 15 de novembro de 2006. cod 3517
Artigo aceito em 16 de abril de 2009.


