INTRODUÇÃOA surdez profunda é uma deficiência que incapacita o indivíduo de se comunicar adequadamente com o meio e também de se desenvolver intelectualmente. Dessa maneira, a surdez tem um impacto importante no estilo de vida e no desenvolvimento da personalidade do indivíduo portador de deficiência auditiva1; apresenta etiologias congênitas e adquiridas e sua prevalência mundial, no ano de 1995, segundo estimativas da World Health Assembly (WHA) é de 2,2%, acometendo 120 milhões de pessoas. No Brasil, é muito difícil estimar a incidência da surdez, uma vez que esta não é uma doença de notificação compulsória aos órgãos públicos.2
A prótese auditiva convencional é um aparelho de amplificação sonora que amplifica o volume dos sons do ambiente. Esse aparelho é usado no tratamento de diversos tipos de perdas auditivas, porém, dependendo do grau da disfunção auditiva, ele possui resultados limitados. Quando um paciente não alcança uma discriminação maior que 40% em testes de reconhecimento de sentenças em apresentação aberta com a melhor prótese possível, uma segunda alternativa de tratamento é o implante coclear.3
O implante coclear é um estimulador elétrico formado por uma unidade externa de processamento de fala e por uma unidade interna de suporte e programação, constituída por uma antena de recepção e eletrodos de estimulação.4 O implante possibilita não apenas a sensação de audição, mas também o reconhecimento dos sons da fala. Ele faz o papel de todo o ouvido, uma vez que capta o som, decodifica as mensagens e as envia por eletrodos para o cérebro, substituindo o órgão de Corti e estimulando diretamente as fibras nervosas e as células ganglionares do nervo auditivo.5
A cirurgia convencional para a colocação do implante coclear é realizada através da via transmastóidea, com timpanotomia posterior e a seguir cocleostomia (abertura do bloco labiríntico com broca perfurante).6
A partir da década de 90 os implantes cocleares multicanais se consolidaram como tratamento cirúrgico para as deficiências auditivas neurossensoriais.5 Dentre as causas de surdez neurossensorial, a meningite é a principal causa adquirida7. Sendo uma doença endêmica no Brasil, a incidência em nosso meio é maior do que na América do Norte e Europa, chegando a 8% de todas as etiologia de surdez profunda.8 A deficiência auditiva pós-meningite se caracteriza por ser neurossensorial, severa ou profunda bilateral.9 A meningite pneumocóccica tem o pior prognóstico auditivo e chega a causar até 30% de perdas auditivas permanentes em sobreviventes.10 Em 80% desses pacientes, a perda auditiva está relacionada a uma ossificação da cóclea.11 Além da ossificação coclear, a degeneração do nervo cócleo-vestibular também é descrita em alguns casos.
A ossificação da cóclea é uma seqüela que pode ser causada por trauma de osso temporal, otosclerose e otites médias crônicas, porém, a principal causa é a meningite.12 O processo de ossificação decorrente dessas patologias geralmente inicia-se próximo à janela redonda e ascende para o ápice. Portanto, a rampa timpânica do giro basal, em geral, é a parte mais afetada.6
Sabe-se que uma obliteração total ou parcial da porção inicial do giro basal da cóclea impede a completa inserção de eletrodos usados nos implantes cocleares convencionais.13 Esse fato é um grande problema, uma vez que estudos baseados em dados de 327 pacientes comprovaram que quanto maior a inserção e conseqüentemente maior o número de eletrodos ligados, melhor o índice de reconhecimento da fala.14 Dessa maneira, várias técnicas foram utilizadas e testadas para que um número cada vez maior de eletrodos pudesse ser implantado profundamente nas cócleas ossificadas. Porém, nenhuma dessas técnicas permitiu a inserção total dos eletrodos ou preservou a anatomia da cóclea.15-17
Em 1993, Cohen e Waltzman propuseram a remoção do osso recém-formado do início do giro basal da cóclea.15 Gantz and et al. sugeriram a completa remoção do giro basal.16 Em 1997, Balkany modificou a técnica descrita por Gantz e preservou a porção inicial do giro basal da cóclea.17 No entanto, nesses casos foram descritos como problemas pós-operatórios, a estimulação do nervo auditivo causando dor e desconforto e a inserção incompleta dos eletrodos intracocleares.
Lenarz et al., em 1997, propuseram a inserção de duas fileiras de eletrodos paralelas entre si, em canais criados separadamente nos giros basal e médio da cóclea, desenvolvendo, assim, o implante coclear com 2 feixes de eletrodos.18 Uma grande vantagem desse implante é que o giro médio está desobstruído em aproximadamente 50% dos casos que são descritos como total obliteração da cóclea. Além disso, essa técnica diminui o risco de lesão do nervo facial. O implante coclear com 2 feixes de eletrodos foi especialmente criado para cócleas totalmente obliteradas ou inacessíveis cirurgicamente.
No implante coclear com 2 feixes de eletrodos também é realizada mastoidectomia e timpanotomia posterior. A seguir, é realizada cocleostomia ântero-superior à janela redonda, no giro basal da cóclea, dando acesso à escala timpânica. Outra cocleostomia é realizada no segundo giro da cóclea. A segunda cocleostomia é feita caudalmente ao processo cocleariforme e a 2mm anteriormente da janela oval.
Em pacientes com obliteração total da escala timpânica após ter sido realizada a primeira cocleostomia, a escala vestibular deverá ser exposta. Se esta também estiver ossificada, o giro basal é brocado da cocleostomia até a parede anterior da cóclea. Via de regra, o tecido ósseo recém-formado tem cor branca que pode ser distinguida do osso da cóclea que é mais amarelado e mais firme. O broqueamento deve ser parado assim que o osso da parede anterior da cóclea for alcançado para evitar lesão da artéria carótida interna, a qual está intimamente relacionada com a porção anterior da cóclea. No entanto, para um procedimento de tão alto risco, essa descrição é muito imprecisa. Lenarz et al.13 estimou que a distância da primeira cocleostomia até a parede anterior da cóclea no giro basal é de 8 a 11mm. Já a distância da segunda cocleostomia, novamente até a parede anterior do segundo giro da cóclea é de 5 a 6mm. Porém, em 2002, o mesmo autor relata que em um estudo com pacientes implantados com o implante coclear com 2 feixes de eletrodos, a inserção mais profunda de eletrodos no giro basal foi de 10,3mm e no segundo giro coclear, essa distância era de 8,2mm.19
Em 10 cirurgias realizadas em 2005, foi encontrada dificuldade na realização da cocleostomia com broca convencional nestas cócleas ossificadas. Em 3 casos houve rompimento da broca quando esta penetrou parcialmente.
Devido à importante relação existente entre a artéria carótida e a cóclea e suas variações anatômicas, bem como a gravidade de uma eventual lesão desse vaso, surgiu a idéia de medir a distância da cocleostomia a essa artéria em ossos de cadáver para se determinar a profundidade máxima que o cirurgião pode chegar.
Os objetivos deste estudo são:
1. Medir a distância da cocleostomia até a artéria carótida interna no giro basal e no giro médio de cócleas de ossos temporais de cadáver.
2. Confeccionar, a partir dessas medidas, um instrumento graduado que possa ser utilizado não só para orientar o cirurgião da profundidade atingida, mas também como uma broca manual.
MATERIAIS E MÉTODOSForam obtidos 21 ossos temporais de cadáveres adultos no Serviço de Verificação de Óbitos da Capital (SVOC). Todos os ossos foram formalizados (formol a 70%) e dissecados utilizando-se motor de alta rotação ( 40.000 rpm) da marca Volvere (Japão). Nesses ossos foi realizada mastoidectomia com retirada de toda a cortical da mastóide e da parede posterior do meato acústico externo de modo a expor o promontório da cóclea na cavidade timpânica e as duas janelas (oval e redonda) e o processo cocleariforme. O martelo e a bigorna foram retirados permanecendo na posição somente o estribo.
Antes da realização das cocleostomias, continuamos o broqueamento, para dissecar e identificar a parte da artéria carótida interna que está intimamente relacionada com a cóclea.
Após a identificação de todas as estruturas citadas, realiza-se a primeira cocleostomia antero-superiormente à janela redonda no giro basal da cóclea. A segunda cocleostomia é feita caudalmente ao processo cocleariforme e a 2mm anteriormente à janela oval, no giro médio da cóclea. Feitas as cocleostomias, brocamos uma comunicação (túnel) entre elas e a artéria carótida interna. A broca utilizada foi de espessura igual a do medidor graduado, para que ele se encaixasse de maneira precisa para realização das medidas. A parte superior da cóclea foi retirada para que pudéssemos visualizar de forma íntegra o medidor atravessando os giros cocleares a partir da cocleostomia e chegando até a artéria carótida interna (Figura 1). Esse procedimento não prejudica em nada os valores das medidas. A medição foi realizada da borda inferior do início da cocleostomia até a maior projeção posterior da artéria carótida interna (Figura 2).
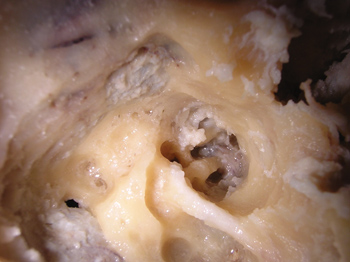
Figura 1. Túnel superior e túnel inferior que comunicam as cocleostomias e a artéria carótida interna.
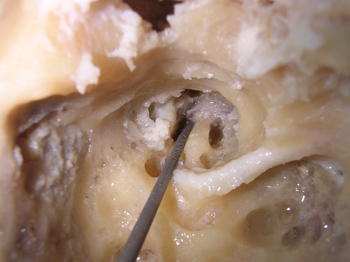
Figura 2. Realização das medidas utilizando o instrumento graduado em milímetros.
As variáveis numéricas foram discutidas por meio de sua média ± desvio-padrão, intervalo de confiança de 95% (IC 95%) e valores mínimos e máximos. Por se tratar de um estudo descritivo e de exploração inicial, não foi calculada a amostra, sendo utilizada uma amostra de conveniência segundo a disponibilidade de peças no período do estudo.
Foi confeccionado um estilete reto com ponta em forma de lança sextavada de aço inox fosco graduado de 1,0 em 1,0mm sob encomenda à empresa Azelindo Mercansoli EPP de Jundiaí- SP. Os estiletes medem em seu comprimento total 16cm. Com diâmetro inicial em sua ponta de 1.0mm, indo engrossando até atingir 1,3 mm junto ao cabo.
O número da comissão de ética é 371/2005.
RESULTADOSDISCUSSÃOO implante coclear (IC) é reconhecido como um método efetivo para o tratamento de surdez profunda sensorial bilateral4,17,20. Os casos de cócleas ossificadas continuam sendo um grande desafio aos cirurgiões, uma vez que não é possível a utilização de todos os eletrodos dos modernos aparelhos de implante coclear, fazendo que com isso os resultados sejam muito piores do que os obtidos em cócleas sem ossificação. Outros fatores podem também ser responsáveis por estes maus resultados, tais como alterações nas sinapses do ramo coclear do nervo cócleo-vestibular que diminuem a condutibilidade do impulso nervoso gerado pelo IC. As técnicas operatórias do IC foram desenvolvidas após intenso estudo anatômico do osso temporal. Um profundo conhecimento da anatomia do ouvido interno, especialmente da cóclea é essencial para o sucesso dessa cirurgia6,21. Sabe-se que a artéria carótida é extremamente próxima da cóclea na junção de seus segmentos vertical e horizontal.22 No entanto, livros e atlas sobre a anatomia dessa região não apresentam informações completas e detalhadas da relação das pequenas estruturas que compõem o ouvido interno, como a cóclea e a artéria carótida interna, que são extremamente importantes para a cirurgia do IC de 2 feixes de eletrodos.
Apesar de existirem alguns estudos22,23 que visam estudar as distâncias e a relação entre essas duas estruturas, as medidas obtidas são da parede externa dos giros cocleares até a artéria, medida que por si só não acrescenta informações muitos relevantes para serem consideradas durante uma cirurgia de IC de 2 feixes de eletrodos. Nessa cirurgia, é importante saber a distância segura que pode ser realizado um broqueamento a partir da cocleostomia em direção à parede anterior da cóclea para que não ocorra lesão da ACI. Esse broqueamento é feito para que um maior número de eletrodos possa ser implantado, uma vez que nesses casos as cócleas estão parcial ou totalmente ossificadas.21
Em nosso estudo resolvemos simular parte do que é feito durante a cirurgia do IC de 2 feixes de eletrodos, realizando nos ossos temporais as cocleostomias nos giros cocleares. A partir dessas cocleostomias continuamos o broqueamento através da cóclea, porém diferente do que se espera durante a cirurgia, brocamos além da parede anterior da cóclea e chegamos até a ACI. Dessa maneira, conseguimos medir a máxima distância que o broqueamento pode ser feito sem lesar a artéria.
Portanto, as medidas encontradas em nosso estudo não podem ser comparadas com as de estudos anteriores20,22,23, uma vez que além de serem medidas diferentes, a angulação em que essas medidas foram realizadas também é diferente. Enquanto em nosso estudo nos baseamos na técnica utilizada durante a cirurgia, mantendo essa angulação, nesses outros estudos as medidas são obtidas utilizando a angulação que irá promover as mínimas distâncias entre essas estruturas.
É importante ressaltar que essas peças foram obtidas no SVOC sem informações sobre sexo e raça das peças. A idade exata no momento da morte também é desconhecida, porém sabe-se que todos os ossos temporais pertencem a cadáveres adultos. No entanto, a importância desses dados é discutível uma vez que estruturas chaves como cóclea, orelha média, ossículos e membrana timpânica já estão com sua configuração pronta na época do nascimento6. Dessa maneira, a técnica cirúrgica usada para a realização do IC em crianças é muito semelhante à técnica feita em adultos5. Porém, apesar da literatura afirmar que as estruturas do ouvido interno já estejam plenamente desenvolvidas no nascimento, respeitando as dimensões na idade adulta24,25,26 em um estudo que a analisa as diferenças entre as distâncias dos giros cocleares e do canal carótico em 2 grupos divididos pela idade (grupo I- até 4 anos e grupo II - maior que 4 anos), o autor afirma que em no grupo I essas distâncias foram significantemente menores.22 No entanto, a amostra no grupo I era de apenas 12 ossos temporais, o que poderia tornar estatisticamente duvidoso esse resultado. Portanto, outros estudos deveriam ser realizados para assegurar se as distâncias obtidas em nosso estudo poderiam também ser aplicadas para IC de 2 feixes de eletrodos feitos em crianças.
Quanto ao sexo e lateralidade, Penido23 afirma não ter encontrado associação significativa entre essas variáveis e a anatomia das estruturas do ouvido interno. Não encontramos na literatura referências sobre a influência da raça nessas estruturas.
CONCLUSÕESApesar dos parâmetros calculados, concluímos que a melhor medida para ser considerada na confecção do instrumento cirúrgico serão as mínimas medidas obtidas em cada um dos giros cocleares. A lesão da ACI durante uma cirurgia é considerada quase fatal, uma vez que pode originar sangramento de difícil controle e trazer graves conseqüências ao Sistema Nervoso Central. Portanto, trabalhar com as mínimas medidas é a maneira mais segura para evitar esses problemas.
Além de o instrumento orientar o cirurgião da maior profundidade que ele pode obter na cocleostomia sem lesar a ACI, pretendemos utilizá-lo como uma broca manual que atuará sem alta rotação, não aquecendo, portanto, com um menor risco de quebra durante a cirurgia como aconteceram com algumas brocas convencionais.
REFERÊNCIAS BIBLIOGRÁFICAS1. Zenari CP, Moretto MLT, Nasralla HR, Gavião ACD, de Lucia MCS, Bento RF et al. Aspectos Psicológicos de indivíduos portadores de surdez profunda bilateral candidatos ao implante coclear. Arq Otorrinolaringol 2004;8(2):142-8.
2. Mencher GT. Challenge of epidemiological research in the developing world: overview. Audiology 2000;39(4):178-83.
3. Bento RF, Brito Neto RV, Castilho AM, Goffi Gomez MVS, SantAnna SBG, Guedes MC. Resultados auditivos com implante coclear multicanal em pacientes submetidos à cirurgia no Hospital das Clínicas da FMUSP. Rev Bras Otorrinolaringol 2004;70(5):632-4.
4. Bento RF, Minit A, Marone SAM. Doenças do ouvido interno. Em: Bento RF, Minit A, Marone SAM. Tratado de Otologia. 1ª ed., São Paulo; 1998. p.315-22.
5. Filho OAC, Bevilacqua MC, Amantini RCB, Neto DL. Implante Coclear em adultos. Em: Sociedade Brasileira de Otorrinolaringologia (SBORL). Tratado de Otorrinolaringologia. Vol 2. 1ª ed. São Paulo: Roca; 2002.p. 270-5.
6. Bento RF, Brito Neto RV, Sanchez TG, Castilho AM. Técnica cirúrgica para implante coclear. Arq Otorrinolaringol 2002;6(2):131-8.
7. Brookhouser PE, Auslander MC. Aided auditory thresholds in children with postmeningitic deafness. Laryngoscope 1989;99:800-8.
8. Bento RF, Silveira JAM, Martucci JR O, Moreira E. Etiologia da deficiência auditiva. Estudo eletrofisiológico de 136 casos. A Folha Med 1986;93(5-6):359-66.
9. Santos TM. Disacusia pós-meningítica: estudo retrospectivo. Dist Com 1990;3:197-203.
10. Porto Cantanhede PR. Avaliação de resultados de implante coclear em pacientes deficientes auditivos secundários à meningite [Dissertação]. Universidade de Campinas; 2001.
11. Steenerson RL, Gray LB, Wynens MS. Scala vestibuli cochlear implantation for labyrinthine ossification. Am J Otol 1990;11:360-3.
12. Raut V, Toner JG. Cochlear implantation in the obliterated cochlear. Clin Otolaryngol 2002;27(3):147-52.
13. Lenarz T, Lesinski-Schiedat A, Weber BP, Issing PR, Frohne C, Buchner A, et al.. The nucleus double array cochlear implant: a new concept for the obliterated cochlea. Otol Neurotol 2001 Jan;22(1):24-32.
14. Rizzi FML, Bevilacqua MC. Efeitos do número e localização de eletrodos na cóclea na percepção da fala de indivíduos pós-linguais implantados. Rev Bras Otorrinolaringol 2003;69(3):364-9.
15. Cohen NL, Waltzman S. Partial insertion on the nucleus multichannel cochlear implant: technique and results. Am J Otol 1993;14:357-61.
16. Gantz BJ, McCabe BF, Tyler RS. Use of multi-channel cochlear implants in obstructed and obliterated cochleas. Otolaryngol Head Neck Surg 1988;98:72-81.
17. Balkany T, Luntz M, Telische F, Hodges AH. Intact canal wall drill out procedure for implantation of the totally ossified cochlea. Am J Otol 1997;18(suppl):58-9.
18. Lenarz T, Battmer RD, Lesisnki A, Parker J. Nucleus double electrode array: a new approach for ossified cochlea. Am J Otol 1997;18(suppl):42-3.
19. Lenarz T, Buchner A, Tasche C, Cristofoli T, Lesinsky-Schiedat A, Wallenberg EV et al. The results in patients implanted with nucleus double array cochlear implant: pitch dicrimination and auditory performance. Ear Hear 2002;23(1 Suppl):90S-101S.
20. Millar DA, Hillman TA, Shelton C. Implantation of the ossified cochlea: management with the split electrode array. Laryngoscope 2005;115(12):2155-60.
21. Wysocki J, Skarzynski H. Distances between the cochlea and adjacent structures related to cochlear implant surgery. Surg Radiol Anat 1998;20(4):267-71.
22. Gastman BR, Hirsch BE, Sando I, Fukui MB, Wargo ML. The potential risk of carotid injury in cochlear implant surgery. Laryngoscope 2002;112(2):262-6.
23. Penido Nde O, Borin A, Fukuda Y, Lion CN. Microscopic anatomy of the carotid canal and its relations with cochlea and middle ear. Rev Bras Otorrinolaringol (Engl Ed) 2005;71(4):410-4.
24. Muren C, Wadin K, Wilbrand HF. The cochlea and the carotid canal. Acta Radiol 1990;31:33-5.
25. Schuknecht HF, Gulya AJ. Anatomy of the temporal bone with surgical implications. Philadelphia: Lea; 1986. p. 350.
26. Shambaugh Jr GE. Surgery of the ear. 2nd ed. Philadelphia: WB Saunders; 1967.p.722.
1 Estudante.
2 Professor Titular da Disciplina de Otorrinolaringologia da Faculdade de Medicina da Universidade de São Paulo, Chefe do Departamento de Oftalmologia e Otorrinolaringologia da FMUSP.
3 Pós-Graduando do Programa de Otorrinolaringologia - Doutorado da Faculdade de Medicina da USP, Médico Assistente da Hospital das Clínicas da Faculdade de Medicina da USP.
Faculdade de Medicina da Universidade de São Paulo.
Endereço para correspondência: Mariana Bogar - Rua da Figueiras 720 ap.141 Bairro Jardim Santo André SP 09080-300.
FAPESP.
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da RBORL em 6 de janeiro de 2007. Cod. 3583.
Artigo aceito em 23 de abril de 2007.


