INTRODUÇÃOO câncer está certamente entre as maiores causas de morte em todos os países do mundo. Há muitos anos, pesquisas buscam tratamentos eficazes para esta patologia. O único consenso é que todas as formas de tratamento funcionam melhor, ou mesmo só funcionam, quando a neoplasia é diagnosticada precocemente. A partir dessa afirmativa, há hoje em dia uma busca incessante por métodos de diagnósticos mais precisos, possibilitando, assim, a condução de um tratamento mais adequado.
Estudos imuno-histoquímicos de componentes da membrana basal vêm se mostrando eficientes no diagnóstico e prognóstico do câncer, pois esta estrutura, além de funcionar como uma importante barreira estrutural1, atua como limite para a invasão neoplásica nos carcinomas epidermóides, impedindo a disseminação das células tumorais2.
A laminina é uma glicoproteína presente na membrana basal, com funções específicas, e dentre elas, destaca-se a adesividade. As células tumorais ligam-se à membrana basal, através de receptores para laminina e, posteriormente, são estimuladas a produzir metaloproteinases, iniciando, assim, a fragmentação e degradação da membrana. Essas características reforçam os estudos imuno-histoquímicos sobre os componentes da membrana basal, relacionados com a invasão tumoral.
Recentemente, Garcia et al. (2006)3 investigaram a expressão imuno-histoquímica do colágeno IV e da laminina em amostras de epitélio normal, displasias leve e moderada, carcinomas "in situ", carcinomas invasivos e nódulos metastásicos. Eles observaram uma perda progressiva da continuidade da expressão imuno-histoquímica destas proteínas seguindo a evolução desde a displasia até o nódulo metastásico, e correlacionaram a fraca expressão dos marcadores como significante na evolução destas lesões orais. Esta relação é considerada importante, pois carcinomas mais agressivos possuem uma maior capacidade de produzir enzimas que degradam componentes da membrana basal, impedindo desta forma nova síntese protéica.
O presente trabalho tem como objetivo investigar a expressão imuno-histoquímica da laminina na membrana basal de carcinoma escamocelular de boca, e correlacionar esta expressão às características histológicas de malignidade.
MATERIAIS E MÉTODOSEste estudo obteve aprovação do Comitê de Ética da Faculdade de Odontologia da Universidade Federal da Bahia com protocolo de nº 011/05.
Trinta e uma biópsias de carcinomas escamocelulares primários de boca foram analisadas histologicamente. Nenhum dos indivíduos foi submetido à quimioterapia ou radioterapia previamente. Vinte e três pacientes (74,2%) eram do sexo masculino e 8(27,8%) do sexo feminino. A idade variou de 29 a 81 anos, com uma média de 60 anos. A localização mais freqüente dos tumores foi a língua, seguida do assoalho de boca. Observou-se um predomínio de indivíduos da raça branca (15 casos; 48,4%), seguido por pardos (9 casos; 29%) e negros (7 casos; 22,6%).
O material de biópsia foi fixado em formol a 10% e emblocado em parafina, sendo preparados cortes de 5mm de espessura para análise morfológica. As lâminas referentes a cada caso foram coradas pela hematoxilina e eosina (H&E) e submetidas a exame histológico sob microscopia de luz, com finalidade de descrever os aspectos morfológicos das lesões. A graduação histológica foi realizada através da microscopia de luz (aumento de 400X), utilizando-se o sistema de graduação de tumores malignos proposto por Anneroth, Batsakis & Luna (1987)4 (Tabela 1). Este sistema consiste da avaliação de seis características morfológicas que caracterizam a população de células tumorais e a relação tumor-hospedeiro, que são: grau de queratinização, pleomorfismo nuclear, número de mitoses, padrão de invasão, estágio de invasão e infiltração linfoplasmocitária. O parâmetro "estágio de invasão" foi omitido por tratar-se de biópsias incisionais de carcinomas escamocelulares de boca. Cada parâmetro morfológico foi graduado de 1 a 4 pontos. O escore final para cada caso foi definido pela média aritmética da soma total dos pontos atribuídos a cada parâmetro avaliado. Os valores entre 1,0 e 2,5 foram considerados baixos graus de malignidade, enquanto os valores entre 2,6 e 4,0 altos graus de malignidade.
A imunomarcação da glicoproteína laminina foi realizada através do método da streptavidina-biotina. Para a técnica imuno-histoquímica, foram realizados cortes de 3mm de espessura a partir do material emblocado em parafina. Os cortes foram desparafinados e imersos em solução TRIS pH 7.4. O anticorpo monoclonal anti-laminina foi utilizado como anticorpo primário (LAM-89, SIGMA) 1:75. As etapas seguintes foram realizadas com o auxílio de um sistema automatizado de marcação imuno-histoquímica (autostainer universal staining system Dako), onde se procedeu a incubação do anticorpo primário, do anticorpo secundário e do complexo terciário streptavidina-biotina, respectivamente. Entre as reações, os cortes foram vigorosamente lavados em solução de TRIS pH 7.6 e Twiin 0,5%. Ainda na máquina, a revelação da reação foi realizada com diaminobenzidina (DAB Plus) e contra-corados com Hematoxilina de Mayer. Como controle positivo foram utilizados cortes de mucosa oral sadia e, como controle negativo o mesmo tecido, sendo suprimido da reação o anticorpo primário.
A análise histológica da expressão imuno-histoquímica da laminina nas secções de todos os casos de carcinomas escamocelulares de boca foi realizada sem o conhecimento prévio da graduação histológica de malignidade a que as lesões pertenciam. Foi adotado método semi-quantitativo para graduação da intensidade bem como da integridade da expressão da laminina na membrana basal de acordo com a metodologia utilizada por Shinohara et al. (1996)2 e Kannan et al. (1994)5. A intensidade de marcação foi graduada como ausente (-), discreta (+), moderada (++), e intensa (+++). A integridade da laminina na membrana basal foi graduada de acordo com os seguintes critérios: contínua (+++), quando a marcação para laminina se mostrou linear, sem interrupções, compatível ao epitélio normal; moderadamente contínua (++); quando a imunorreatividade se apresentou superior ou igual a 50% da membrana basal, discretamente contínua (+), quando menos de 50% da membrana basal mostrou-se positiva para o anticorpo e ausente ou quase ausente (±). Foi evitada a observação de áreas com intenso infiltrado inflamatório para que não houvesse distorção dos resultados.
Foi feita uma análise descritiva com a finalidade de identificar as características gerais e específicas da amostra estudada. Para verificar a existência de associações significativas entre a intensidade e continuidade de expressão imuno-histoquímica da laminina em relação aos grupos de alta e baixa malignidade utilizou-se o teste não-paramétrico de Mann-Whitney. A existência de relação linear entre a intensidade e continuidade de expressão da laminina e o grau de malignidade foi observada utilizando-se o teste de correlação de Spearman. Foram consideradas como estatisticamente significantes associações com p-valor < 0,05.
RESULTADOSDo ponto de vista morfológico, no total de 31 casos, 19 casos (61,2%) exibiram baixo grau de malignidade (escore entre 1,0 e 2,5 pontos), enquanto 12 casos (38,7%) apresentaram escores iguais ou acima de 2,6, sendo portanto classificadas como tumores de alto grau de malignidade.
Com relação à intensidade de marcação para laminina nas lesões com baixo grau de malignidade, sete casos (36,8%) demonstraram intensa marcação (+++) desta glicoproteína circundando as bordas dos ninhos de células neoplásicas (Figuras 1 e 2). Expressão moderada (++) foi evidenciada em cinco casos (26,3%) e uma discreta expressão (+) da laminina foi encontrada em sete casos (36,8%), (Figuras 3 e 4). Quanto à integridade da laminina na membrana basal, o padrão de continuidade estava relacionado com a intensidade de expressão da laminina. O padrão contínuo (+++) foi observado em 10 casos (52,6%), 5 casos (26,3%) apresentaram continuidade moderada (++), enquanto que o padrão discreto de continuidade (+) foi exibido em 3 casos (15,7%). Neste grupo de lesões com baixo grau de malignidade, a quase ausência de continuidade (+/-) da membrana basal, foi encontrada em apenas uma única lesão (5,2%).
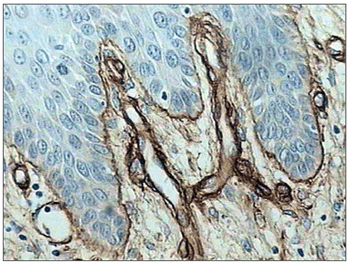
Figura 1. Expressão imuno-histoquímica da laminina em carcinoma escamocelular de boca, evidenciando marcação contínua, linear e sem interrupções. (Streptavidina biotina, 100X)
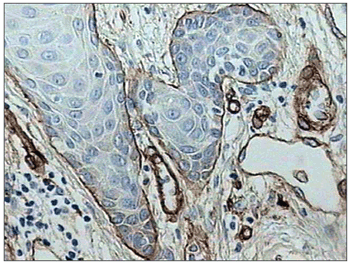
Figura 2. Intensa expressão imuno-histoquímica da laminina em membrana basal de carcinoma escamocelular de boca. Observar áreas com perda de continuidade. (Streptavidina biotina, 100X)
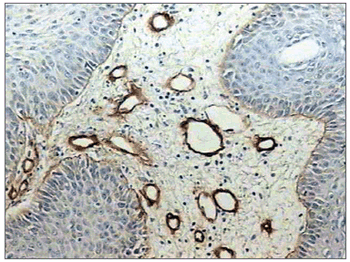
Figura 3. Moderada expressão imuno-histoquímica da laminina em membrana basal de carcinoma escamocelular de boca. (Streptavidina biotina, 100X)
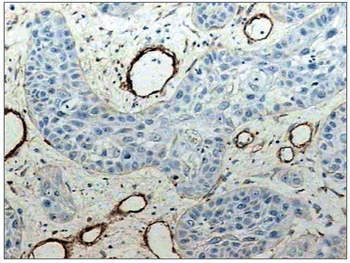
Figura 4. Discreta expressão imuno-histoquímica da laminina. Observar intensa marcação dos vasos sanguíneos no estroma tumoral. (Streptavidina biotina, 100X)
Nos carcinomas escamocelulares com alto grau de malignidade, considerando-se a intensidade de marcação, observou-se um predomínio de casos com discreta expressão (+) para a laminina (66,6%), moderada expressão (++) em 2 casos (16,6%) e nos outros 2 casos (16,6%), cujas lesões mostravam graus de malignidade mais elevados, foi notada ausência de expressão (-) da laminina (Figura 5). Não foi observado nenhum caso com intensa marcação (+++) para esta glicoproteína. Em relação à continuidade da marcação da laminina na membrana basal neste grupo, verificou-se que metade das lesões (6 casos) evidenciou continuidade discreta (+), caracterizada pela expressão de menos de 50% da laminina da membrana basal. Continuidade moderada (++) foi expressa em 4 casos (33,3%) e a perda quase que total da continuidade (+/-) foi notada em 2 casos (16,6%). Em nenhuma das lesões foi observado um padrão de continuidade linear (+++) semelhante à membrana basal de epitélio normal.
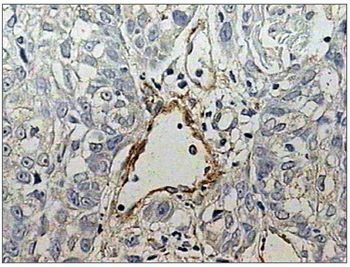
Figura 5. Ausência de expressão imuno-histoquímica da laminina. (Streptavidina biotina, 100X)
Comparando-se os valores médios da intensidade e continuidade de marcação imuno-histoquímica da laminina entre os carcinomas de baixo e alto grau de malignidade, observou-se diferenças estatisticamente significativas. (Tabela 2).
O teste de correlação de Spearman mostrou haver correlação estatisticamente significante entre a intensidade e a continuidade de marcação da laminina e o grau histológico de malignidade dos carcinomas estudados. (Tabela 3).
DISCUSSÃOA matriz extracelular é uma estrutura constituída por proteínas e polissacarídeos que são secretados localmente e distribuídos em uma extensa rede organizada associada à superfície celular. Na interface entre epitélio e tecido conjuntivo, a matriz é chamada de lâmina ou membrana basal, uma cobertura fina, porém resistente, que possui importante papel no controle do comportamento celular6. Na sua composição estão presentes proteínas como o colágeno do tipo IV, heparam sulfato, fibronectina, entactina e a laminina7, uma glicoproteína que desempenha diversas funções, tais como adesão celular, migração, atividade proteolítica, proliferação celular, crescimento tumoral e metástase8.
A membrana basal não é uma estrutura estática, e sim dinâmica, remodelada constantemente, por processos de rupturas e sínteses de glicoproteínas, como a laminina. Estes processos são de suma importância na inflamação e no reparo, pois a membrana necessita ser fragmentada para que haja a entrada e saída de células que participam ativamente do processo infamatório. Essa fragmentação precisa ser reparada de forma rápida, organizada e precisa, e esse processo não acontece na presença de células tumorais. Na invasão neoplásica a síntese de glicoproteínas da membrana basal é mais lenta e desorganizada, promovendo perdas permanentes de continuidade5. Ao reconhecermos esta característica, durante a análise dos carcinomas escamocelulares da mucosa oral e, posterior avaliação da expressão da laminina, evitou-se o estudo desta glicoproteína em áreas com intenso infiltrado inflamatório para que não houvesse uma distorção dos resultados.
No momento da invasão, a maior barreira encontrada pelas células neoplásicas é a membrana basal8. Demonstrou-se que células neoplásicas de tumores escamocelulares de boca apresentam receptores de 32/67kDa para laminina que agem como uma molécula acessória de integrina, estabilizando a célula tumoral no momento da sua adesividade à laminina. A partir dessa ligação, inicia-se a secreção de enzimas por parte do tumor9,10 que promoverá rupturas na membrana, através da destruição de colágeno do tipo IV e laminina, e conseqüente penetração das células tumorais para o interior do tecido conjuntivo, dando inicio ao processo de invasão11,12. Estas modificações na distribuição da membrana basal têm sido demonstradas através de técnicas imuno-histoquímicas utilizando-se anticorpos do tipo anti-colágeno IV e também anti-laminina3, anticorpo este utilizado em nosso estudo.
A membrana basal não funciona apenas como uma estrutura de suporte ou barreira para células neoplásicas. Ela também participa da sinalização no processo da angiogênese. Isto ocorre devido ao fato de que diversas moléculas identificadas como moduladoras da angiogênese, fatores de crescimento e citocinas ficam estocados na membrana basal, e são apenas liberados e ativados mediante sua dissolução. A laminina, por exemplo, ao ser degradada, expõe sítios que induzem a angiogênese, o que é crítico para sobrevivência das células neoplásicas8. Isso é confirmado pelo nosso estudo ao observarmos um aumento do número de vasos sanguíneos próximos à frente de invasão neoplásica, quando comparado a áreas de epitélio normal.
A perda da membrana basal, evidenciada pela diminuição da expressão da laminina e do colágeno IV, tem sido observada em áreas com perda de diferenciação3,13,14, indicando que essas regiões em breve serão sítios de progressiva invasão neoplásica no estroma adjacente15. Este fato é comprovado por Jiang et al. (1994)16 e Harada et al. (1994)17, ao observarem menor expressão de laminina em tumores metastásicos. Em nosso estudo, das 12 lesões consideradas de alto grau de malignidade, 2 lesões não expressaram a laminina, e em outras 8 observou-se marcação com uma intensidade considerada discreta. Um achado histológico interessante é que neste grupo de lesões não foi observado nenhum caso com intensa marcação para a laminina. Quando os valores médios das variáveis intensidade e continuidade foram confrontados com os diferentes graus de malignidade, observou-se diferenças estatisticamente significantes. Estudos imuno-histoquímicos em membrana basal de carcinoma da mucosa oral realizados por Aznavoorian et al. (1993)11 e Nigar & Dervan (1998)18 chegaram a resultados semelhantes.
A laminina tem sido investigada também em outras lesões a exemplo dos tumores de pele19, tumores de glândulas salivares20-22 e em neoplasias malignas de cólon e reto9. Em alguns destes estudos uma maior expressão desta glicoproteína foi encontrada na membrana basal de lesões bem diferenciadas. Estes resultados refletiram os achados da nossa pesquisa, pois foi demonstrado estatisticamente que a intensidade mais acentuada de expressão da laminina esteve relacionada às lesões mais diferenciadas.
Na análise da expressão da laminina de acordo com a integridade da membrana basal, os nossos resultados demonstraram que nenhuma das lesões consideradas de alto grau de malignidade mostrou padrão contínuo de marcação, compatível com o epitélio normal. No entanto, neste grupo, observou-se que 4 lesões mantiveram a membrana basal com mais de 50% de integridade. Esta característica foi embasada por Kumagai et al. (1994)23 e Bosman & Stamenkovic (2003)24, que estabeleceram em seus respectivos estudos que a perda de componentes da membrana basal nem sempre ocorre em todos os momentos de invasão tumoral. A membrana basal em volta das células tumorais é fragmentada durante os estágios ativos da invasão e reconstituída nos estágios de latência.
Tumores mais diferenciados, conseqüentemente menos invasivos, expressaram um padrão de marcação para laminina que se assemelha bastante ao epitélio normal. No presente estudo, entre os 19 tumores classificados como de baixo grau de malignidade, 10 casos apresentaram continuidade na expressão da laminina. Isto indica que as células adjacentes à membrana basal e as células tumorais ainda possuíam a capacidade de secretar esta glicoproteína o que vem a confirmar o já descrito na literatura7,8,12, 25.
Maatta et al. (2001)1, em um estudo realizado através de marcações específicas para as diferentes isoformas de laminina, constataram que os carcinomas humanos são geralmente capazes de sintetizar quantidades substanciais de diferentes cadeias desta glicoproteína. Observou-se que carcinomas possuíam em suas respectivas membranas basais quase todas as cadeias de laminina existentes, sugerindo que a capacidade de deposição de macromoléculas da membrana basal não é totalmente perdida durante o processo de invasão15,26. Talvez isto explique a moderada expressão da laminina em 2 lesões com alto grau de malignidade.
Firth & Read (1996)15 constataram uma grande freqüência de defeitos focais da laminina na membrana basal de tumores nos estágios clínicos T3 e T4. Resultados semelhantes foram observados em lesões nos estágios clínicos T1 e T223. Assim, entende-se que a expressão de componentes da membrana basal é melhor correlacionada com os estágios de diferenciação do tumor, como em nosso estudo, e não com suas graduações clínicas.
CONCLUSÃONo presente estudo conclui-se que houve menor expressão imuno-histoquímica da laminina na membrana basal de carcinoma escamocelular de boca com alto grau de malignidade. Sugere-se que esta modificação estrutural pode comprometer o dinamismo da membrana basal e favorecer a invasão tumoral.
REFERÊNCIAS BIBLIOGRÁFICAS1. Maatta M, Virtanen I, Burgeson R, Autio- Harmainen H. Comparative analysis of the distribution of laminin chains in the basement membranes in some malignant epithelial tumors: the alpha1 chain of laminin shows a selected expression pattern in human carcinomas. J Histochem Cytochem 2001;:711-26.
2. Shinohara M, Nakamura S, Harada T, Shimada M, Oka M. Mode of tumor invasion in oral squamous cell carcinoma: improved grading based on immunohistochemical examination of extracellular matrices. Head Neck 1996;:153-9.
3. Garcia AS, Hernández MMA, Sánchez EF, Gonzalez RJ, Villardón PG, Hernández JJC et al. E-caderin, laminin and collagen IV expression in the evolution from dysplasia to oral squamous cell carcinoma. Med Oral Patol Oral Cir Bucal 2006;:E100-5.
4. Anneroth G, Batsakis J, Luna M. Review of the literature and a recommended system of malignancy grading in oral squamous cell carcinomas. Scand J Dent Res 1987;229-49.
5. Kannan S, Balaram P, Chandran GJ, Pillai MR, Mathew B, Nalinakumari KR et al. Alterations in expressions of basement membrane proteins during tumor progression in oral mucosa. Histopathology 1994:531-7.
6. Alberts B. Junções celulares, adesão celular e a matrix extracelular. 3ª ed. Porto Alegre (RS): Artes Médicas; 1997.
7. Hirota J, Yoneda K, Osaki T. Basement membrane type IV collagen in oral squamous cell carcinoma. Head Neck 1990:400-5.
8. Engbring JA, Kleinman KH. The basement membrane matrix in malignancy. J Pathol 2003:465-70.
9. Hewitt ER, Desmond G, Powe G, Carter I, David R, Turmer E et al. Basement membrane collagen IV synthesis in colorectal tumors, Int J Cancer 1992:530-6.
10. Wu XZ, Chen D, Xie GR. Extracellular matrix remodeling in hepatocellular carcinoma: Effects of soil on seed? Medical Hypotheses 2006:1115-20.
11. Aznavoorian S, Murphy AN, Stevenson WGS, Liota LA. Molecular aspects of tumor cell invasion and metastasis. J Pathol 1993:1368-83.
12. Wilson DF, Jiang D, Smith PS, Pierce AM, Wiebkim OW. Oral cancer: role of the basement membrane in invasion. J Aust Dent 1999:93-7.
13. Gomes APN. Expressão imuno-histoquímica de proteínas da membrana basal e beta-catenina em lesões bucais potencialmente malignas. [Dissertação] São Paulo (SP); 2001.
14. Haas KM, Berndt A, Stiller KJ, Hyckel P, Kosmehl H. A comparative quantitative analysis of laminin-5 in the basement membrane of normal, hyperplastic, and malignant oral mucosa by confocal immunofluorescence imaging. J Histochem Cytochem 2001:1261-8.
15. Firth NA, Reade PC. The prognosis of oral mucosal squamous cell carcinomas: a comparison of clinical and histopathological grading and of laminin and type IV collagen staining. J Aust Dent 1996:83-6.
16. Jiang D, Wilson DF, Smith PS, Pierce AM, Wiebkim OW. Distribuition of basal lamina IV collagen and laminin in normal rat tongue mucosa and experimental oral carcinoma: ultraestructural imunolocalization and imunogold quantitation. Euro J Cancer B Oral Oncol 1994:237-43.
17. Harada T, Shinohara M, Nakamura S, Oka M. An immunohistochemical study of the extracellular matrix in oral squamous cell carcinoma and its association with invasive and metastatic potential. Virchows Arch 1994:257-66.
18. Nigar E, Dervan PA. Quantitative assentment of basement membranes in soft tissue tumors. Computerized image analysis of laminina and type IV collagen. J Pathol 1998:184-7.
19. Kondo T, Ohshima T, Yasunori S, Mayama T, Eisenmenger W.Immunohistochemical study on the expression of extracelular matrix in human skin wounds. The Histochemical Jornal 2000:509-14.
20. Karja V, Syrjanen K, Syrjanen S. Collagen IV, laminin and tenascin immunorectivity as prognostic determinant in benign and malignant salivary gland tumors. Acta Otolaryngol 1995:569-75.
21. Kumamoto M, Kuratomi Y,Yasumatsu R, Nakashima T, Masuda M, Inokuchi A. Expression of laminin 5 basement membrane components in invading and recurring adenoid cystic carcinoma of head and neck. Auris Nasus larynx [serial on line] sep 2005. Encontrado em: www.elsevier.com/locate/anl
22. Raitz R, Martins MD, Araújo VC. A study of the extracellular matrix in salivary gland tumors. J Oral Pathol Med 2003:290-6.
23. Kumagai S, Kojima S, Imai K, Nakagawa K, Yamamoto E, Kawarrara N. Immunohistological distribuition of basement membrane in squamous cell carcinoma. Head Neck 1994:51-7.
24. Bosman FT, Stamenkovic I. Functional structure and composition of the extracellular matrix, J Pathol 2003:423-8.
25. Freitas VM, Souza LNG, Oliveira EC, Furuse C, Araújo, VC, Jaeger RG. Malignancy-related 67KDa laminin receptor in adenoid cystc carcinoma. Effect on migration and b-catetin expression. J Oral Oncol [serial on line] nov 2006. Encontrado em: www.elsevierhealth.com/journals/oron/
26. Franz M, Hansen T, Borsi L, Geier C, Hyckel P, Schleier P et al. A quantitative co-localization analysis of large unspliced tenascin-CL and laminin-5/y2-chain in basement membranes of oral squamous cell carcinoma by confocal laser scanning microscopy. J Oral Pathol Med 2007:6-11.
1 Mestre em Odontologia, Professor Substituto do Departamento de Propedêutica e Clínica Integrada da Faculdade de Odontologia da Universidade Federal da Bahia.
2 Mestre em Odontologia, Professora Assistente da Faculdade de Odontologia da Universidade Estadual do Sudoeste da Bahia.
3 Bolsista do Programa de Educação Tutorial, Graduanda da Faculdade de Odontologia da Universidade Federal da Bahia.
4 Doutor em Odontologia, Professor Adjunto do Departamento de Propedêutica e Clínica Integrada da Faculdade de Odontologia da Universidade Federal da Bahia.
5 Doutora em Odontologia, Professora Adjunto do Departamento de Propedêutica e Clínica Integrada da Faculdade de Odontologia da Universidade Federal da Bahia.
Faculdade de Odontologia da Universidade Federal da Bahia.
Endereço para correspondência: Profa Drª Sílvia R. A. Reis - Rua Araújo Pinho 62 Canela. Faculdade de Odontologia da UFBA Salvador-BA Brasil 40.110-150.
Tel. (0xx71) 3336-5976; ramal: 237 - E-mail: srareis@uol.com.br
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da RBORL em 26 de setembro de 2006. cod. 3414.
Artigo aceito em 28 de junho de 2007.


