INTRODUÇÃOA via de drenagem do seio frontal (SF) é composta por três diferentes regiões e geralmente apresenta uma configuração em ampulheta. A parte mais superior da ampulheta é representada pelo SF propriamente dito, enquanto que a parte mais estreita corresponde ao óstio deste seio. A parte mais inferior da ampulheta é formada pelo recesso frontal.1-3.
O recesso frontal (RF) é um espaço de desenvolvimento variável das células pneumatizadas anteriores, o qual é usualmente chamado de "ducto" ou "canal nasofrontal"1. As paredes e limites do RF pertencem às estruturas adjacentes, sendo que o seu grau de patência é largamente determinado por essas estruturas2-4. Como esse espaço se estende para dentro do seio frontal (SF), o estado do SF é inteiramente dependente das condições do RF1.
A cirurgia endoscópica funcional do SF, que permite o tratamento seletivo do RF, apresenta resultados semelhantes às técnicas por vias externas, sendo que os trabalhos recentes reportam sucesso entre 82% a 90% dos casos tratados por esta técnica5,6. Contudo, a cirurgia do SF e RF continua sendo considerada o maior desafio da cirurgia endoscópica nasossinusal. A localização obscura dessa área, as variações anatômicas e a sua íntima proximidade com o globo ocular e a fossa craniana anterior tanto podem induzir ao cirurgião a não realizar uma adequada dissecção, como também podem expor o paciente a complicações maiores7.
Conhecimento detalhado da anatomia da parede nasal lateral e do RF é essencial para o sucesso da cirurgia endoscópica funcional do SF. O objetivo principal desse estudo de dissecção endoscópica em cadáveres foi identificar e descrever as estruturas anatômicas do recesso frontal que dificultam o reconhecimento endonasal do óstio do seio frontal.
CASUÍSTICA E MÉTODOSApós aprovação pela Comissão de Ética para Análise de Projetos de Pesquisa (CAPPesq - Protocolo no 414/02), foram estudados 32 cadáveres (59 fossas nasais) do Serviço de Verificação de Óbito.
Foram utilizados neste estudo os seguintes critérios de exclusão: idade menor do que 20 anos; agenesia de seio frontal bilateral; história prévia de trauma nasal; antecedentes de cirurgia nasossinusal; afecções nasossinusais que distorciam a anatomia local (ex: polipose nasal e tumores).
A presença do SF foi avaliada por meio de osteotomia da tábua óssea frontal em seu ponto mais inferior possível, ou seja, imediatamente acima e medial ao rebordo orbitário ipsilateral. Na presença de SF, foi realizada a cateterização do seu óstio sob visão direta com uma sonda plástica flexível, até a sua exteriorização no meato médio (Figura 1).
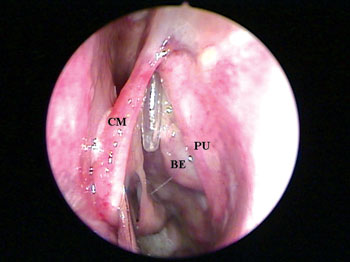
Figura 1. Endoscopia de fossa nasal esquerda evidenciando a exteriorização da sonda plástica flexível através do meato médio (CM = concha média; PU = processo uncinado; BE = bolha etmoidal).
Após a incisão e exérese endoscópica do processo uncinado (PU) utilizando uma pinça reta cortante, preservando a sua inserção superior, foi avaliada a visibilização endonasal do óstio do SF, o qual se encontrava cateterizado pela sonda plástica flexível, sem a necessidade de remoção de nenhuma outra estrutura anatômica (Figura 2). Com esta finalidade foi utilizado um endoscópio rígido 4mm de 45o posicionado no meato médio e direcionado superiormente para o RF. Quando essa visibilização direta do óstio do SF não era possível, foram identificadas quais estruturas anatômicas necessitavam ser removidas até que fosse possível a sua completa visibilização.
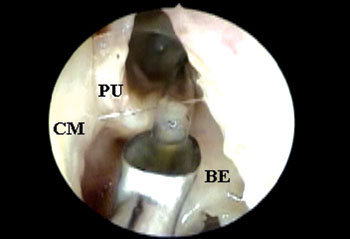
Figura 2. Endoscopia de fossa nasal esquerda com endoscópio rígido de 4mm e 45 graus evidenciando a visibilização direta do óstio do seio frontal cateterizado pela sonda plástica flexível após a remoção apenas da porção inferior do processo uncinado(CM = concha média; PU = processo uncinado; BE = bolha etmoidal).
Os dados foram divididos em grupos segundo o sexo e a raça. Nesta última, agrupamos os indivíduos da raça branca e comparamos com aqueles das raças parda e negra, conjuntamente. A análise dos dados de sexo e raça foi feita através da obtenção de dados nominais. Foram utilizados dados contínuos para quantificação do número de estruturas que impediam a visibilização do óstio do seio frontal. Foi realizada a análise da distribuição das variáveis com dados contínuos através do teste de normalidade de Komogorof-Smirnov. Para a comparação entre a visibilização endonasal do óstio do seio frontal em relação ao sexo, foi utilizado o teste exato de Fisher e, em relação à raça, o teste do qui-quadrado. Para a pesquisa da relação entre o número de estruturas impedindo a visualização do óstio do seio frontal com o sexo e com a raça, foi utilizado o teste t de Student. Foi considerado índice de significância de 95% (p<0,05).
RESULTADOSA faixa etária dos cadáveres variou de 30 a 88 anos, sendo que a média e o desvio-padrão da idade estão detalhados no Gráfico 1. Quanto ao sexo, ocorreu um predomínio do sexo masculino (Gráfico 2). A raça branca correspondeu à metade dos cadáveres, sendo que a distribuição detalhada encontra-se no Gráfico 3.
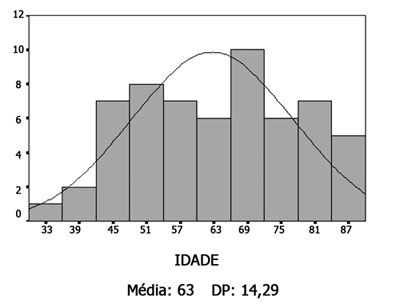
Gráfico 1. Histograma das idades (DP = desvio padrão).
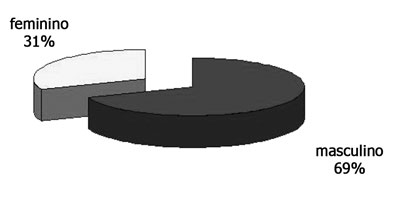
Gráfico 2. Distribuição dos cadáveres quanto ao sexo.
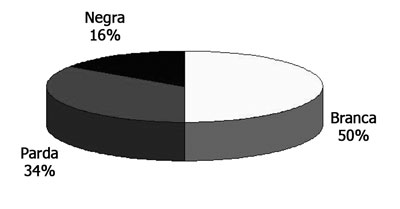
Gráfico 3. Distribuição dos cadáveres quanto à raça.
Dos 32 cadáveres dissecados, cinco (15,63%) apresentaram agenesia unilateral do SF. Logo, a avaliação em relação à visibilização endonasal do óstio do SF foi realizada em 59 fossas nasais.
A visibilização direta do óstio do SF com o endoscópio rígido 4mm de 45o posicionado no meato médio e direcionado superiormente para o RF, imediatamente após a remoção da porção inferior do PU, foi possível em 11 (18,64%) fossas nasais. Nas 48 (81,36%) fossas nasais restantes o óstio do SF, identificado pela sonda plástica flexível, não foi claramente evidenciado, sendo que as estruturas anatômicas que impossibilitaram essa visibilização serão descritas a seguir. Quando a visibilização endonasal do óstio do seio frontal, após a remoção apenas da porção inferior do processo uncinado, foi comparada em relação ao sexo, observamos que a mesma foi mais freqüente no sexo masculino, apesar de não haver uma significância estatística (p=0,079). Das 11 fossas nasais, nas quais foi possível a visibilização direta do óstio do SF, 10 eram de indivíduos do sexo masculino. Não encontramos associação entre raça e a capacidade de visibilização direta do óstio do SF (p=0,88).
O PU inserido na lâmina papirácea (recesso terminal), evidenciado em 45 (76,27%) fossas nasais, foi a principal estrutura anatômica que impossibilitou a visibilização endonasal do óstio do SF entre as 59 fossas nasais avaliadas (Figuras 3A e 3B), seguido pela bolha etmoidal (Figuras 4A e 4B) que esteve presente em 10 (16,95%) fossas nasais e a célula agger nasi (Figuras 5A e 5B) em 4 (6,78%) fossas nasais.
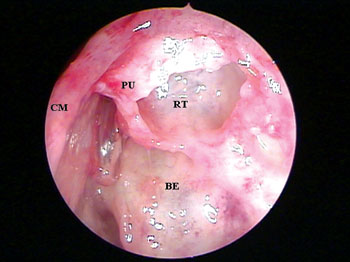
Figura 3A. Endoscopia de fossa nasal esquerda com endoscópio rígido de 4mm e 45 graus evidenciando a presença de recesso terminal dificultando a visibilização direta do óstio do seio frontal;
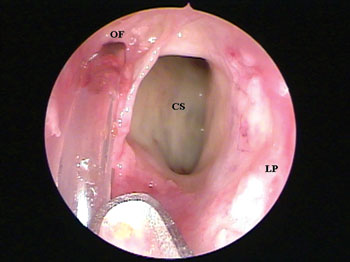
Figura 3B. Visibilização do óstio do seio frontal cateterizado pela sonda plástica flexível e localizado medialmente a uma célula supra-orbitária após exérese do recesso terminal (CM = concha média; PU = processo uncinado; BE = bolha etmoidal; OF = óstio do seio frontal; CS = célula supra-orbitária; RT = recesso terminal; LP = lâmina papirácea).
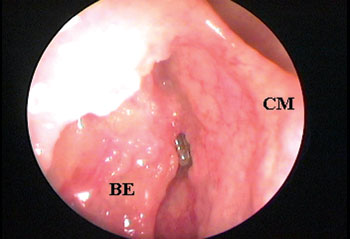
Figura 4A. Endoscopia de fossa nasal direita com endoscópio rígido de 4mm e 45 graus evidenciando a presença da bolha etmoidal dificultando a visibilização endonasal do óstio do seio frontal;
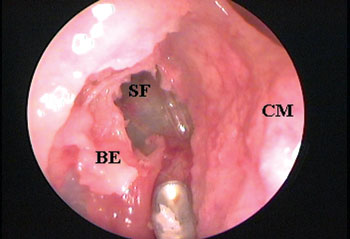
Figura 4B. Exérese da porção superior da bolha etmoidal e conseqüente visibilização do óstio do seio frontal cateterizado pela sonda plástica flexível (CM = concha média; BE = bolha etmoidal; SF = seio frontal).
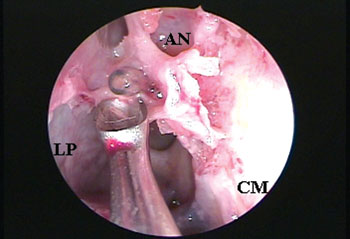
Figura 5A. Endoscopia de fossa nasal direita com endoscópio rígido de 4mm e 45 graus evidenciando a presença de uma célula agger nasi dificultando a visibilização endonasal do óstio do seio frontal.
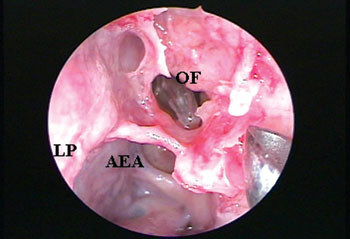
Figura 5B. Exérese da célula agger nasi e conseqüente visibilização do óstio do seio frontal cateterizado pela sonda plástica flexível (CM = concha média; LP = lâmina papirácea; AN = agger nasi; OF = óstio do seio frontal; AEA= artéria etmoidal anterior).
Em 11 (18,64%) das 59 fossas nasais, mais de uma estrutura anatômica estava encobrindo o óstio do SF, sendo que a associação entre o processo uncinado e a bolha etmoidal, presente em nove (15,25%) fossas nasais, foi a mais freqüente. A outra associação encontrada foi entre o processo uncinado e a célula agger nasi, evidenciada em duas (3,39%) fossas nasais.
Comparando os indivíduos da raça branca com os pardos e negros em relação ao número de estruturas impedindo a visibilização do óstio do SF, não observamos diferença estatisticamente significante (p=0,68), fato também observado quando os grupos foram comparados em relação ao sexo (p=0,31).
DISCUSSÃOSegundo Caliot et al.8 (1990), o óstio do SF encontra-se localizado quase sempre profundo e de difícil visibilização. Essa afirmação corrobora com o presente estudo no qual a visibilização direta do óstio do SF com o endoscópio de 45o, imediatamente após a remoção da porção inferior do PU foi possível em apenas 11 (18,64%) das 59 fossas nasais avaliadas. Nas 48 (81,36%) fossas nasais restantes, o óstio do SF encontrava-se encoberto por alguma estrutura anatômica. Provavelmente devido a esse alto índice de dificuldade em se identificar o óstio do SF, Stamberger4 (1999) afirma que o acesso endonasal ao SF sem dúvida requer profundo conhecimento anatômico, grande habilidade cirúrgica e destreza.
O PU foi a principal estrutura anatômica que impossibilitou a visibilização endonasal do óstio do SF entre as 59 fossas nasais avaliadas. Em 45 (76,27%) fossas nasais a inserção superior do PU esteve presente encobrindo o óstio do SF, isoladamente ou em associação com outras estruturas anatômicas. Ao analisar esses resultados, podemos inferir que de maneira similar ao óstio natural do seio maxilar, o qual pode ser exposto após a remoção da porção mais inferior do PU, o óstio do SF pode, na maioria das vezes, ser exposto após a remoção da inserção superior do PU. Logo, concordamos com Friedman et al.7 (2000) ao afirmarem que a identificação das variações anatômicas do PU e a precisa remoção cirúrgica da sua inserção superior permitem o acesso cirúrgico ao SF através da identificação do seu óstio natural, o que torna maior a chance do mesmo permanecer patente. Consideramos também fundamental a observação realizada por Lee et al.9 (1997) de que o cirurgião deve inspecionar a anatomia do RF antes de remover o PU (o deslocamento medial da concha média normalmente é necessário), e após a uncinectomia, mas antes de completar a etmoidectomia. As variações em relação à drenagem do SF devem ser identificadas e as estruturas adjacentes analisadas.
O significado da inserção do PU na lâmina papirácea já havia sido observada por Kasper10 desde 1936, quando o mesmo escreveu que o conhecimento desse freqüente fundo cego do infundíbulo etmoidal é importante para o médico realizar cirurgias no nariz. Os nossos resultados reforçam ainda mais esta colocação de Kasper10, pois além do recesso terminal ter sido de ocorrência bastante freqüente, a sua identificação tornou-se fundamental para uma correta dissecção e acesso ao óstio do SF, dissecção esta realizada medialmente ao PU.
A extensa pneumatização da BE, posterior ao RF, e da célula agger nasi, anterior a este recesso, predispõem à aparência semelhante a um ducto nos cortes sagitais, daí a incorreta denominação de "ducto nasofrontal" por alguns autores. Muitos recessos frontais parecem drenar superior e medial ao infundíbulo etmoidal, alguns drenam diretamente no infundíbulo etmoidal e poucos drenam no recesso retro-bular2. O recesso retrobular é o espaço situado entre a BE e a lamela basal da concha média, também denominado de seio lateral. Desde 1936, KASPER10 já havia relatado a drenagem do SF para o recesso retrobular em 2% dos casos. Chamou a atenção para o fato de que essa condição, apesar de ser rara, resultava em um difícil acesso endonasal para o SF, principalmente devido a uma acentuada angulação decorrente da projeção da BE. De maneira semelhante a KASPER10 (1936), Van Alyea11 (1946) e Kim12 (2001) observam que em apenas 1% dos casos o SF drenava diretamente para o recesso retrobular.
A BE foi a segunda estrutura anatômica que mais dificultou a visibilização endonasal do óstio do SF, fato ocorrido em 10 (16,95%) entre as 59 fossas nasais avaliadas. Em 4 (6,78%) casos o óstio do SF estava drenando para o recesso retrobular e em 6 (10,17%) casos a hiperpneumatização da bolha etmoidal impossibilitava a identificação endonasal do óstio do seio frontal.
Como na maioria das vezes a parede posterior do RF é formada pela lamela basal da BE, concordamos com Loury13 (1993) quando o mesmo afirma que a BE intacta, além de proteger a artéria etmoidal anterior, é um excelente reparo anatômico para a margem posterior do recesso e SF, devendo ser preservada durante o acesso cirúrgico endoscópico do RF sempre que possível. Gostaríamos apenas de ressaltar o fato de que a BE eventualmente pode representar a parede anterior do RF ou a sua pneumatização anterior pode recobrir o óstio do frontal, sendo assim, nos casos de não-identificação do óstio do SF após a adequada e criteriosa remoção de toda inserção ântero-superior do PU, a remoção da BE deve ser necessariamente o passo seguinte do procedimento cirúrgico.
A célula agger nasi, a mais anterior célula etmoidal pneumatizada, está presente em mais de 98% dos pacientes. Esta célula pode pneumatizar posteriormente em direção ao RF, podendo causar problemas relacionados à obstrução do SF variando de mucocele assintomática até cefaléias e outras sinusopatias. A localização e o grau de pneumatização da célula agger nasi são muito variáveis14. Algumas vezes torna-se difícil diferenciar entre uma célula agger nasi e um recesso terminal alto porque ambos aparecem ântero-superiormente como um fundo cego15. Apesar da célula agger nasi ser bastante constante e presente na anatomia nasossinusal do ser humano, a sua contribuição em dificultar a visibilização o óstio do SF foi a menor em nosso estudo (6,78% dos casos).
CONCLUSÃOO processo uncinado inserido na lâmina papirácea (recesso terminal) representou a principal estrutura anatômica que dificultou o reconhecimento do óstio do seio frontal, seguido pela bolha etmoidal e a célula agger nasi.
REFERÊNCIAS BIBLIOGRÁFICAS 1. Messerklinger W. Uber den Recessus frontalis und seine klinik. Laryngol Rhinol Otol 1982;61:217-223.
2. McLaughlin RB, Rehl RM, Lanza DC. Clinically relevant frontal sinus anatomy and physiology. Otolaryngol Clin North Am 2001;34(1):1-22.
3. Stammberger H. Functional Endoscopic Sinus Surgery - The Messerklinger Technique. Philadelphia, PA: BC Decker; 1991.
4. Stammberger H. "Uncapping The Egg"- The Endoscopic Approach to Frontal Recess and Sinuses. Tuttlingen: Endo-Press; 1999.
5. Metson R. Endoscopic treatment of frontal sinusitis. Laryngoscope 1992;102:712-6.
6. Schaefer SD, Close LG. Endoscopic management of frontal sinus disease. Laryngoscope 1990;100:155-60.
7. Friedman M, Landsbreg R, Schults RA, et al. Frontal Sinus Surgery: Endoscopic Technique and Preliminary Results. Am J Rhinol 2000;14:393-403.
8. Caliot P, Midy D, Plessis JL. The surgical anatomy of the middle nasal meatus. Surg. Radiol Anat 1990;12:97-101.
9. Lee D, Brody R, Har-El G. Frontal Sinus Outflow Anatomy. Am J Rhinol 1997;11:283-5.
10. Kasper KA. Nasofrontal connections: a study of one hundred consecutive dissections. Arch Otolaryngol 1936;23:322-43.
11. Van Alyea OE. Frontal sinus drainage. Ann Otol Rhinol Laryngol 1946;55:267-77.
12. Kim KS, Kim HU, Chung IH, Lee JG, Park IY, Yoon JH. Surgical anatomy of the nasofrontal duct: anatomical and computed tomographic analysis. Laryngoscope 2001;111:603-8.
13 Loury MC. Endoscopic frontal recess and frontal sinus ostium dissection. Laryngoscope 1993;103:455-8.
14. Kuhn FA, Bolger WE, Tisdal RG. The Agger nasi cell in frontal Recess obstruction: An anatomic, radiologic and clinical correlation. Op Tech Otolaryngol Head Neck Surg 1991;2(4):226-31.
15. Landsberg R, Friedman M. A computer-assisted anatomical study of the nasofrontal region. Laryngoscope 2001;111:2125-30.
1 Doutor em Ciências pela Disciplina de Otorrinolaringologia da FMUSP; Pesquisador Associado dos Serviços de Imunologia e Otorrinolaringologia do HUPES da Universidade Federal da Bahia; Fellow em Cirurgia Endoscópica Nasossinusal pela Universidade de Graz/Áustria.
2 Professor Associado da Disciplina de Otorrinolaringologia da Faculdade de Medicina da Universidade de São Paulo.
3 Doutorando da Disciplina de Otorrinolaringologia da Faculdade de Medicina da Universidade de São Paulo.
4 Doutorando da Disciplina de Otorrinolaringologia da Faculdade de Medicina da Universidade de São Paulo.
5 Professor Associado da Disciplina de Otorrinolaringologia da Faculdade de Medicina da Universidade de São Paulo.
6 Professor do Departamento de Otorrinolaringologia da Universidade de Graz - Áustria.
Divisão de Clínica Otorrinolaringológica do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
Endereço para correspondência: Marcus Miranda Lessa - Rua João das Botas s/n Canela 40110-160 Salvador BA.
Serviço de Imunologia - 5º andar Hospital Universitário Prof. Edgard Santos UFBA
Fax: (0xx71) 245-7110 - E-mail: imuno@ufba.br/ lessamm@terra.com.br
EsEste artigo foi submetido no SGP (Sistema de Gestão de Publicações) da RBORL em 21 de maio de 2006. cod. 1956.
Artigo aceito em 2 de julho de 2006.


