INTRODUÇÃOFisiopatologia coclear e zonas mortas na cóclea
A região da cóclea onde as células ciliadas internas (CCI) estão lesadas, inativas, ou ausentes, e os neurônios que inervam essa região estão inativos ou até degenerados, tem sido chamada de região morta da cóclea ou zona morta.1-3
Apesar do conceito de zona morta ter sido citado há vários anos por Gravendeel e Plomp4, o mesmo não havia despertado muito interesse clínico, até que Moore et al., em suas recentes publicações acerca do tema, retomaram a utilização do termo. Os autores a descrevem pela característica de freqüência da CCI lesadas e/ ou pelos neurônios da zona morta.3,5,6
As configurações do audiograma também foram consideradas como evidência para a presença de zonas mortas, como, por exemplo, nos audiogramas em rampa, onde os limiares pioram bruscamente com o aumento da freqüência (mais que 50dB/oitava), em altas freqüências. Perdas auditivas de 40-50dB nas baixas freqüências e audição próxima do normal nas médias e altas freqüências podem indicar zona morta nas baixas freqüências, o que provavelmente acontece também em perdas auditivas maiores que 50dB nas baixas freqüências, com limiares melhores para as altas freqüências. Audiogramas em "U", com audição melhor para baixa e altas freqüências e zona morta nas freqüências médias, são considerados os mais raros e em geral não interferem significativamente na compreensão da fala, pois a audição residual contribui para um bom reconhecimento, descartando, em alguns casos, a necessidade do uso de aparelhos de amplificação sonora individuais (AASI).5
Huss et al. investigaram a percepção do tom puro por indivíduos com e sem zonas mortas, diagnosticadas pela curva psicofísica de sintonia e pelo teste TEN, onde os participantes eram instruídos a pontuar a nitidez de um tom puro, numa escala que variava de nítido (1) a ruidoso (7). Os autores concluíram que a impressão subjetiva de nitidez do tom puro não é um indicativo consistente da presença de zonas mortas na cóclea, pois o aumento da pontuação foi observado não só em orelhas com regiões mortas, mas também sem as mesmas, coincidindo nas freqüências em que os limiares eram maiores.7
Portanto, torna-se evidente que apenas o audiograma ou o relato do paciente não são suficientes para determinar a presença ou não de regiões mortas, muito menos identificar sua extensão. Assim, alguns experimentos têm utilizado o mascaramento para investigá-la.
Avaliação de zonas mortas na cóclea
A pesquisa de zonas mortas utiliza o mascaramento ipsolateral, ou seja, o sinal de teste e o ruído mascarante são apresentados na mesma orelha, a fim de elevar o limiar das freqüências não-testadas de modo que estas não possam responder por meio de difusão da excitação ao sinal que está sendo oferecido na freqüência testada.
Moore et al. desenvolveram um teste denominado de Threshold-Equalizing Noise (TEN - ruído de equalização dos limiares) para investigar a presença de zonas mortas. Vale ressaltar que, apesar do mascaramento ser definido como um procedimento utilizado dentro da avaliação audiológica, e não um teste propriamente dito, o TEN é considerado pelos autores como tal, pois é baseado na detecção de tons puros por indivíduos com audição normal ou com perda de audição, mas sem zona morta, na presença de um ruído de banda larga (TEN), desenvolvido para produzir praticamente o mesmo nível de mascaramento (em dBNPS) por toda a extensão de freqüências do audiograma (250 Hz a 10000 Hz).3,5
No Brasil, Eguti investigou a eficiência da técnica de mascaramento com ruído branco para identificar possível presença de zonas mortas na cóclea em 32 indivíduos adultos que apresentavam perda auditiva adquirida neurossensorial ou mista e configuração audiométrica descendente. Os critérios estabelecidos por Moore5 e os resultados com o teste de mascaramento com o uso do ruído branco apresentaram concordância muito forte (concordância Kappa = 96,1%). A autora concluiu que a técnica de mascaramento com uso do ruído branco é um teste confiável e de simples aplicação que pode ser utilizado em rotina clínica para identificação de possível presença de zonas mortas na cóclea em perdas auditivas neurossensoriais adquiridas de configuração descendente.8
O diagnóstico de zonas mortas na cóclea é importante na prática clínica, pois estudos sugerem que sua presença limita a adaptação de AASI, com mínimo ou nenhum benefício observado com a amplificação dessas regiões.5,6,9
OBJETIVOO presente trabalho teve como objetivo investigar, por meio do teste TEN, a presença de zonas mortas na cóclea de indivíduos com perda auditiva neurossensorial atendidos no Centro dos Distúrbios da Audição, Linguagem e Visão (CEDALVI) do Hospital de Reabilitação de Anomalias Craniofaciais da Universidade de São Paulo, campus Bauru (HRAC-USP-Bauru).
MATERIAL E MÉTODOO trabalho foi desenvolvido no CEDALVI/HRAC/USP-Bauru, no período de agosto de 2003 a fevereiro de 2004.
CASUÍSTICAPerfilDe acordo com a rotina de atendimento dos pacientes no CEDALVI, onde o paciente é acompanhado por uma equipe multidisciplinar durante o atendimento audiológico, os participantes foram avaliados por um médico otorrinolaringologista, que realizou a otoscopia e atestou se havia condições adequadas para a realização do teste TEN, ou seja, membranas timpânicas íntegras e ausência de comprometimento de orelha externa e média.
A casuística desse trabalho é apresentada na Tabela 1.
Critérios para seleção dos indivíduos
A seleção dos indivíduos foi baseada nos seguintes critérios de inclusão:
a) G1: limiares tonais aéreos dentro do padrão de normalidade (até 15dBNA);
b) G2: presença de perda auditiva neurossensorial com configuração plana de grau moderado (Davis e Silverman);10
c) G3: presença de perda auditiva neurossensorial descendente, com o grau variando entre leve a profundo.
Aspectos éticos geraisOs participantes assinaram um termo de consentimento livre e esclarecido, conforme modelo aprovado pela Comissão de Ética em Pesquisa do HRAC-USP, sob ofício no. 263/2004-UEP-CEP, atestando sua permissão para participação no trabalho e publicação dos dados obtidos.
MÉTODOSInstrumento e Procedimentoa) Calibração Biológica do TEN
Utilizou-se a técnica de calibração biológica proposta por Veniar11, e o procedimento consistiu em apresentar no mesmo fone de ouvido, ou seja, simultaneamente e ipsolateralmente, o tom puro na intensidade inicial de 30 dBNPS (mínima do audiômetro), e o ruído (TEN) sendo aumentado em passos de 5 dB até mascarar o estímulo em teste.
b) Teste TEN
Foi aplicado o teste TEN utilizando um audiômetro de dois canais, modelo PAC 2000 da Acústica Orlandi, com fone supra-aural TDH-39 P e discman Sony, modelo Digital MEGA BASS, em cabina acusticamente tratada. Para facilitar e disponibilizar a aplicação clínica do TEN, Moore et al. (2000) gravaram o teste em CD, com o ruído (TEN) em um canal, e um sinal de teste (tom puro) digitalmente gerado gravado em outro canal do CD.
O teste foi realizado de acordo com os seguintes procedimentos:
(1) A saída do CD player foi conectada com as entradas direita e esquerda do audiômetro (geralmente utilizadas para entrada de tape). A primeira faixa do CD contém um tom de calibração, e, ao iniciá-la, o VU meter dos canais direito e esquerdo do audiômetro foram ajustados para -5 dB, ou seja, 5 dB abaixo do nível zero, a fim de calibrar a relação sinal/ruído, ou seja, as diferenças de intensidade entre o tom puro e o ruído. Para as demais faixas, o nível de intensidade do ruído no canal direito era lido como 10 dB melhor que o nível indicado no dial do audiômetro e o tom puro do canal esquerdo como 10 dB pior. Assim, os controles do audiômetro puderam ser ajustados para as intensidades desejadas de tom puro e ruído, isto é, se a intensidade de tom puro e ruído desejada fosse 50 e 40dBNPS, o dial era ajustado para 40 e 50 dB, respectivamente.
(2) Os limiares absolutos (LA) e os limiares mascarados (LM), avaliados apenas por via aérea, puderam ser obtidos por meio da audiometria manual, proposta por Carhart e Jerger7, com os estímulos controlados no audiômetro, onde o CD estava acoplado. Os LA foram avaliados em dBNPS nas freqüências de 250, 500, 1000, 2000, 3000, 4000, 6000, 8000 Hz, utilizando os tons puros de testes gravados no canal esquerdo do CD. Isso foi realizado separadamente para cada orelha, e não foi necessário o uso do mascaramento contralateral, pois em nenhum caso a orelha oposta apresentou limiar suficiente para responder pela orelha testada.
(3) Os LM com o ruído (TEN) foram avaliados nas mesmas freqüências, de acordo com a configuração audiométrica. Para tanto, os dois canais do audiômetro deveriam estar funcionando. A intensidade utilizada de TEN dependia do LA do paciente por freqüência, sendo 10 dB melhor que o LA, ou seja, se o LA fosse 50 dB, o TEN deveria ser ajustado para 40 dB no dial.
(4) Se o limiar mascarado fosse apenas 5 dB pior que o limiar absoluto, o teste era repetido com uma intensidade maior de ruído mascarante.
Análise dos dadosCritérios para análise de resultadosa) Calibração biológica do TEN
Foi considerada como nível mínimo de mascaramento efetivo a quantidade de ruído (TEN) necessária para eliminar o tom de teste (30dBNPS) por freqüência.
b) Teste TEN
De acordo com os critérios de Moore et al.3, foi considerado indicativo de zona morta na cóclea quando, em uma determinada freqüência, o LM era no mínimo 10 dB pior que o LA e 10 dB pior que o ruído mascarante (TEN). Se o LM fosse igual ao LA não era considerado indicativo de zona morta. Assim, caso a diferença entre LA e LM fosse de 5dB, ou se não houvesse intensidade suficiente disponível no audiômetro para avaliar o LM, o resultado era considerado inconclusivo.
c) Método Estatístico
A análise estatística foi realizada por meio dos seguintes testes: teste t (teste para comparação de duas amostras emparelhadas ou teste t-student), o coeficiente de correlação por postos de Spearman. Foi fixado em 5% o valor para rejeição da hipótese de nulidade (Ho).
RESULTADOSEstudo sobre a variação dos limiares absolutos com o uso do ruído TENSão apresentados, na Tabela 2, os resultados para os limiares absolutos e valores de limiares obtidos sob o uso do ruído TEN para o grupo G1.Conforme pode se observar na Tabela 2, o valor de TEN necessário para eliminar o tom de teste (LA) foi, em média, próximo ao LA para todas as freqüências, demonstrando a efetividade do mascaramento, visto que a diferença mínima oferecida pelo dial entre intensidades de estímulo é de 5dB e o desvio padrão variou de 2,42 a 3,54dB.
A seguir são apresentados, nas Tabelas 3 e 4, os resultados obtidos nos grupos G2 e G3
De acordo com os critérios de Moore et al.3, não foi observada na Tabela 3 presença de zona morta para nenhuma das orelhas testadas. As orelhas 7 e 11, nas freqüências de 6kHz e 3kHz, respectivamente, apresentaram LM 5dB pior que o LA, e não foi possível pesquisar a freqüência de 8KHz da orelha 3, pois apresentou desconforto auditivo. Para essas três orelhas, o teste foi considerado inconclusivo para a presença de zona morta.
Para o grupo G3 (Tabela 4), foi realizada uma análise de freqüência de ocorrência, conforme demonstram as Figuras 1, 2 e 3.
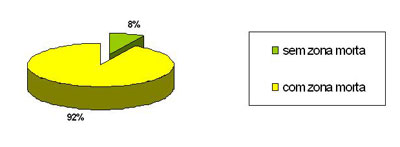
Figura 1. Freqüência de ocorrência de zonas mortas para 76 orelhas do grupo G3.

Figura 2. Freqüência de ocorrência de resultados inconclusivos e sem zona morta para 6 orelhas com resultados não indicativos de zona morta do grupo G3.
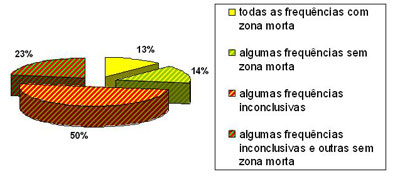
Figura 3. Freqüência de ocorrência de resultados inconclusivos e sem zona morta para 70 orelhas com resultados indicativos de zona morta do grupo G3.
Para o grupo G3, que apresentou indícios de zonas mortas na cóclea segundo os critérios estabelecidos por Moore et al.3, foi realizada análise estatística utilizando o teste t (Ho= A=B e H1= B>A), para verificar se, no caso de perdas auditivas neurossensoriais descendentes, é maior a presença de zonas mortas nas altas freqüências, definida pelo valor da diferença entre LM e LA. Assim, foi avaliada a existência de acréscimo na diferença entre LM e LA para as altas freqüências. De acordo com a análise estatística, a diferença entre o LM e o LA de 8kHz não foi significativamente maior do que diferença entre o LM e o LA de 1kHz. O mesmo ocorreu entre 6 e 1kHz, 8 e 6kHz e 4 e 3kHz. A diferença entre o LM e o LA foi significativamente maior para 2kHz do que para 1kHz.
Comparação da diferença entre LM e LA por freqüênciasPara verificar se, no caso de perdas auditivas neurossensoriais descendentes, há diferença significativa entre o LM e o LA após a aplicação do teste TEN, foi aplicado no grupo G3 o teste t (Ho= A=B e H1= B>A), não sendo observada diferença significativa entre o LM e o LA para todas as freqüências.
Correlação da diferença entre LM e LA entre freqüênciasPara verificar se, no caso de perdas auditivas neurossensoriais descendentes, a presença de zona coclear morta pode estar associada entre diferentes freqüências, calculou-se o coeficiente de correlação por postos de Spearman (rs) (Ho= rs = 0 e H1= rs ? 0), relacionando os resultados referentes às diferenças entre LM e LA por freqüências no grupo G3.
Verificou-se que a correlação é significativa apenas entre as diferenças de LM e LA entre as freqüências de 1e 2kHz, 6 e 8kHZ e 3 e 4kHz para o grupo G3. Nas demais relações, ou seja, entre 1 e 8kHz e 1 e 6kHz a correlação não é significativa.
DISCUSSÃOA variação de 5dB sobre o limiar absoluto de audibilidade com a apresentação do TEN foi considerada como resultado indicativo de ausência de zona morta na cóclea. Essa variação foi observada no procedimento de calibração biológica com dez orelhas normais (grupo G1; Tabela 2), e na aplicação do teste TEN em quinze orelhas com perda auditiva moderada plana (grupo G2; Tabela 3), em que se observou essa diferença em apenas duas orelhas. Moore et al.3 verificaram uma variação de 2 a 3dB nos limiares de audibilidade, padronizando a diferença de 5dB como resultado inconclusivo para presença de zonas mortas. Eguti8 também verificou uma variação de 5dB sobre o limiar absoluto de audibilidade com a apresentação do ruído branco no procedimento de calibração biológica com dez ouvintes normais.
Para as setenta e seis orelhas do grupo G3 (Figura 1) se observou setenta orelhas com resultados indicativos de zonas mortas, segundo os critérios de Moore et al.3, que também relacionou como evidência para a presença de zona morta a configuração audiométrica em rampa. Todos os audiogramas do grupo G3 apresentavam, no mínimo, uma diferença de 50dB por oitava entre duas das freqüências testadas. Os resultados apresentaram diferença significativa entre o LM e LA para todas as freqüências.
Na análise estatística, pôde-se observar que a diferença entre LM e LA foi maior apenas para a freqüência de 2kHz quando comparada à de 1kHz. A diferença de 10dB entre LM e LA é definida por Moore et al.3 como indicativa de zona morta na cóclea. Nos estudos de Moore et al.3,5,6,13,14 sobre zonas mortas em altas freqüências em perdas auditivas neurossensoriais descendentes, geralmente a freqüência estimada como limite da zona morta iniciava-se em 2kHz, o que justificaria a diferença entre 2kHz e 1kHz encontrada no presente estudo. Moore13 recomendou para perdas auditivas descendentes a aplicação do teste TEN a partir da freqüência de 2kHz, ou em casos que a mudança do limiar implique em alteração do grau da perda auditiva de leve ou moderado a severo.
As relações de igualdade para as freqüências de 8 e 6kHz, e 4 e 3kHz poderiam ser associadas à proximidade entre essas freqüências, já tendo sido observado que há uma diferença maior a partir de 2kHz, o que sugere uma constância nessa variação dos limiares mascarados para as altas freqüências.
As freqüências de 6 e 8kHz foram as que apresentaram mais resultados inconclusivos (Tabela 4), devido principalmente à presença de desconforto, ausência de resposta ou intensidade insuficiente de mascaramento. Esses resultados podem ter influenciado a não-observação de diferença entre as relações de LM e LA para as freqüências de 8 e 1kHZ e 6 e 1kHZ, apesar de Moore et al.3 afirmarem que freqüências com ausência de respostas para o nível mais intenso de estímulo oferecido pelo audiômetro é grande indicativo de presença de zonas mortas na cóclea.
O coeficiente de correlação por postos de Spearman foi calculado para o grupo G3, a fim de verificar se, no caso de perdas auditivas neurossensoriais descendentes, a presença ou não de zona morta poderia ser associada entre diferentes freqüências. Não houve correlação significativa entre freqüências distantes, ou seja, entre 1 e 8kHz e entre 1 e 6kHz. Entre freqüências próximas, como 1 e 2kHz e entre 3 e 4kHz para G3 e 6 e 8kHz, houve correlação significativa, o que poderia ser explicado pelo fenômeno de difusão de excitação no caso de zonas mortas dentro da área de resposta da fibra nervosa. Segundo Henderson et al.15, Bess e Humes16 e Lent17, qualquer combinação de freqüência e intensidade representada nessa área produz uma resposta da fibra nervosa, porém quando o estímulo se afasta da característica de freqüência para mais ou para menos, é preciso aumentar a intensidade para ativar a fibra. Já nas perdas auditivas neurossensoriais, em que as curvas de sintonia são mais alargadas, a excitação seria distribuída de uma forma mais ampla próxima ao limiar do que ocorreria na audição normal (Evans18).
Na Figura 1, pôde-se observar que 92% das setenta e seis orelhas testadas apresentaram resultados indicativos de zona morta, o que está de acordo com resultados de estudos anteriores, que sugerem uma grande prevalência de zona morta para indivíduos com perda auditiva neurossensorial em rampa.3,5,6,13,14,9,19 Summers et al.19 avaliaram dezoito orelhas com perdas neurossensoriais em rampa de grau moderado a severo com o TEN e o PTC ( psychophysical tuning curves). Os dois testes apresentaram concordância de resultados em presença (seis orelhas) e ausência (quatro orelhas) de zona morta para dez orelhas. Para oito orelhas os resultados divergiram para uma ou mais freqüências no TEN e no PTC, onde os resultados obtidos com o TEN sugeriam presença de zona morta e o PTC não. Os autores explicaram que a dificuldade de escutar no ruído experimentada por indivíduos com perda auditiva neurossensorial estaria relacionada ao prejuízo da atividade de filtragem devido ao alargamento da curva de sintonia, o que influenciaria para que esses indivíduos apresentassem limiares elevados com o TEN. No PTC, como o ruído é muito próximo em intensidade do limiar, não haveria dificuldade, visto que a relação sinal ruído seria maior. Para Moore et al.3, os resultados foram concordantes entre o PTC e o TEN em 20 orelhas com deficiência auditiva neurossensorial, e Eguti8 observou concordância muito forte (concordância Kappa = 96,1%) entre os critérios estabelecidos por Moore (2001) e os resultados com o teste de mascaramento com o uso do ruído branco.
No entanto, acredita-se que os resultados de testes com ruído branco para pesquisa de zona morta devam ser validados ainda com a comparação de resultados obtidos com o PTC, por ser um método já comprovado e aceito internacionalmente para pesquisas de curva de sintonia da cóclea (Halpin20).
Na pesquisa de Summers et al.19, foi utilizado um nível fixo de 70, 85 ou 90 dB/ERB de TEN, o que, para alguns limiares corresponderia a uma relação sinal/ruído (S/R) negativa. No presente trabalho, o nível do TEN era fixado em uma relação S/R +10dB, e, portanto, não haveria maiores dificuldades em relação aos filtros de ruído.
O teste TEN descrito por Moore et al.3 é um procedimento simples e baseado na rotina de pesquisa de limiares tonais aéreos, porém não utiliza como escala de valores para intensidade dBNA, que é a medida convencional utilizada na prática clínica para descrição do audiograma. O valor do ruído TEN é expresso em dB/ERB e foi calibrado para ser equivalente ao dBNPS. Dessa forma, o clínico precisa primeiramente pesquisar os limiares tonais aéreos em dBNA pelo estímulo do audiômetro e depois convertê-los em dBNPS, o que demanda tempo adicional na rotina de diagnóstico audiológico. Uma opção é a utilização do tom puro em dBNPS gravado no CD do teste TEN, que foi adotada no presente trabalho. No entanto, essa conduta é viável apenas quando se tem o objetivo de investigar a presença de zona morta, o que, por sua vez, só pode ser definido após a conclusão de um audiograma com configurações que indiquem essa lesão, como, por exemplo, diferença inter-oitavas igual ou maior que 50dB5. Moore21 indicou também a aplicação do TEN em indivíduos que relatam perceber o tom puro como "barulho, e não apito", para usuários de AASI que não observam benefícios com a amplificação, para definição de indicação de implante coclear de curta inserção e na audiometria ocupacional, como suporte legal nos casos em que as altas freqüências poderiam estar mais prejudicadas do que o indicado pelo audiograma convencional.
Durante o teste TEN a leitura no dial do audiômetro pode ser confusa, pois de acordo com as recomendações de Moore el al.3, o nível de intensidade do ruído no canal direito deve ser lido como 10dB melhor que o nível indicado no dial, e o tom puro do canal esquerdo como 10dB pior.
Para contemplar essas dificuldades apresentadas na aplicação do teste TEN, Moore22 apresentou no site de seu laboratório (hearing. psychol.cam.ac.uk) uma nova versão publicada em CD, o TEN(HL), agora calibrado em dBNA e com o nível do tom puro e do ruído correspondentes ao valor do dial.
Apesar de observada diferença significativa entre o LM e LA para todas as freqüências, o número de resultados inconclusivos obtidos (Figura 1) e a forma de calibração da versão do TEN utilizada nessa pesquisa, bem como os resultados de Summers19 que observou divergência entre o TEN e o PTC para 8 orelhas de 18 avaliadas, questiona-se sobre a necessidade de novas investigações que demonstrem a sensibilidade do TEN para detectar zonas mortas da cóclea.
Conforme sugeriu Moore5, elevação dos limiares no TEN pode representar problemas centrais, e não zona morta, porém, vale ressaltar que nesse trabalho foi observada diferença significativa entre LM e LA apenas para perdas auditivas descendentes e não para as planas, o que sugere uma diferença na detecção do tom puro na presença de ruído para indivíduos com perda auditiva em altas freqüências e também para aqueles com perda auditiva plana.
CONCLUSÃOA partir da análise crítica dos resultados obtidos no presente estudo, foi possível concluir que:
- Observa-se presença de zona morta na cóclea em 92% das perdas auditivas neurossensoriais descendentes e ausência nas perdas planas.
- O teste TEN é efetivo para indicar presença de zona morta da cóclea em indivíduos com perda auditiva neurossensorial descendente.
REFERÊNCIAS BIBLIOGRÁFICAS1. Moore BCJ. Perceptual consequences of cochlear hearing loss and their implications for the design of hearing aids. Ear Hear 1996;17(12):133-61.
2. Moore BCJ, Glasberg BR. A model of loudness perception applied to cochlear hearing loss. Auditory Neuroscience 1997;3:289-311.
3. Moore BCJ, Huss M, Vickers DA, Glasberg BR, Alcântara JI. A test for diagnosis of dead regions in the cochlea. Br J Audiol 2000;34:205-24.
4. Gravendeel DW, Plomp R. Perceptive bass deafness. Acta Otolaryngol 1960;51:549-60.
5. Moore BCJ. Dead regions in the cochlea: diagnosis, perceptual consequences, and implications for the fitting of hearing aids. Trends in Amplification 2001;5:1-34.
6. Moore BCJ. Dead regions in the cochlea: implications for the choice of high-frequency amplification. In: Seewald RC, Gravel JS, Ed. A sound foundation through early amplification 2001: Proceedings of the second international conference. Great Britain: St. Edmundsburry Press; 2002. p.153-66.
7. Huss M, Moore BCJ, Baer T, Glasberg B. Perceptions of pure tones by listeners with and without a dead region. Br J Audiol 2001;35:149-50.
8. Eguti EY. Identificação das zonas mortas na cóclea utilizando a técnica de mascaramento com ruído branco [dissertação]. São Paulo: Universidade Federal de São Paulo; 2002.
9. Vickers DA, Moore BCJ, Baer T. Effects of low-pass filtering on the intelligibility of speech in quiet for people with and without dead regions at high frequencies. J Acoustic Soc Am 2001;110 (2):1164-75.
10. Davis H, Silverman RS. Hearing and deafness. New York: Rinehart & Winston;1978.
11. Veniar FA. Individual masking levels in pure tone audiometry. Arch Otolaryng 1965;82:518-21.
12. Carhart R, Jerger JF. Preferred method for clinical determination of pure-tone thresholds. J Speech Hear Dis 1959;24:330-45.
13. Moore BCJ. Practical application of the TEN test for diagnosis of dead regions. Iranian Audiology 2002;1:17-21.
14. Moore BCJ. Response to "articulation index predictions for hearing impaired listeners with and without cochlear dead regions". J Acoustic Soc Am 2002, 111:2549-671.
15. Henderson D, Salvi RJ, Boettcher FA, Clock AE. Correlatos Neurofisiológicos da perda auditiva neurossensorial. In: Katz J, Ed. Tratado de audiologia Clínica. São Paulo: Manole; 1999, p.36-55.
16. Bess FH, Humes LE. Fundamentos de Audiologia. Porto Alegre: Artmed; 1998.
17. Lent R. Cem bilhões de neurônios:conceitos fundamentais de neurociência. São Paulo: Atheneu; 2001.
18. Evans EF. The sharping of frequency selectivity in the normal and abnormal cochlea. Audiology 1975;14:419-42.
19. Summers V, Molis MR, Müsch H, Walden BE, Surr RK, Cord MT. Identifying dead regions in the cochlea: psychophysical tuning curves and tone detection in threshold-equalizing noise. Ear Hear 2003;24(2):133-142.
20. Halpin C. The tunning curve in clinical audiology. Am J Audiol 2002;11:56-64.
21. Moore BCJ. Dead regions en the cochlea: conceptual foundations, diagnosis, and clinical applications. Ear Hear 2004;25:98-116.
22. Moore BCJ, Glasberg BR, Stone MA. A new version of the TEN test with calibrations in dBHL. Ear Hear 2004;25(5):478-487.
1 Doutora em Ciências da Reabilitação/Distúrbios da Comunicação Humana pelo Hospital de Reabilitação de Anomalias Craniofaciais da Universidade de São Paulo/Campus Bauru (HRAC/USP/Bauru), Fonoaudióloga do CEDALVI/HRAC/USP Bauru.
2 Livre-Docente da UNESP/Bauru, Professor do Programa de Pós-Graduação em Ciências da Reabilitação/Distúrbios da Comunicação Humana do HRAC/USP/Bauru.
3 Doutor em Agronomia pela UNESP/Botucatu, Chefe do Departamento de Engenharia de Produção UNESP/ Bauru.
4 Doutora em Distúrbios da Comunicação Humana pela UNIFESP/EPM, Professora Adjunto do Curso de Fonoaudiologia da UNIFESP/EPM.
Hospital de Reabilitação de Anomalias Craniofaciais da Universidade de São Paulo/ Campus Bauru.
Endereço para correspondência: Rua Ivane de Andrade Almeida 1-86 Condomínio Villagio 17018-825 Bauru SP.
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da RBORL em 11 de outubro de 2005. Cod. 1501.
Artigo aceito em 05 de maio de 2006.


