INTRODUÇÃOA Oftalmopatia de Graves é uma doença auto-imune caracterizada pela deposição de imunocomplexos antitireoglobulina nos músculos extra-oculares. Os complexos induzem a uma resposta inflamatória através de linfócitos, mastócitos e células plasmáticas, resultando em edema e posterior fibrose, com hipertrofia dos músculos extra-oculares, principalmente retos médio e inferior e gordura orbitária. Além disso, ocorre uma estimulação de atividade fibroblastomiogênica, resultando em aumento de volume orbitário, manifestado primariamente como proptose. Ocorre mais comumente em mulheres que homens, com idade média entre os 20 e 40 anos1-3.
As manifestações clínicas mais comuns são a proptose, em diversos graus de intensidade, podendo ser assimétrica ou até mesmo unilateral e a diplopia, pela motilidade anormal assimétrica da musculatura extra-ocular infiltrada por células inflamatórias. Em casos mais severos ocorre ceratoconjuntivite, retração palpebral e úlceras de córnea, por insuficiente oclusão palpebral e finalmente perda visual por neuropatia óptica, ocasionada em conseqüência da compressão no terço posterior da órbita do nervo oftálmico, junto ao ápice orbitário.
As manifestações orbitárias acometem cerca de 50% dos pacientes com doença de Graves, mas somente 5 a 10% destes desenvolvem a oftalmopatia severa.
A doença evolui lenta e progressivamente até estabilizar, havendo, entretanto, casos raros de resolução espontânea. Entretanto, aqueles pacientes que evoluem com acentuada proptose ou neuropatia óptica necessitam tratamento clinico ou cirúrgico.
Cerca de dois terços dos pacientes respondem a outros tratamentos, especialmente se empregados durante a fase aguda, que consistem de corticoterapia, irradiação orbitária (que não é eficaz para a proptose e diplopia), imunossupressores e plasmaferese. A fase aguda dura cerca de 6 a 18 meses, estando associada com inflamação e congestão da órbita, havendo um aumento do volume intra-orbitário que resulta em proptose, com deslocamento anterior do globo ocular. Evoluiu para uma fase crônica, estável, que pode iniciar de 18 meses a 3 anos após o início da orbitopatia. Nesta fase há o estabelecimento do processo fibrótico.
A orbitopatia parece seguir um caminho independente do tratamento tireoideano, e normalmente não apresenta uma relação com as anormalidades da tireóide. Pode preceder, acompanhar ou evoluir após o hipertireoidismo, ou até mesmo ocorrer na ausência de hipertireoidismo detectado.
O tratamento cirúrgico da oftalmopatia de Graves é usado para tratar as conseqüências da doença, e, portanto, é empregado na fase estável da mesma. É indicado sempre que existir sintomas de exposição da superfície ocular, neuropatia óptica ou desejo de correção estética. Ele inclui o reparo do estrabismo, ajuste da retração palpebral e descompressão orbitária para a exoftalmia6. Os principais objetivos da descompressão são obter mais espaço para acomodar o conteúdo orbital, reduzindo a pressão do tecido orbitário; restaurar a visão; permitir a função dos músculos extra-oculares e o fechamento das pálpebras, e conseqüentemente, reduzir a proptose. Cosmeticamente melhora a aparência. Vários acessos têm sido descritos para a descompressão orbitária: orbitotomia lateral, craniotomia frontal, frontoetmoidectomia externa, descompressão transantral orbital7-9. Através destes, podem ser removidas as paredes lateral ou medial da órbita, assoalho orbitário, ambos, assoalho e parede medial, ambos, assoalho e parede lateral, e fossa craniana anterior. O procedimento de Walsh-Ogura7, que utiliza um acesso via transantral foi o mais empregado. Por uma antrostomia maxilar ampla é realizada a remoção do assoalho orbitário com preservação do infra-orbitário, sendo a seguir realizada uma etmoidectomia transantral e descompressão da parede orbitária medial. Entretanto é um método associado à morbidade do procedimento de Caldwell-Luc e pode resultar em um deslocamento inferior do globo ocular, com limitações de acesso para a descompressão do ápice orbitário.
Com o advento da instrumentação endoscópica, a remoção transnasal da lâmina papirácea tem produzido uma redução na proptose comparável aos resultados dos outros acessos, com vantagens. Foi descrita por Kennedy et al.10 e Michel et al.4. Ela proporciona uma excelente visualização sem incisões externas, com menor morbidade e abordagem para a neuropatia óptica mais eficaz.
O objetivo desse trabalho é descrever a técnica cirúrgica enfocando suas vantagens e desvantagens.
Pré-operatórioFundamentalmente, além dos exames de rotina para qualquer cirurgia, a avaliação endoscópica e radiológica é fundamental. Através do exame endoscópico, alterações como desvios septais e presença de infecções podem ser detectadas, tratadas clinicamente ou no mesmo tempo cirúrgico. O corte coronal da tomografia computadorizada é útil para avaliar o grau de pneumatização do etmóide, a integridade e inclinação do teto etmóide, bem como a parede medial orbitária (é importante acessar a altura do etmóide posterior e sua relação com o teto do seio maxilar e determinar se o etmóide posterior pneumatiza posterior e superiormente envolvendo o nervo óptico, e ou, a artéria carótida interna), a espessura do assoalho orbitário (quanto mais espesso, mais difícil removê-lo endoscopicamente pela antrostomia meatal média), a posição da base do crânio. O corte axial é útil para demonstrar a relação entre artéria etmoidal posterior, nervo óptico e ápice orbitário. Ambos os cortes mostram a hipertrofia da musculatura extrínseca do olho (Figura 1a e 1b).
TÉCNICA CIRÚRGICAO paciente, sob anestesia geral, é posicionado inicialmente em decúbito dorsal, com cabeça ligeiramente elevada a 30º. É realizada a infiltração da parede lateral com colocação de cotonóides com vasoconstrictor em fossas nasais. Em caso de desvio septal realizamos a correção septal previamente. A descompressão orbitária (DO) inicia-se na uncifectomia, com etmoidectomia completa11. Realiza-se a meatotomia média de forma mais alargada possível, para visualização do assoalho da órbita, até o nível da parede posterior do maxilar, suficientemente para acomodar o conteúdo orbitário e prevenir sinusite maxilar obstrutiva. Utiliza-se o endoscópio de 45º para visualizar o nervo infraorbitário no seu canal, ao longo do teto do seio maxilar, pois ele representa o limite lateral para remoção óssea. Em seguida, faz-se uma esfenoidectomia transetmoidal, e anteriormente, a abertura do recesso frontal. Atenção especial deve ser dada à presença da célula de Onodi, onde o óptico pode estar saliente. O limite anterior corresponde até o processo frontal da maxila, juntamente ao duto nasolacrimal. O limite superior corresponde ao assoalho da fossa craniana anterior, onde as artérias etmoidais correspondem a um reparo anatômico importante. Inferiormente, a inserção da concha inferior é o limite. A concha media pode ser removida para otimizar o prolapso do conteúdo intraorbitário. A lâmina papirácea é então esqueletizada e removida com o elevador de periósteo, que facilmente a separa da periórbita (Figura 2).
A lâmina é cuidadosamente removida para evitar lacerações da periórbita, onde podem ocorrer herniações de gordura que podem obscurecer e prejudicar a esqueletização da periórbita. Disseca-se até o feixe etmoidal posterior, junto ao nervo óptico, quando o osso torna-se mais espesso. Nesta topografia encontra-se o ânulo de Zinn, onde se insere a musculatura extra-ocular, e centralmente a passagem ao óptico. Com o endoscópico de 45º realiza-se a remoção do assoalho orbitário até o nível do feixe vásculo-nervoso infra-orbital, nosso limite lateral da dissecção. Segue-se a dissecção tão posterior possível.
Uma vez que a periórbita esteja plenamente dissecada e exposta, realiza-se a incisão para permitir um prolapso livre da gordura da periórbita. Duas a quatro incisões na periórbita são realizadas longitudinalmente póstero-anteriormente e ínfero-superiormente. Esta seqüência minimiza a propensão de a gordura herniada obscurecer a visão do cirurgião. Deve-se ter cuidado para evitar que a foice de uncifectomia seja superficial e não adentre no conteúdo intraorbitário. Ao final do procedimento há uma extrusão da gordura e do conteúdo orbitário (Figura 3). Caso necessário, pode-se realizar a descompressão orbitária lateral neste momento, pois devido à descompressão medial haverá facilidade para a exposição da parede óssea lateral. Não há necessidade de tamponamento nasal. O paciente terá alta no dia seguinte ao procedimento, com antibioticoterapia via oral (amoxicilina por 10 dias) e soro fisiológico nasal.
DISCUSSÃOO advento da cirurgia endoscópica potencializou a possibilidade de o otorrinolaringologista atuar em campos outrora mais difíceis como a dacriocistorrinostomia, a descompressão orbitária, a descompressão do nervo óptico, de maneira segura e minimamente invasiva. A técnica foi inicialmente descrita por Kennedy et al. no início da década de 9010. A via endoscópica possibilita uma excelente visualização para uma remoção segura da estruturas da parede orbitária medial e inferior, particularmente nas regiões do teto etmoidal e ápice orbitário. A descompressão orbitária por via endoscópica utiliza uma ampla meatotomia média para uma boa visualização e acesso ao assoalho orbitário.
Em relação à via transantral, a descompressão orbitária via endoscópica não ocasiona hipoestesia por lesão ao infra-orbitário, e causa menor incidência de hipoglobo, possibilitando um período de hospitalização menor que o procedimento tradicional de Walsh-Ogura7. Permite ainda uma descompressão mais efetiva do ápice orbitário, especialmente indicada nos casos de neuropatia orbitária.
O passo mais difícil da cirurgia é a remoção da porção medial do assoalho orbitário, medialmente ao infra-orbitário, devido à espessura acentuada que pode estar presente no assoalho, mas que pode ser visualizada previamente pela tomografia computadorizada. Ressecções ósseas lateralmente ao infraorbitário promovem pouca redução da proptose, enquanto aumentam a incidência de hipoglobo e diplopia. Michel et al.4 descrevem ainda a remoção rotineira da concha média bilateralmente durante a descompressão, objetivando aumentar a área para extrusão do conteúdo orbitário.
Através da via endoscópica tem se conseguido uma retração da proptose variável, entre 3,2 a 4,7 milímetros, conforme podemos observar na tabela14,10,12,13. Entretanto, maiores reduções podem ser atingidas se associados a procedimentos por via externa como remoção da parede orbitária lateral.
Entre as desvantagens estão a maior incidência de diplopia, que poder ser corrigida posteriormente, e o potencial desenvolvimento de sinusite ou mucocele secundária14-18.
As complicações mais freqüentemente relatadas com o procedimento são a sinusite ou mucocele maxilar ou frontal, fístulas nasoliquóricas, lesão do duto nasolacrimal e o estrabismo e diplopia, que pode ocorrer em 15 a 60% dos casos. Esta última pode ter resolução espontânea em até três a quatro semanas, mas também pode ter seu surgimento tardiamente, pela evolução da doença. Nestes casos há necessidade de cirurgias para correção do estrabismo.
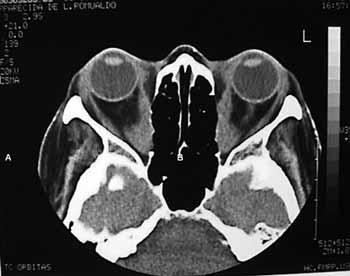
Figura 1a. Cortes tomográficos axiais (A) de paciente com oftalmopatia de Graves evidenciando hipertrofia da musculatura extrínseca ocular.
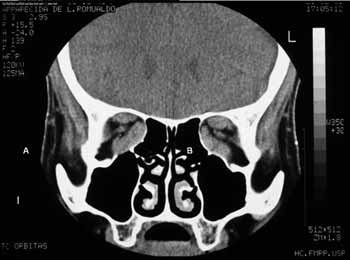
Figura 1b. Cortes tomográficos coronal (B) de paciente com oftalmopatia de Graves evidenciando hipertrofia da musculatura extrínseca ocular.
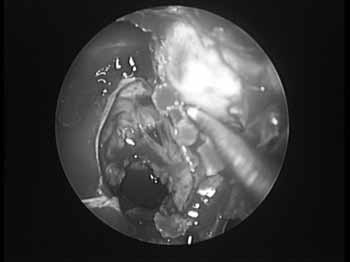
Figura 2. Remoção da lâmina papirácea em descompressão orbitária à esquerda.

Figura 3. Extrusão do conteúdo orbitário após descompressão endoscópica de órbita esquerda.

Outrora realizada por técnicas de acesso externo, atualmente a descompressão orbitária pode ser realizada por procedimento minimamente invasivo, via endoscópica, permitindo a remoção da parede ínfero-medial sem incisões externas. É um procedimento seguro para o tratamento da orbitopatia tireoideana, com menor morbidade, evitando lesões ao duto nasolacrimal, nasofrontal, ou ao infraorbital, possibilitando redução da proptose entre 3 a 4mm. Esta técnica permite uma descompressão máxima do ápice orbitário nos casos de neuropatia óptica. Entretanto, é necessário que seja realizada por cirurgião endoscópico habilitado, para obter bons resultados e evitar complicações.
REFERÊNCIAS BIBLIOGRÁFICAS1. Weetman AP. Thyroid-associated eye disease: Pathophysiology. Lancet 1991; 338: 25-8.
2. Mc Cord Jr CD. Current trends in orbital decompression. Ophthalmology 1985; 92: 21-33.
3. Naffizer HC. Progressive exophathalmos following thyroidectomy: Its pathology and treatment. Ann Surg 1931; 94: 582-6.
4. Michel O. Endoskopish kontrolierte endonasale orbitadekompression beim malignen ophtalmus. Laryngorhinootologie 1991; 70: 656-62.
5. Shorr N, Baylis HI. Ocular motility problems after orbital decompression for disthyroid ophthalmopathy. Ophthalmology 1982; 89: 323-8.
6. Mc Cord Jr CD. Orbital decompression for Graves disease: Exposure through lateral canthal and inferior fornix incision. Ophthalmology 1981; 88: 533-6.
7. Walsh TE, Ogura JH. Transantral orbital decompression for malignant exophtalmos. Laryngoscope 1957; 67: 544-68.
8. Hirsch O. Surgical decompression of exophthalmos. Arch Otolaryngol Head Neck Surg 1950; 51: 325-31.
9. Sewall EC. Operative control of progressive exophthalmos. Arch Otolaryngol Head Neck Surg 1936; 24: 621-4.
10. Kennedy DW, Goodstein MZ, Miller NR, Zinreich SJ. Endoscopic transnasal orbital decompression. Arch Otolaryngol Head Neck Surg 1990; 116: 275-82.
11. Kennedy DW. Functional endoscopic sinus surgery technique. Arch Otolaryngol Head Neck Surg 1985; 111: 643-9.
12. Lund VJ, Adams G. Orbital decompression for thyroid eye disease: a comparison of external and endoscopic techniques. J Laryngol Otol 1997; 111: 1051-5.
13. Metson R, Shore JW. Endoscopic orbital decompression. Laryngoscope 1994; 104: 950-7.
14. Henrich DH, Kennedy DW. Endoscopic orbital decompression - Graves disease. In: Stankiewcz JA. Advanced Endocopic Sinnus Surgery. St Louis: Mosby; 1995. p. 103-13.
15. Sacks EH, Anand VK, Lisman RD. Orbital decompression: Endoscopic perspective. In: Anand VK, Panje ER. Practical Endoscopic Sinnus Surgery. New York: Mc Graw-Hill; 1993. p. 138-59.
16. Hwang PH, Kennedy DW. Endoscopic transnasal orbital decompression. In: Stamm Ac & Draf W. Micro-Endoscopic Surgery of the Paranasal Sinuses And the Skull Base Springer Berlin; 2000. p. 433-9.
17. Luxenberger W, Stammberger H, Jebeles JA, Walch C. Endoscopic optic nerve decompression: The Graz experience. The Laryngoscope 1998; 108: 873-82.
18. De Santo LW. The total rehabilitation of Graves ophthalmopathy. Laryngoscope 1980; 90: 1652-78.
1Professora Associada.
2Médico Residente do Hospital das Clínicas do Departamento de Oftalmologia, Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da FMRP-USP.
3Médico Assistente do Hospital das Clínicas do Departamento de Oftalmologia, Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da FMRP-USP.
4Médico Assistente do Hospital das Clínicas do Departamento de Oftalmologia, Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da FMRP-USP.
Endereço para correspondência: Profa. Dra. Wilma T. Anselmo-Lima - Departamento de Oftalmologia e Otorrinolaringologia e Cirurgia de Cabeça e Pescoço do HCFMRP-USP, Avenida Bandeirantes 3900 Ribeirão Preto SP 14049-900.
Tel. (0xx16) 602-2862 - Fax: (0xx16) 602-2860.
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da RBORL em 8 de setembro de 2005.
Artigo aceito em 8 de setembro de 2005.


