IntroduçãoO primeiro relato de redução da saliva com a utilização da toxina botulínica foi em gatos por Dickson e Shevry em 1923¹. A utilização da toxina botulínica nas glândulas salivares, in vivo, foi relatada primeiramente em pacientes com Esclerose lateral amiotrófica (ELA) para bloquear a ação nas fibras autonômicas colinérgicas¹.
Em muitas doenças neurológicas, a estase de saliva na cavidade oral e na orofaringe e/ou o escape extra-oral de saliva indicam uma falha neurogênica na coordenação dos músculos da língua, palato e face que atuam na primeira fase da deglutição.
Em torno de 50% dos pacientes com ELA vão apresentar distúrbios importantes do controle da saliva². Além disso, muitas outras centenas de pacientes com doenças neurológicas cursam com esta alteração. Estas queixas colaboram para o estigma social da doença, com a dificuldade de integração social, acentuando os quadros de depressão e de dificuldade de reabilitação.
Entre as opções de tratamento estão a utilização de drogas com efeitos anti-colinérgicos, drogas anti-parkinsonianas, tratamento cirúrgico dos ductos ou glândulas salivares, radioterapia nas glândulas salivares e, mais recentemente, a aplicação de toxina botulínica tipo A (Botox®) nas glândulas salivares. Muitos pacientes apresentam intolerância aos efeitos adversos das drogas utilizadas, ou apresentam condições clínicas muito avançadas e graves da doença neurológica para que sejam submetidos ao tratamento cirúrgico, sendo o Botox® a melhor alternativa de tratamento da sialorréia. No entanto, na literatura, as amostras populacionais são pequenas e heterogêneas, as doses, o local e a técnica de aplicação são variáveis.
ObjetivoDemonstrar os resultados da aplicação do Botox®, num estudo prospectivo, num grupo populacional homogêneo, com doses e técnica de aplicação padronizadas, com finalidade de reduzir a saliva e os sintomas decorrentes da inabilidade de controlá-la, bem como as repercussões na qualidade de vida.
Material e MétodoNo período de dezembro de 2002 a dezembro de 2004, cinco pacientes com ELA com diagnóstico há 2,8 anos foram selecionados consecutivamente na clínica de Otorrinolaringologia da AACD (Associação de Assistência à Criança Deficiente) para aplicação de Botox® nas glândulas salivares. O seguimento foi feito no 10º dia da aplicação (primeira avaliação), e avaliações subseqüentes mensais por doze meses. Os critérios utilizados para inclusão foram:
1. Diagnóstico de ELA há pelo menos 2 anos;
2. Manifestações clínicas sugestivas de sialorréia: acúmulo de saliva na cavidade oral com contínua necessidade de eliminação, escape oral de saliva, dificuldade na fala agravada pelo acúmulo de saliva na cavidade oral e faringe.
3. Intolerância à utilização de drogas anti-colinérgicas
4. Não utilização de toxina botulínica em outros sítios nos últimos seis meses;
5. Tratamento dentário e periodontal prévio à aplicação de Botox.
O questionário de resultados e qualidade de vida foi realizado no dia da aplicação (pré-aplicação) e em cada consulta subseqüente (pós-aplicação) e as respostas foram dadas em três categorias (nunca, ocasionalmente ou freqüentemente). As quatro perguntas realizadas foram: necessidade de eliminar a saliva da boca, participação no grupo familiar no momento das refeições, constrangimento em ambientes públicos por causa da sialorréia; cumprimento por contato físico na face por familiares e amigos íntimos. Foi considerado sucesso no tratamento da aplicação e na qualidade de vida quando no mínimo três das respostas do período pré-aplicação fossem alteradas "freqüentemente" para "nunca" no período de pós-aplicação.
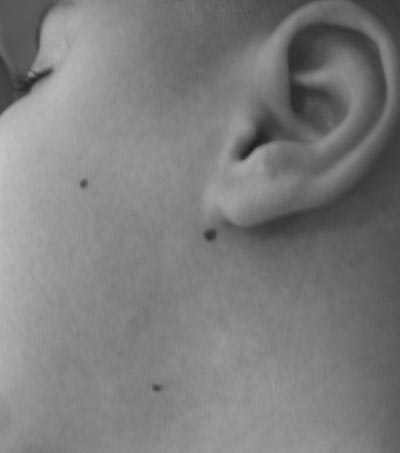
Figura 1. Aplicação de toxina botulínica em glândulas salivares - Pontos de aplicação em glândula parótida (dois pontos) e submandibulares (um ponto).
Foi realizada a anestesia tópica com prilocaína na região da glândula parotídea (PT) e submandibular (SM) trinta minutos antes da aplicação. A aplicação de Botox® na região PT foi feita em dois pontos: 10U no ângulo entre o ramo posterior da mandíbula e o processo mastóideo e 10U no ângulo entre o processo zigomático e o processo ascendente da mandíbula. Na SM, a aplicação foi feita guiada por ultra-sonografia (USG), e foram injetadas 30U em cada glândula, em um ponto central.
ResultadosNo período de dezembro de 2002 a dezembro de 2004, cinco pacientes consecutivos com ELA, com idade entre 45 e 59 anos, sendo três do gênero feminino e dois masculino, foram submetidos à aplicação de Botox® para redução da saliva. O seguimento foi de doze meses. Quatro dos cinco pacientes experimentaram significativa melhora dos sintomas e da qualidade de vida, de acordo com nossos critérios de sucesso, manifestando o desejo de reaplicação. Em um deles não houve redução da saliva, sendo este paciente que apresentava as alterações mais graves da doença, com completa imobilidade dos músculos da cavidade oral e orofaringe. Não houve efeitos colaterais sistêmicos ou locais. Em três pacientes, a melhora prolongou-se até o quarto mês, e em um paciente, a ação do Botox® não se fazia presente a partir do terceiro mês da aplicação.
DISCUSSÃOIndivíduos saudáveis secretam de 1000 a 1500ml de saliva em 24 horas³. Muitas doenças neurológicas evoluem com dificuldades no controle motor oral. Quando a produção de saliva excede a habilidade do indivíduo de transportá-la da boca até o estômago, a estase, o escape extra-oral e a aspiração podem ocorrer, além de concomitante dificuldade na mastigação e articulação. É estigmatizante, e a prevalência em muitas doenças neurológicas é elevada. A sialorréia ocorre em torno de 50% dos pacientes com ELA, e 20% são vítimas de necessidade contínua eliminação da saliva², tem prevalência em torno de 70% na doença de Parkinson4, e entre 10 a 80% dos pacientes com Paralisia Cerebral5. A prevalência da sialorréia nestas afecções é elevada com comprometimento da integração social, com importantes dificuldades na realização das atividades motoras orais durante a alimentação e a fala, com repercussões na qualidade de vida6. Nós selecionamos cinco pacientes com diagnóstico de ELA há pelo menos dois anos.
Entre as opções de tratamento para a sialorréia, as drogas anti-colinérgicas são as mais amplamente utilizadas para reduzir a saliva, no entanto podem ter efeitos colaterais sistêmicos (retenção urinária, perda da acomodação visual, cefaléia, olho seco), além do desenvolvimento de tolerância à droga¹.
Outra opção mais recente é a utilização de Botox® nas glândulas PT e SM, apesar de a toxina botulínica ter duração de ação limitada, sendo até desaconselhada por alguns no tratamento de doenças crônicas por exigir a reaplicação³. Na nossa opinião, trata-se de procedimento pouco invasivo, com discretos ou nulos efeitos colaterais locais ou sistêmicos, constituindo uma ótima alternativa de tratamento.
Encontramos na literatura uma diversidade de aspectos em relação à técnica, dose, número de pontos de aplicação nas glândulas, seleção de glândulas salivares a serem tratadas, critérios de respostas ao tratamento, e efeitos colaterais. Pelo número limitado de trabalhos que esclareçam objetivamente todos estes aspectos, gostaríamos de salientar a importância de se estabelecer um protocolo de tratamento, com padronização da técnica e dose da toxina botulínica aplicada, e realização de estudos objetivos quantitativos e qualitativos da secreção de saliva. A ação da toxina botulínica nas glândulas salivares se faz na inibição da captação da acetil-colina na junção neuroglandular, no entanto, diferentemente da ação neuromuscular, outros estímulos autonômicos são responsáveis pela secreção de saliva7.
Na revisão realizada, as glândulas selecionadas para serem submetidas à aplicação de Botox® foram as PT isoladamente³ ou as SM5, a combinação de aplicação nos dois grupos PT e SM no mesmo momento7, ou ainda, a aplicação nas PT e caso não houvesse o efeito desejado em duas semanas, a reaplicação feita nas PT e SM8. Como as PT e SM são responsáveis por 80-90% da secreção salivar em repouso, nós decidimos incluir os dois grupos no mesmo momento da aplicação, acreditando numa maior redução da saliva, e melhores resultados.
Nos primeiros relatos não havia descrição da utilização da ultra-sonografia para guiar a aplicação. Estudos mais recentes relatam a dificuldade da identificação da glândula SM com a palpação, especialmente em crianças, e relataram que a acurácia do método poderia ser aumentada quando se tem a visão direta da agulha sob controle ultra-sonográfico. Outros autores propõem que a punção seja guiada por USG nas PT e SM². Alguns autores preconizam a administração na PT em um ponto1,6, dois pontos7 ou três pontos8. Jongerius et al.. (2004) demonstraram radiologicamente que a melhor distribuição da substância na SM se dá com a aplicação em dois pontos.
A dose injetada na PT variou na literatura de 5U6 a 72U² de Botox®, e na SM variou de 5U² a 50U5. Nós estabelecemos a dose de 20U na PT (distribuídas em dois pontos) e 30U na SM (em um ponto).
Aplicamos anestesia tópica 30 minutos antes da aplicação. Os autores que relatam aplicação sob anestesia geral são Jongerius et al. (2004), pois fizeram o estudo em crianças com a aplicação em dois pontos na glândula SM, com controle USG, e provavelmente a acurácia poderia ser prejudicada pela não colaboração da criança.
Outro ponto muito controverso é o relato de sucesso que é descrito em todos os trabalhos, surpreendentemente com doses e técnicas tão diversas. Isto pode ser justificado pela subjetividade dos controles pré e pós-aplicação. Na maioria dos estudos, o índice de sucesso é dado pela resposta subjetiva do paciente ao controle da sialorréia, em outros pela medida do peso de algodão seco colocado na cavidade oral antes e depois da aplicação³ e o critério mais objetivo que observamos foi descrito analisou os resultados com a aplicação de um questionário de qualidade de vida e cintilografia das glândulas salivares². Nosso critério de melhora foi subjetivo com um questionário de quatro perguntas respondidas pelo paciente, que demonstrava a redução do escape extra-oral de saliva e a sua reintegração social, permitindo-nos inferir a redução da secreção salivar e a melhora da qualidade de vida. Quatro dos cinco pacientes tiveram sucesso com o procedimento. No final do período de acompanhamento, os quatro pacientes manifestaram desejo de repetição da aplicação, situação que reflete também o sucesso do procedimento. O tempo mínimo de ação do Botox® com respostas clínicas foi de três meses. O paciente que não demonstrou sucesso no tratamento apresentava-se em condições bastante avançadas da doença de base, o que foi relatado também por outros autores². Todos os autores relatam sucesso com a aplicação de Botox® em glândulas salivares na maioria dos pacientes estudados.
Não observamos aumento na incidência de problemas odontológicos com a redução da saliva, apesar do tempo de seguimento de 12 meses, embora tenhamos enfatizado a importância de rigorosa higiene dentária, e o tratamento odontológico prévio à aplicação, pois a saliva torna-se mais espessa. Alguns autores referem que a redução do fluxo salivar poderia causar aumento da incidência de cáries dentárias8. Entre os efeitos adversos potenciais estão a xerostomia e a piora da disfagia por difusão da droga para os músculos da mastigação. Nós não observamos efeitos adversos nos nossos pacientes.
CONCLUSÃOA aplicação de 20U de Botox® em glândulas parótidas e 30U em glândulas submandibulares, com a técnica preconizada neste estudo, foram suficientes para reduzir a saliva em pacientes e melhorar a qualidade de vida de pacientes com ELA, constituindo uma alternativa ao tratamento da sialorréia.
REFERÊNCIAS BIBLIOGRÁFICAS1. Bushara KO. Sialorrhea in amyotrophic lateral sclerosis: a hypothesis of a new treatment - botulinum toxin A injections of the parotid glands. Medical Hypothesis 1997; 48: 337-9.
2. Gies R, Naumann M, Werner E, Riemann M, Beck I, Puls I, Reiners C, Toyka KV. Injections of botulinum toxin A into salivary glands improve sialorrhoea in amyothrophic lateral sclerosis. J Neurol Neurossurg Psychiatry 2000; 69: 121-3.
3. Pal PK, Calne DB, Calne RN, Tsui JKC. Botulinum toxin A as treatment for drooling saliva en PD. Neurology 2000; 54: 244-7.
4. Mancini F, Zangaglia R, Cristina S, Sommaruga MG, Martignoni E, Pachetti C. Double-blind placebo-controlled study to evaluate the efficacy and safety of botulinum toxin type A in the treatment of drooling in parkinsonism. Mov Disord 2003; 18 (6): 685-8.
5. Jongerius PH, Rotteveel JJ, Van Limbeek J, Gabreels FJM, Van Hulst KBS, Van den Hoogen FJA. Botulinum toxin effect on salivary flow rate in children with cerebral palsy. Neurology 2004; 63: 1371-5.
6. Bothwell JE, Clarke K, Dooley JM, Gordon KE , Anderson R, Wood Camfield CS, Camfield PR. Botulinum toxin A as a treatment for excessive drooling in children. Pediatr Neurol 2002; 27(1): 18-22.
7. Suskind DL, Tilton A. Clinical Study of Botulinum - A Toxin in the Treatment of Sialorrhea in Children with Cerebral Palsy. Laryngoscope 2002; 112 (1): 73-81.
8. Maik E, Laskawi R, Rohrbach-Volland S, Christian A, Wolfgang B. Botulinum Toxin to Reduce Saliva Flow: Selected Indications for Ultrasound-Guided Toxin Application Into Salivary Glands. Laryngoscope 2002; 112(1): 82-6.
1 Doutora em Medicina, Professora do Depto. de ORL da UNIFESP.
AACD - Associação de Assistência à Criança Deficiente.
Endereço para correspondência: Dayse Manrique - Rua Canário 1112 ap. 61 São Paulo SP 04521-005.
Tel. (0xx11) 5542-0645 - (0xx11) 5549-4630 - (0xx11) 9126-0325.
Artigo recebido em 02 de maio de 2005. Artigo aceito em 23 de junho de 2005.


