Ano: 2013 Vol. 79 Ed. 4 - Julho - Agosto - (17º)
Seção: Artigo Original
Páginas: 494 a 499
Definição de valores de corte para medida de PTH intraoperatório no tratamento cirúrgico do hiperparatiroidismo secundário e terciário
Intraoperative PTH cutoff definition to predict successful parathyroidectomy in secondary and tertiary hyperparathyroidism
Autor(es): Monique Nakayama Ohe1; Rodrigo Oliveira Santos2; Ilda Sizue Kunii3; Aluizio Barbosa Carvalho4; Márcio Abrahão5; Murilo Catafesta das Neves6; Marise Lazaretti-Castro7; Onivaldo Cervantes8; Jose Gilberto Henriques Vieira9
DOI: 10.5935/1808-8694.20130088
Palavras-chave: hiperparatireoidismo; hiperparatireoidismo secundário; hormônio paratireóideo; paratireoidectomia.
Keywords: hyperparathyroidism; hyperparathyroidism, secondary; parathyroid hormone; parathyroidectomy.
Resumo:
Avaliamos medida de PTH intraoperatório (IO-PTH) no intuito de melhorar índices de sucesso no tratamento cirúrgico do hiperparatiroidismo associado à doença renal.
MÉTODO: Oitenta e seis pacientes realizaram paratiroidectomia total com autoimplante em musculatura pré-esternal entre abril de 2000 e outubro de 2009 com 26,5 meses de seguimento em média, prospectivo. Foram divididos em dois grupos: hiperparatiroidismo secundário (HPS) - pacientes em diálise e hiperparatiroidismo terciário (HPT) - transplantados renais. Medido IO-PTH (Elecsys-PTH-Immunoassay/Roche) na indução anestésica (IOPTH-0') e 20 minutos (IOPTH-20') após a retirada das paratireoides.
RESULTADOS: 80,2% (69/86) do total de pacientes apresentaram queda de 80% ou mais do IOPTH-20' e todos se curaram. Em 11/86 (12,7%) pacientes, foi observada queda entre 70-79%, sendo que dois (18,1%) deles evoluíram com falha cirúrgica. 6/86 (6,9%) pacientes apresentaram redução de IOPTH-20' menor do que 70%: dois foram curados; três apresentaram paratireoide supranumerária/ectópica que foi localizada e removida; um paciente evoluiu com persistência da doença após término da cirurgia com a retirada de quatro paratireoides.
CONCLUSÃO: Queda do IOPTH-20' de 80% ou mais foi preditor de cura em todos os pacientes renais durante o período avaliado. Redução menor que 70% sugere paratireoide hiperfuncionante não reconhecida/supranumerária, sendo preditor de falha cirúrgica em 66.6%. A queda marginal de 70%-79% delega ao cirurgião experiente a decisão de continuar ou não o procedimento cirúrgico.
Abstract:
In order to improve success rates in surgery of renal hyperparathyroidism, we evaluated intraoperative PTH (IOPTH) measurement utility.
METHOD: 86 patients underwent total parathyroidectomy with intramuscular presternal autotransplantation from 04/2000 to 10/2009 and were followed for 26.5 months on average (prospective cohort). Patients were divided in secondary (SHPT) and tertiary hyperparathyroidism (THPT). SHPT group was composed by patients under dialysis treatment, THPT group included renal grafted ones. IOPTH (Elecsys-PTH-Immunoassay/Roche) was measured at anesthesia induction (IOPTH-0') and 20 minutes (IOPTH-20') after parathyroidectomy.
RESULTS: 80.2% (69/86) presented with 80% decrease or more in the IOPTH-20' and all were cured. In 11/86 patients (12.7%), a lower IOPTH-20' drop (70-79%) was observed, and 2 of them (18.1%) failed to cure. 6/86 (6.9%) patients presented IO-PTH-20' decrease of less than 70%: two were cured, in three a supernumerary/ectopic parathyroid was found and removed, and in one of these six patients, surgery was finished after 4-gland excision and the patient failure to cure.
CONCLUSION: IOPTH-20' decrease of 80% or more compared to IOPTH-0' predicts cure in all renal patients throughout follow-up. A decay of less than 70% points to missed or hyperfunctioning supernumerary gland and is predictive of surgical failure in 66.6%. A marginal IOPTH drop of 70-79% leaves the decision whether or not surgery should be continued up to the experienced surgeon.
![]()
INTRODUÇÃO
Hiperparatireoidismos secundário e terciário resultam de hiperplasia da glândula paratireoide e excessiva secreção de hormônio paratireoidiano (PTH)1. Apesar dos recentes avanços na terapêutica médica, a excisão cirúrgica da paratireoide pode ser necessária em um número considerável de doentes renais2. A melhor abordagem cirúrgica para hiperparatiroidismo renal ainda está em discussão e ainda há muita polêmica com relação à melhor opção terapêutica, uma vez que a recidiva pós-cirúrgica ou o risco de hipoparatireoidismo definitivo devem ser evitados. Paratireoidectomia total com autotransplante de tecido da paratireóide é uma técnica bem aceita para o tratamento destes pacientes3-6. O procedimento cirúrgico envolve a exploração cervical bilateral, buscando a remoção total do tecido da paratireoide anormal. Persistência e/ou recidiva indicam ressecção inadequada de tecido hiperfuncionante. A reoperação pode ser necessária para hiperparatiroidismo renal recorrente em cerca de 15% dos casos, principalmente devido à presença de glândulas supranumerárias, paratireoidectomia inicial inadequada, ou hiperplasia contínua de tecido remanescente7-8.
Desde o seu início, o monitoramento intraoperatório do PTH (PTH-IO) tem sido realizado em pacientes com hiperparatiroidismo primário em vários centros médicos, tornando-se um reconhecido preditor de sucesso cirúrgico nestes pacientes9-13. Por meio de medidas de PTH-IO, o cirurgião pode confirmar a remoção total das glândulas paratireoides anormais, evitando deixar ficarem glândulas restantes hiperfuncionantes ou supranumerárias. No entanto, diferentemente de pacientes com hiperparatiroidismo primário, o papel do monitoramento do PTH-IO no tratamento cirúrgico do hiperparatiroidismo renal é menos estabelecido14. Não existe uma definição padrão de queda no PTH-IO no tratamento cirúrgico do hiperparatiroidismo renal, uma vez que a função renal e a depuração renal tardia de PTH podem interferir no monitoramento do PTH-IO. Além disso, há poucas grandes casuísticas publicadas usando-se o monitoramento de PTH-IO em pacientes renais14.
O objetivo do presente estudo foi avaliar a utilidade da monitorização intraoperatória de PTH em pacientes sob diálise ou transplantados renais com hiperparatireoidismos secundário e terciário. Nosso objetivo foi definir um valor de corte de PTH-IO, a fim de evitar que fiquem glândulas paratireoides remanescentes ou supranumerárias, assim melhorando as taxas de sucesso cirúrgico.
MÉTODO
Tipo de estudo
Este é um estudo prospectivo da coorte em um grupo de pacientes operados em um centro universitário de referência. Todas as cirurgias foram realizadas pelo mesmo cirurgião. Este estudo foi aprovado pelo Comitê de Ética da instituição (aprovação nº CEP 886/00) e os pacientes deram seu consentimento informado antes de sua inclusão no estudo.
Pacientes
Oitenta e seis pacientes renais submetidos a paratireoidectomia total com autotransplante intramuscular pré-external6 entre abril de 2000 a outubro de 2009 em São Paulo, Brasil. Os pacientes foram acompanhados em nossa instituição e encaminhados para tratamento cirúrgico devido a: hipercalcemia persistente não responsiva a intervenções clínicas e/ou hiperfosfatemia persistente apesar do uso contínuo de restrição dietética de fósforo e de quelantes de fosfato; e sintomas como, dor óssea intensa, prurido intratável, fraturas ou alto risco de fraturas, deformidades esqueléticas, calcificações extraesqueléticas, desenvolvimento de calcifilaxia e evidências radiográficas de osteodistrofia renal.
Eles foram divididos em grupos com hiperparatireoidismo secundário e terciário. O hiperparatireoidismo secundário é caracterizado como um distúrbio adquirido associado à doença renal em estágio terminal, em que o estado urêmico apresenta um estímulo contínuo para as glândulas paratireoides. Foram incluídos no grupo HPTS os pacientes em tratamento por diálise que apresentaram hiperparatiroidismo grave, com níveis séricos de cálcio normais ou elevados. O grupo de hiperparatireoidismo terciário foi composto por pacientes transplantados renais com hiperplasia não suprimível da paratireoide, com o aumento persistente dos níveis de PTH e hipercalcemia mesmo após a restauração da função renal normal. A hipercalcemia após o transplante renal geralmente ocorre devido a hiperparatiroidismo que persiste desde o período anterior da doença renal crônica15.
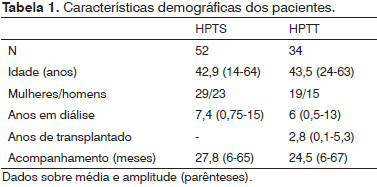
Antes da paratiroidectomia, medimos os níveis séricos de cálcio ionizado (iCa), fósforo (P), fosfatase alcalina (AP), e do hormônio paratireoide intacto (iPTH) (Tabela 1) e anualmente após a cirurgia em todos os pacientes de ambos os grupos.
A cura cirúrgica foi definida como a restauração dos níveis séricos de cálcio e iPTH como esperado para cada fase da função renal, ao longo dos primeiros 6 meses após a cirurgia15. A recidiva pós-operatória foi definida quando altos níveis de PTH foram observados no acompanhamento tardio pós-operatório (1 ano após o procedimento cirúrgico), que não responderam ao tratamento clínico-farmacológico. O hipoparatireoidismo definitivo foi descrito quando os níveis séricos de PTH estiveram inferiores a 10 pg/mL por 01 ano após a paratireoidectomia, com níveis séricos de cálcio normais ou baixos sob vitamina D e reposição oral de cálcio.
Métodos
A paratireoidectomia total com autotransplante intramuscular pré-external6 foi realizada em 86 pacientes entre abril de 2000 e outubro de 2009. Os pacientes foram avaliados durante uma média de 26,5 meses de acompanhamento (intervalo de 6-67 meses).
A avaliação intraoperatória de PTH (PTH-IO) foi realizada na tentativa de confirmar a remoção total das glândulas paratiroides, de modo a evitar deixar glândulas hiperfuncionantes remanescentes ou supranumerárias. O PTH-IO foi medido usando-se o Imunoensaio PTH Elecsys (Sistema Elecsys 1010, Roche, Mannheim, Alemanha). O tempo necessário para a realização do ensaio é de 9 minutos e os valores de referência são de 10-70 pg/mL. Uma amostra de sangue venoso periférico (4,0 mL) foi obtida imediatamente após a indução da anestesia e 20 minutos após a remoção de toda a paratireoide12-13.
O fósforo, a fosfatase alcalina total e a creatinina foram medidos por meio de ensaios automáticos padronizados (Hitachi 912, Roche). O cálcio ionizado sérico foi medido por meio de um eletrodo íon-específico (AVL 9180 Electrolyte Analyzer, Roswell, Georgia, EUA). O hormônio da paratireoide foi medido por meio de um ensaio imunométrico (Immulite, DPC, MedLab).
RESULTADOS
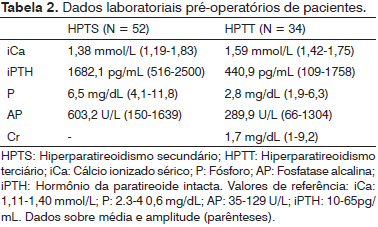
No total, 86 pacientes foram submetidos à paratireoidectomia total com autotransplante intramuscular pré-esternal com monitoramento do PTH-IO. Os pacientes foram avaliados de forma prospectiva em um seguimento médio de 26,5 meses (variando de 6 a 67 meses). Havia 52 pacientes no grupo de HPTS e 34 no grupo HPTT. Os pacientes do grupo HPTS apresentaram média de 7,4 anos em tratamento dialítico antes da paratireoidectomia e aqueles do grupo HPTT foram os pacientes que se submeteram a tratamento de diálise por uma média de 6 anos antes de receberem um transplante de rim, com média de 2,8 anos de enxerto renal funcional antes da paratireoidectomia. As características demográficas dos pacientes estão descritas na Tabela 1 e os dados bioquímicos pré-operatórios dos pacientes estão apresentadas na Tabela 2.
Quanto aos achados cirúrgicos, pelo menos 4 glândulas paratiroides foram identificadas e excisadas em todos os 86 pacientes, e glândulas supranumerárias foram encontrados em 3 (a 5ª paratireoide estava localizada na região cervical em dois pacientes e no timo em um).
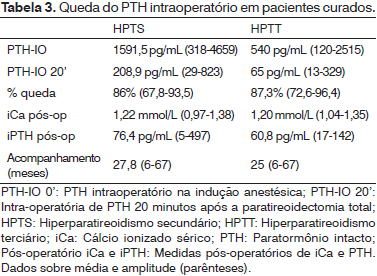
Os pacientes em tratamento por diálise, que foram curados após a cirurgia, apresentaram PTH-IO em níveis basais de 1.591,5 pg/mL, em média; e PTH-IO 20 minutos após a paratireoidectomia total de 208,9 pg/mL, em média; com 86% de redução. Entre os doentes curados com transplante renal, o valor basal do PTH-IO foi 540 pg/ml, em média; e 65 pg/ml, em média aos 20 minutos após a paratireoidectomia total, com um decréscimo médio de 87,3% (Tabela 3).
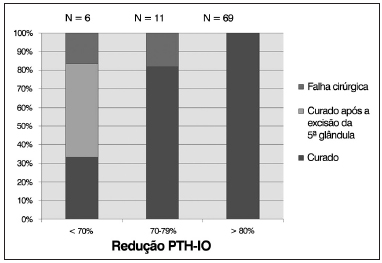
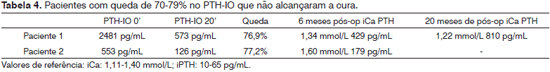
No total, 69 pacientes (80,2%) apresentaram diminuição de 80% ou mais nos níveis de PTH-IO, e todos os pacientes foram curados (Gráfico 1). Onze pacientes (12,7%) apresentaram uma redução de 70-79%, e entre eles, dois não conseguiram a cura (redução de 76,9% e 77,2% no PTH-IO) (Tabela 4, Gráfico 1). O PTH-IO impediu falha cirúrgica em 3 pacientes, nos quais a o PTH-IO apresentou queda de 58,5%, 51,8% e 62%, respectivamente; a queda no PTH-IO foi considerada insuficiente. A exploração cirúrgica foi continuada e uma glândula paratireoide cervical supranumerária foi removida em dois pacientes; e em um deles foi ressecada uma glândula paratireoide ectópica supranumerária no timo (Tabela 5, Gráfico 1). Um paciente apresentou queda de 67,4% no PTH-IO (Tabela 5, o paciente 4). Essa queda foi considerada suficiente e a cirurgia foi concluída após a excisão de quatro glândulas paratireoides. Os níveis de PTH no pós-operatório mantiveram-se elevados no início do acompanhamento pós-operatório, e o paciente não foi considerado curado (Tabela 5, paciente 4).
Hipoparatireoidismo definitivo foi observado em dois pacientes, um em cada grupo (de 2,3% entre todos os pacientes).
DISCUSSÃO
A determinação rápida intraoperatória do hormônio paratireóideo intacto tornou-se amplamente estabelecida no tratamento cirúrgico do hiperparatiroidismo primário, no qual a remoção de todo o tecido paratireóideo hiperfuncionante é confirmada por uma queda rápida em PTH circulante dentro de 5 a 10 minutos4,12-13,16-19. A queda intraoperatória de PTH circulante em pacientes renais é reproduzível, mas marcadamente mais lenta do que nos pacientes com função renal normal. Isto está em acordo com o aumento da meia-vida de iPTH na insuficiência renal (6,6 minutos, contra 2,2 minutos)20. Estudos com rápida medição intraoperatória do PTH no hiperparatireoidismo secundário demonstraram uma redução gradual no iPTH circulante, correspondente à ressecção sequencial da glândula12,21; e esses achados, juntamente com uma maior incidência de glândulas paratireoides supranumerárias/ectópicas no hiperparatiroidismo renal7,8, apontam para a medição do PTH-IO como uma ferramenta interessante, em uma tentativa de se evitar a falha cirúrgica.
Diferenças entre pacientes com HPTS e aqueles com HPTT podem ser apontadas em relação ao perfil de queda do PTH-IO: os pacientes em tratamento por diálise podem apresentar uma queda mais lenta de PTH-IO em comparação com os transplantados renais, nos quais a função renal esteja restaurada. Além disso, os pacientes com HPTT se assemelham àqueles com HPT primário, com hipercalcemia e função renal normal. No entanto, o HPTT é uma doença multiglandular (contrário à doença típica que é o hiperparatiroidismo primário uniglandular), necessitando de diferente abordagem cirúrgica, provavelmente interferindo com a análise cinética do PTH-IO. Isso, juntamente com a dificuldade de assumir função renal completamente normal anos após o transplante renal, deixa o HPTT mais parecido com HPTS do que com o hiperparatiroidismo primário. Devido ao aumento da meia-vida do iPTH em pacientes com insuficiência renal, escolhemos uma medida de PTH-IO a 20 minutos, uma medida atrasada em comparação com os 10 minutos de medição do PTH-IO estabelecidos no hiperparatiroidismo primário. Além disso, apesar de potenciais diferenças entre os pacientes com HPTS e HPTT, os dados foram estudados considerando os dois grupos em conjunto.
Já foram publicados alguns estudos com pequenas séries e/ou acompanhamento limitado avaliando a redução em percentil do PTH-IO em pacientes renais8,13,14,22. Alguns autores observaram queda de 50 a 60% no PTH-IO entre 10 a 20 minutos após a paratireoidectomia como um indicador confiável de cura pós-operatória23-25. Outros autores esperavam mais do que 80% de queda no PTH-IO 15 minutos após a paratiroidectomia, a fim de assegurar a cura cirúrgica26. A nossa experiência anterior mostrou que uma diminuição de 70% 20 minutos após a paratiroidectomia indica procedimento bem sucedido13.
Neste estudo, a queda de 80% ou mais no PTH-IO 20 minutos após a paratireoidectomia garantiu cura cirúrgica em todos os pacientes. No geral, 69 (80,2%) pacientes apresentaram PTH-IO com queda de 80% ou mais, e todos foram curados. Seis pacientes (6,9%) apresentaram menos de 70% de redução no PTH-IO e, entre eles, 4 (66,6%) apresentaram paratireoides supranumerárias/ectópicas removidas (3 deles) e um permaneceu sem cura.
Tendo em conta estes resultados, podemos concluir que 80% ou mais de redução no PTH-IO medido aos 20 minutos após a remoção total de tecido da paratireoide hipersecretora é esperado e prevê 100% de cura. Além disso, a queda de menos de 70% no PTH-IO está associada a 66,6% de insucessos cirúrgicos, a maioria dos quais associado a glândula paratireoide supranumerária/ectópica.
Preocupações especiais têm que ser levantadas no tocante à queda "marginal" do PTH-IO entre 70% a 79% - observadas em 11 pacientes (12,7%), uma vez que dois pacientes entre eles (18,1%) não foram curados. Questões específicas permanecem sem solução: como pode o cirurgião reconhecer esses pacientes? Até que ponto a cirurgia deve continuar na busca por mais glândulas hipersecretoras? Estas questões permanecem sem resposta, e cabe ao cirurgião experiente apontar quando e como concluir o procedimento cirúrgico, com base em aspectos clínicos do paciente e nos resultados cirúrgicos em andamento.
As limitações deste estudo estão relacionadas com as características heterogêneas de pacientes renais com suas particularidades clínicas e laboratoriais, e considerá-los como um grupo representa um grande desafio. Outra limitação diz respeito à gravidade dos pacientes: a relevância da condição e seu aspecto duradouro agrupam-os em uma classe especial, cujo resultado não poderia ser esperada em pacientes convencionais com doença renal crônica. Além disso, os níveis de vitamina D 25OH não estavam disponíveis.
CONCLUSÃO
A diminuição de PTH-IO de 80% ou mais a partir dos seus valores basais pré-operatórios prevê cura em todos os pacientes renais durante o acompanhamento. A queda de menos de 70% no PTH-IO acontece em casos de glândulas hiperfuncionantes que não foram retiradas ou supranumerárias, e é preditivo de falha cirúrgica em 66,6% dos casos. A queda marginal de 70-79% no PHT-IO leva à necessidade do cirurgião experiente decidir se a cirurgia deve ser continuada ou não.
REFERÊNCIAS
1. Triponez F, Clark OH, Vanrenthergem Y, Evenepoel P. Surgical treatment of persistent hyperparathyroidism after renal transplantation. Ann Surg. 2008;248(1):18-30. http://dx.doi.org/10.1097/SLA.0b013e3181728a2d
2. Malberti F, Marcelli D, Conte F, Limido A, Spotti D, Locatelli F. Parathyroidectomy in patients on renal replacement therapy: an epidemiologic study. J Am Soc Nephrol. 2001;12(6):1242-8.
3. Packman KS, Demeure MJ. Indications for parathyroidectomy and extent of treatment for patients with secondary hyperparathyroidism. Surg Clin North Am. 1995;75(3):465-82.
4. Sokoll LJ, Drew H, Udelsman R. Intraoperative parathyroid hormone analysis: A study of 200 consecutive cases. Clin Chem. 2000;46(10):1662-8.
5. Weber KJ, Misra S, Lee JK, Wilhelm SW, DeCresce R, Prinz RA. Intraoperative PTH monitoring in parathyroid hyperplasia requires stricter criteria for success. Surgery. 2004;136(6):1154-9. http://dx.doi.org/10.1016/j.surg.2004.05.060
6. Santos RO, Ohe MN, Carvalho AB, Neves MC, Kunii I, Lazaretti-Castro M, et al. Total parathyroidectomy with presternal intramuscular autotransplantation in renal patients: a prospective study of 66 patients. J Osteoporos. 2012;2012:631243.
7. Pattou FN, Pellissier LC, Noël C, Wambergue F, Huglo DG, Proye CA. Supernumerary parathyroid glands: frequency and surgical significance in treatment of renal hyperparathyroidism. World J Surg. 2000;24(11):1330-4. http://dx.doi.org/10.1007/s002680010220
8. Clary BM, Garner SC, Leight GS Jr. Intraoperative parathyroid hormone monitoring during parathyroidectomy for secondary hyperparathyroidism. Surgery. 1997;122(6):1034-8. http://dx.doi.org/10.1016/S0039-6060(97)90206-3
9. Nussbaum SR, Thompson AR, Hutcheson KA, Gaz RD, Wang CA. Intraoperative measurement of parathyroid hormone in the surgical management of hyperparathyroidism. Surgery. 1988;104(6):1121-7.
10. Westerdahl J, Lindblom P, Bergenfelz A. Measurement of intraoperative parathyroid hormone predicts long-term operative success. Arch Surg. 2002;137(2):186-90. http://dx.doi.org/10.1001/archsurg.137.2.186
11. Bergenfelz A, Isaksson A, Lindblom P, Westerdahl J, Tibblin S. Measurement of parathyroid hormone in patients with primary hyperparathyroidism undergoing first and reoperative surgery. Br J Surg. 1998;85(8):1129-32. http://dx.doi.org/10.1046/j.1365-2168.1998.00824.x
12. Ohe MN, Santos RO, Kunii IS, Carvalho AB, Abrahão M, Cervantes O, et al. Usefulness of a rapid immunometric assay for intraoperative parathyroid hormone measurements. Braz J Med Biol Res. 2003;36(6):715-21. http://dx.doi.org/10.1590/S0100-879X2003000600006
13. Ohe MN, Santos RO, Kunii IS, Abrahão M, Cervantes O, Carvalho AB, et al. Utilidade da medida de PTH intra-operatório no tratamento cirúrgico do hiperparatireoidismo primário e secundário: Análise de 109 casos. Arq Bras Endocrinol Metab. 2006;50(5):869-75. http://dx.doi.org/10.1590/S0004-27302006000500007
14. Moor JW, Roberts S, Atkin SL, England RJ. Intraoperative parathyroid hormone monitoring to determine long-term success of total parathyroidectomy for secondary hyperparathyroidism. Head Neck. 2011;33(3):293-6.
15. Kidney Disease: Improving Global Outcomes (KDIGO) CKD-MBD Work Group. KDIGO clinical practice guideline for the diagnosis, evaluation, prevention, and treatment of Chronic Kidney Disease-Mineral and Bone Disorder (CKD-MBD). Kidney Int Suppl. 2009;(113):S1-130.
16. Irvin GL 3rd, Dembrow VD, Prudhomme DL. Operative monitoring of parathyroid gland hyperfunction. Am J Surg. 1991;162(4):299-302. http://dx.doi.org/10.1016/0002-9610(91)90135-Z
17. Irvin GL 3rd, Deriso GT 3rd. A new, practical intraoperative parathyroid hormone assay. Am J Surg. 1994;168(5):466-8. http://dx.doi.org/10.1016/S0002-9610(05)80101-1
18. Boggs JE, Irvin GL 3rd, Molinari AS, Deriso GT. Intraoperative parathyroid hormone monitoring as an adjunct to parathyroidectomy. Surgery. 1996;120(6):954-8. http://dx.doi.org/10.1016/S0039-6060(96)80040-7
19. Garner SC, Leight GS Jr. Initial experience with intraoperative PTH determinations in the surgical management of 130 consecutive cases of primary hyperparathyroidism. Surgery. 1999;126(6):1132-7. http://dx.doi.org/10.1067/msy.2099.101429
20. Brossard JH, Cloutier M, Roy L, Lepage R, Gascon-Barré M, D'Amour P. Accumulation of a non-(1-84) molecular form of parathyroid hormone (PTH) detected by intact PTH assay in renal failure: importance in the interpretation of PTH values. J Clin Endocrinol Metab. 1996;81(11)3923-9. http://dx.doi.org/10.1210/jc.81.11.3923
21. Proye CA, Goropoulos A, Franz C, Carnaille B, Vix M, Quievreux JL, et al. Usefulness and limits of quick intraoperative measurements of intact (1-84) parathyroid hormone in the surgical management of hyperparathyroidism: sequential measurements in patients with multiglandular disease. Surgery. 1991;110(6):1035-42.
22. Koeberle-Wuehrer R, Haid A, Sprenger-Maehr H, Koeberle D, Meusburger E, Neyer U. Intraoperative blood sampling for parathyroid hormone measurement during total parathyroidectomy and autotransplantation in patients with renal hyperparathyroidism. Wien Klin Wochenschr. 1999;111(6):246-50.
23. Lokey J, Pattou F, Mondragon-Sanchez A, Minuto M, Mullineris B, Wambergue F, et al. Intraoperative decay profile of intact (1-84) parathyroid hormone in surgery for renal hyperparathyroidism--a consecutive series of 80 patients. Surgery. 2000;128(6):1029-34. http://dx.doi.org/10.1067/msy.2000.110431
24. Pitt SC, Panneerselvan R, Chen H, Sippel RS. Secondary and tertiary hyperparathyroidism: the utility of ioPTH monitoring. World J Surg. 2010;34(6):1343-9. http://dx.doi.org/10.1007/s00268-010-0575-4
25. Chou FF, Lee CH, Chen JB, Hsu KT, Sheen-Chen SM. Intraoperative parathyroid hormone measurement in patients with secondary hyperparathyroidism. Arch Surg. 2002;137(3):341-4. http://dx.doi.org/10.1001/archsurg.137.3.341
26. Gioviale MC, Gambino G, Maione C, Luna E, Calderone F, Di Bona A, et al. Intraoperative parathyroid hormone monitoring during parathyroidectomy for hyperparathyroidism in waiting list and kidney transplant patients. Transplant Proc. 2006;38(4):1003-5. http://dx.doi.org/10.1016/j.transproceed.2006.02.140
1. Mestrado concluído e Doutorado na Disciplina de Endocrinologia e Metabologia EPM-UNIFESP em andamento (Pós-Graduanda na Disciplina de Endocrinologia e Metabologia EPM-UNIFESP).
2. Doutor (Professor Doutor do Departamento ORL-CCP da EPM-UNIFESP Vice-chefe do Departamento ORL-CCP da EPM-UNIFESP).
3. Mestrado (Biomédica do Laboratório de Endocrinologia e Metabologia da EPM-UNIFESP).
4. Doutor em Nefrologia (Professor-afiliado da Disciplina de Nefrologia).
5. Professor Livre Docente do Departamento ORL-CCP da EPM-UNIFESP (Chefe da Disciplina de CCP EPM-UNIFESP).
6. Cirurgião de Cabeça e Pescoço (Assistente da Disciplina de CCP EPM-UNIFESP)
7. Livre Docente da Disciplina de Endocrinologia e Metabologia EPM-UNIFESP (Professor Doutor da Disciplina de Endocrinologia e Metabologia EPM-UNIFESP. Chefe do Ambulatório de Doenças Osteo-Metabólicas da Disciplina de Endocrinologia e Metabologia EPM-UNIFESP).
8. Professor Livre Docente do Departamento de Otorrinolaringologia e Cirurgia de Cabeça e Pescoço.
9. Doutorado (Professor Doutor da Disciplina de Endocrinologia e Metabologia EPM-UNIFESP).
Endereço para correspondência:
Rodrigo Oliveira Santos
Av. Conselheiro Rodrigues Alves, nº 804, apto. 51. Vila Mariana
São Paulo - SP. Brasil. CEP: 04014-002
E-mail: rodrigoorlccp@uol.com.br
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) do BJORL em 23 de janeiro de 2013. cod. 10729.
Artigo aceito em 8 de abril de 2013.