Ano: 2012 Vol. 78 Ed. 4 - Julho - Agosto - (9º)
Seção: Artigo Original
Páginas: 42 a 47
Artéria esfenopalatina: desafio cirúrgico na epistaxe
The sphenopalatine artery: a surgical challenge in epistaxis
Autor(es): Gustavo Lara Rezende1; Vitor Yamashiro Rocha Soares2; Waldete Cabral Moraes3; Carlos Augusto Costa Pires de Oliveira4; Márcio Nakanishi5
Palavras-chave: artéria maxilar, epistaxe, nariz.
Keywords: epistaxis, maxillary artery, nose.
Resumo:
O conhecimento anatomocirúrgico da artéria esfenopalatina (AEP) e de seus ramos é de fundamental importância para o sucesso no tratamento endoscópico da epistaxe posterior. Contudo, essa complexa variação anatômica da irrigação da cavidade nasal ainda é um desafio cirúrgico.
OBJETIVO: Descrever a anatomia endoscópica da AEP em cadáveres humanos.
CASUÍSTICA E MÉTODOS: Estudo de coorte histórica com corte transversal de abril de 2010 a agosto de 2011. Foi descrita a presença da crista etmoidal da lâmina perpendicular do osso palatino, a localização do forame esfenopalatino principal (FEP) e acessório (FEA) e quantificados os ramos que emergem dos forames.
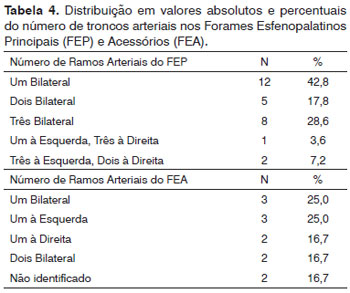
RESULTADOS: Foram analisadas 56 fossas nasais. A crista etmoidal estava presente em 96% dos casos e na maioria das vezes anterior ao FEP. O FEP se localizava na transição do meato médio para o meato superior em todos os casos. O FEA estava presente em 12 casos. Foi mais prevalente a presença de um único tronco arterial bilateral na emergência do FEP (43%). Em outros casos, observaram-se três (n = 8) e dois (n = 5) troncos arteriais, emergindo do FEP bilateralmente. Observou-se que na maioria dos casos um único tronco se emergia do FEA.
CONCLUSÕES: A anatomia da artéria esfenopalatina é bastante variável. O conhecimento das possíveis variações anatômicas implica no sucesso do tratamento da epistaxe grave.
Abstract:
Knowledge on the anatomy of the sphenopalatine artery (SPA) and its branches is fundamental for the success of the endoscopic treatment of posterior epistaxis. However, the complex anatomical variations seen in the irrigation of the nasal cavity poses a significant surgical challenge.
OBJECTIVE: This paper aims to describe the endoscopic anatomy of the SPA in human cadavers.
MATERIALS AND METHODS: This is a contemporary cross-sectional cohort study carried out between April 2010 and August 2011. The presence of the ethmoidal crest on the lamina perpendicular to the palatine bone and the location of the principal sphenopalatine foramen (PSF) and the accessory sphenopalatine foramen (ASF) were analyzed in 28 cadavers, and the branches emerging from the foramens were counted.
RESULTS: Fifty-six nasal fossae were analyzed. The ethmoidal crest was present in 96% of the cases and was located anteriorly to the PSF in most cases. The PSF was located in the transition area between the middle and the superior meatus in all cases. The ASF was seen in 12 cases. Most nasal fossae (n = 12) presented a single bilateral arterial trunk emerging from the PSF. In other cases, three (n = 8) or two (n = 5) arterial trunks emerged bilaterally from the PSF. In most cases, the SPA emerged as a single trunk from the ASP.
CONCLUSIONS: The anatomy of the SPA is highly variable. The success of the treatment for severe epistaxis relies heavily on adequate knowledge of the possible anatomical variations of the sphenopalatine artery.
![]()
INTRODUÇÃO
A principal fonte de sangue da cavidade nasal provém da artéria esfenopalatina, ramo do sistema carotídeo externo. Situada na região posterior da cavidade nasal, esta artéria é responsável pela maioria dos episódios graves de epistaxe1,2. Em um episódio de sangramento nasal grave, a falha em cauterizar ou ligar este vaso varia entre 2% a 10% dos casos3. Mesmo nas mãos de cirurgiões experientes, a complexa variação anatômica da irrigação da cavidade nasal ainda é um desafio.
O forame esfenopalatino é uma incisura na margem superior do osso palatino entre a órbita e o processo esfenopalatino. Este é transformado em forame quando o osso palatino articula-se com o osso esfenoide na parede lateral nasal. Variações quanto ao seu tamanho, formato, localização e o número de ramos que emergem do seu orifício são pouco descritas na literatura4,5. Estudos que possam prever ou definir pontos de referência da anatomia endoscópica nasal são essenciais ao tratamento cirúrgico eficaz da epistaxe.
A atual tendência é substituir o tamponamento posterior pela ligadura endoscópica da artéria esfenopalatina em casos de epistaxe posterior, reduzindo morbidades e o desconforto para o paciente6. Desta forma, o domínio técnico da cirurgia endoscópica nasal e o perfeito conhecimento da vascularização nasal são essenciais ao sucesso do tratamento. Contudo, a visualização endoscópica muda a forma de identificar essas mesmas estruturas. Isto é, não existe uma nova anatomia, o que muda é a forma com que enxergamos essa anatomia sob a ótica do endoscópio.
Este estudo tem como objetivo descrever a anatomia endoscópica da artéria esfenopalatina de cadáveres e suas possíveis variações anatômicas, e avaliar os pontos ósseos de reparo anatômico para identificação do forame esfenopalatino.
MATERIAIS E MÉTODOS
Foi realizado estudo descritivo da anatomia da artéria esfenopalatina no Serviço de Anatomia-Patológica de hospital terciário entre abril de 2010 e agosto de 2011. Entraram no estudo 28 cadáveres. O tempo entre o óbito e a coleta das amostras ocorreu entre 3 e 12 horas. As características dos cadáveres estudados, como raça, sexo, idade, hora do óbito, hora da autópsia e causa do óbito foram colhidos de acordo com o protocolo de necropsia do Serviço de Anatomia-Patológica do hospital. Foram excluídos do estudo cadáveres com trauma nasal, cirurgia nasal prévia ou doenças nasais que impediam a dissecção anatômica.
A análise da anatomia endoscópica da artéria esfenopalatina foi realizada sob videoendoscopia nasal, com uma óptica rígida de 30 graus, 4,0 mm (Karl Storz), fibra ótica e fonte de luz Komlux (250 watts), monitor de vídeo Toshiba (modelo CRT 1030) e aparelho de videoendoscopia (modelo Toshiba IK-CU44A). As imagens foram gravadas e armazenadas, utilizando um capturador de vídeo (Pinnacle Systems, Inc., Studio Movie Box HD).
Todas as dissecções foram realizadas bilateralmente, de acordo com os seguintes passos cirúrgicos endoscópicos nasais: (1) Deslocava-se medialmente a concha média e identificava-se, com uma pinça palpadora, a região de transição entre a fontanela maxilar posterior e a porção perpendicular do osso palatino; logo no início da porção penpendicular do osso palatino era realizada apenas uma incisão vertical na mucosa da parede nasal lateral de aproximadamente 1,5 cm até a porção superior da concha inferior; (2) Confeccionava-se um retalho mucoperiosteal ao longo da região posterior do nariz, da transição do meato médio com o superior até se identificar o forame esfenopalatino e os seus vasos; (3) Continuava-se a dissecção até a parede anterior do seio esfenoide para identificar outros possíveis ramos arteriais. Eram colhidas amostras do melhor segmento arterial bilateralmente, da sua emergência do forame até 1,0 cm adiante, para análise histológica e, assim, assegurar a origem arterial da estrutura visualizada.
As estruturas anatômicas foram identificadas e classificadas quanto a: (1) Presença da espinha etmoidal anterior do pilar perpendicular do osso palatino; (2) Localização e presença do forame esfenopalatino principal (FEP) e acessório (FEA). O FEP foi considerado como o maior orifício ósseo na parede nasal lateral por onde emergiam os troncos arteriais adjacentes à crista etmoidal da lâmina perpendicular do osso palatino. Já o FEA foi considerado como um orifício ósseo menor além do FEP; (3) Números de ramos arteriais saindo através dos forames identificados; e (4) Prevalência e análise de simetria (presença e localização do FEP e do FEA, e número de ramos arteriais oriundos do FEP e FEA).
A localização do forame esfenopalatino e do forame acessório foi definida com relação à inserção da concha média: a) no meato superior (MS): a abertura do FEP surge acima da inserção da concha média; b) na transição entre o meato superior e médio (MM/MS): a abertura do FEP ocorre sob a espinha etmoidal; c) no meato médio (MM): a abertura do FEP está abaixo da linha de inserção da concha média.
O estudo foi aprovado pelo Comitê de Ética local (protocolo 36/2010).
RESULTADOS
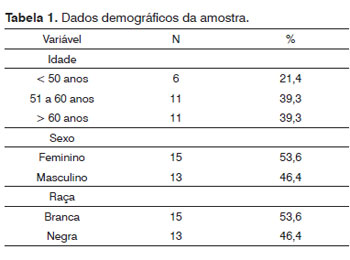
Foram analisadas 56 fossas nasais de 28 cadáveres, sendo 13 do sexo masculino e 15 do sexo feminino. A idade média foi 58,32 ± 17,17 anos, sendo o mais jovem com 11 anos e o mais velho com 91 anos. Quanto à raça, 15 eram brancos e 13 negros. (Tabela 1).
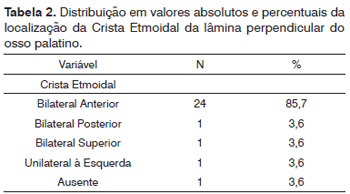
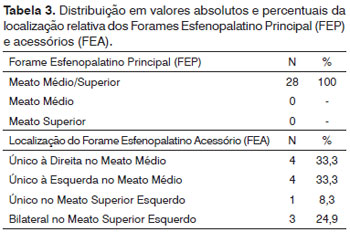
A espinha etmoidal estava presente em 96,4% dos casos (Tabela 2). Sua ausência ocorreu em apenas um dos casos analisados. Na maioria das vezes, apresentou-se bilateralmente anterior ao FEP (n = 24) e apenas uma vez posterior bilateralmente ao FEP, superior bilateralmente e unilateral à esquerda. A descrição anatômica do forame esfenopalatino (FEP) demonstrou que em todos os casos (n = 28) este se localizava na transição do meato médio para o meato superior. O forame esfenopalatino acessório estava presente em 12 casos. A sua localização se distribuiu conforme a Tabela 3.
A maioria das fossas nasais apresentava um tronco arterial único bilateral (n = 12) emergindo do FEP. Outras apresentam bilateralmente três troncos arteriais (n = 8) ou dois troncos (n = 5) (Figuras 1 e 2). Em apenas três casos ocorreram variações entre o número de ramos de cada lado analisado. Observou-se que, na maioria dos casos, um único tronco emergia do FEP acessório. Em apenas dois casos foram observados dois ramos no FEP acessório (Tabela 4).
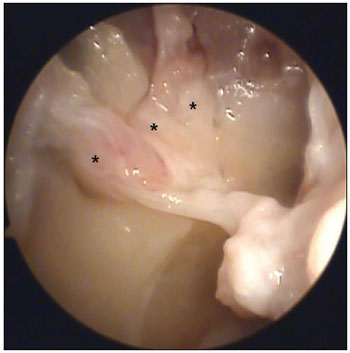
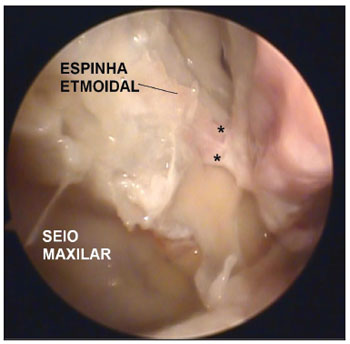
Figura 1. Fotografia da fossa nasal direita exibindo três ramos arteriais (*) emergindo do forame esfenopalatino.
Figura 2. Fotografia da fossa nasal direita evidenciando dois ramos arteriais emergindo do forame esfenopalatino principal. Observar a correlação anatômica existente entre o seio maxilar esquerdo, espinha etmoidal anterior e o forame esfenopalatino.
A análise histológica de todas as amostras colhidas confirmou a origem arterial das estruturas visualizadas.
DISCUSSÃO
O conhecimento anatomocirúrgico da artéria esfenopalatina e seus ramos é de fundamental importância para o tratamento endoscópico da epistaxe posterior grave. A taxa de sucesso pode ser superior a 95% quando realizado por cirurgiões experientes. Além disso, é um procedimento associado a poucas complicações7. Contudo, as variações anatômicas da cavidade nasal podem dificultar a exposição dos ramos principais e acessórios da artéria esfenopalatina. O ideal seria identificar alguns marcos anatômicos que serviriam para facilitar o cirurgião na localização dessas estruturas. Os estudos sobre anatomia nasal, seja com cadáveres ou crânios secos, objetivam a identificação desses marcos anatômicos, como também suas possíveis variações.
Observou-se que a metodologia empregada entre os estudos de anatomia nasal variam com relação ao espécime e técnica utilizada. HerreraTolosana et al.8 fizeram um estudo descritivo de 32 hemicrânios ósseos e sem a utilização de nenhum equipamento de ópticas. Já Shires et al.9 demonstraram várias referências anatômicas em 45 cabeças seccionadas sagitalmente utilizando uma óptica de zero grau e um sistema de videocâmera. Na maioria dos seus trabalhos, Navarro et al.10 fazem referências às distâncias entre o FEP e vários outros pontos anatômicos nasais utilizando hemicrânios e cabeças de cadáveres sob o olhar direto. Nosso estudo optou pela utilização de equipamentos de videoendoscopia por se tratar, também, de uma oportunidade para o ensino e treinamento cirúrgico dos residentes e otorrinolaringologistas participantes.
A citação da faixa etária dos espécimes analisados nos estudos sobre anatomia nasal raramente é encontrada. Sabemos que o desenvolvimento crânio facial ósseo, da infância até a idade adulta, altera as relações entre as referências cirúrgicas do crânio11. No presente estudo, tivemos apenas dois cadáveres jovens, um com 11 anos e outro com 15 anos, não permitindo uma análise osteológica consistente. Talvez estudos com uma amostragem maior e com o enfoque na faixa etária poderão evidenciar melhor as diferenças de posição entre as estruturas endonasais, contribuindo muito com o tratamento de tumores vasculares e outras comorbidades nasais da infância12.
A espinha etmoidal está presente e bem próxima ao forame esfenopalatino na maioria dos seres humanos. Vários autores consideram esta espícula óssea como o principal ponto de referência anatômica aos cirurgiões que se encontram em dificuldades para ligadura da artéria esfenopalatina durante um episódio de epistaxe10,13. Ao estudarem 22 cadáveres, Bolger et al.13 observaram que 21 espécimes apresentam a espícula etmoidal anterior ao FEP e que em apenas um caso esta espícula estava 3 mm abaixo do FEP. Da mesma forma, Pádua & Voegels3 demonstraram que em 98,4% dos casos analisados a espinha etmoidal se encontrava anterior ao forame esfenopalatino. No presente estudo, também observamos que na maioria dos casos (86%) a espinha etmoidal se encontrava anterior ao forame esfenopalatino. Porém, observamos que, em um caso, a espinha etmoidal se encontrava superior ao FEP e em outro caso posterior ao FEP. Em apenas um cadáver a espinha etmoidal estava ausente bilateralmente e em outro cadáver presente somente à esquerda. Apesar destas variações, também consideramos a espinha etmoidal um importante marco anatômico no tratamento de episódios de epistaxe grave.
Herrera Tolosana et al.8, ao estudar 32 hemicrânios ósseos, demonstraram com precisão a localização do FEP. Em sua amostra, a porção mais superior do FEP se localizava ao mesmo nível da porção mais elevada do arco da coana em 62,5% dos casos. Nos outros 32,5%, a porção mediana do FEP estava nivelada com a porção mais alta do arco da coana. Scanavini et al.14 descrevem a localização do FEP no meato superior em 81,4% dos casos. As outras localizações foram entre o meato médio e o meato superior em 14,8% dos casos, no meato médio em apenas um caso e em um caso não foi localizado o FEP. Em nossa análise, encontramos o FEP em todos os casos localizados na transição do meato médio para o meato superior. Esta seria a localização mais frequente dos FEP, também observada em outros estudos3,15. Consideramos que a localização do FEP em cadáveres frescos ser mais difícil comparada à localização em hemicrânios secos. A peça anatômica seca permite maior precisão ao medir rebordos e forames ósseos comparada a cadáveres frescos com mucosa nasal íntegra e vasos sangrantes.
Simmen et al.16 discutem a quantidade e a localização dos ramos que emergem do FEP. Descreveram que a maioria dos espécimes apresentam de dois a três ramos arteriais e, em um caso, até 10 ramos arteriais. Explicam, também, que estes ramos se distribuem superior e inferiormente à espinha etmoidal e que não foi possível comparar os lados porque os espécimes foram de cabeças diferentes. Da mesma forma, Babin et al.17 descrevem que a apresentação com dois e três ramos é a mais comum e referem um caso com até cinco ramos. Nosso estudo observou que a maioria dos cadáveres apresentava mais de um ramo arterial em 18 casos. Em dois casos, observou-se que o lado esquerdo apresentava um ramo a mais do que o lado direito. Somente a completa exposição da mucosa adjacente ao FEP permite a visualização de todos esses ramos arteriais emergentes. Desta forma, novamente acreditamos que o domínio da técnica de dissecção do FEP pode determinar o sucesso do tratamento cirúrgico da epistaxe grave.
A presença do forame acessório na parede lateral nasal é bem estabelecida na literatura; entretanto, sua frequência é bastante variável. Sua presença poderia estar relacionada com a falha no tratamento endoscópico da epistaxe posterior grave18. Pádua & Voegels3 encontraram o forame acessório em apenas 12 (10%) casos estudados. Já em nosso estudo, observamos que 12 (43%) cadáveres apresentaram o FEA. Nossos resultados são semelhantes aos de Herrera Tolosana et al.8, que encontraram o FEA em 16 (50%) casos, sendo seis casos com dois orifícios e dez casos com apenas um. Quanto a localização do FEA, Herrera Tolosana et al.8 relatam que estes se localizam mais no meato médio (73%) logo abaixo do FEP. Também observamos que orifícios ósseos menores por onde emergiam ramos arteriais diferentes do forame principal, na maioria das vezes localizavam-se no meato médio. Estes considerados como forames esfenopalatinos acessórios (FEAs), na maioria das vezes eram únicos. Navarro et al.10 acreditavam que um desses ramos acessórios poderiam constituir a artéria nasal lateral posterior e outros ramos arteriais. Entendemos que um consenso quanto ao nome destes ramos acessórios seria muito complexo, uma vez que são evidentes as variações anatômicas destes vasos. O simples conhecimento da possível presença destes forames acessórios durante uma cirurgia endoscópica nasal pode evitar manobras ou dissecções inadvertidas da parede nasal lateral, diminuindo a morbidade e o tempo sob anestesia geral dos nossos pacientes.
Como forma de garantir a identificação de todos os ramos e forames da artéria esfenopalatina, propomos a delimitação do "quadrilátero esfenopalatino" (Figura 3) endoscópico da irrigação da parede posterior nasal. Estes limites se coincidem com as bordas de um quadrado com as seguintes denominações:
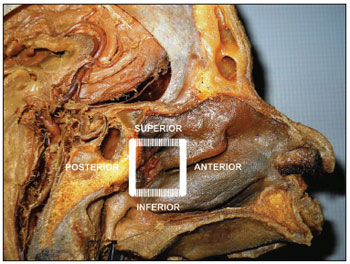
Figura 3. Fotografia de crânio em corte sagital com exposição da fossa nasal esquerda e da artéria esfenopalatina ipsilateral. O conhecimento dos limites do "quadrilátero esfenopalatino" pode ajudar o cirurgião a identificar todos os ramos e forames da artéria esfenopalatina.ANTERIOR: A borda anterior da porção perpendicular do osso palatino é o melhor ponto cirúrgico para se iniciar a dissecção do retalho mucoperiosteal. A forma mais fácil para se encontrar este ponto é palpando a fontanela posterior do seio maxilar ao nível da porção horizontal da concha média. A fontanela posterior do seio maxilar é uma estrutura móvel e macia. Ao continuar sua palpação de anterior para posterior na fossa nasal, logo se encontra uma superfície dura e rígida, que é exatamente a pilar óssea anterior do osso palatino, onde se inicia o descolamento mucoperiosteal (Figuras 3 e 4).
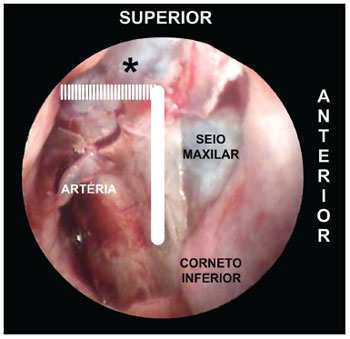
Figura 4. Fotografia da fossa nasal esquerda com detalhes do "quadrilátero esfenopalatino". O limite superior para se encontrar os forames acessórios esfenopalatinos é o tecido gorduroso da fossa pterigopalatina (*). A porção perpendicular do osso palatino é o limite anterior para se iniciar a confecção do retalho mucoperiosteal em busca do forame esfenopalatino principal.SUPERIOR: O ponto mais alto do pilar anterior do osso palatino se encerra no encontro do tecido gorduroso da fossa pterigopalatina. A dissecção do retalho mucoperiosteal até este nível identificará todos os possíveis forames acessórios desta porção superior do complexo arterial esfenopalatino (Figura 4). INFERIOR: A inserção da concha inferior é o ponto mais inferior da extensão do retalho mucoperiosteal. A partir desta linha não se identificam ramos acessórios da artéria esfenopalatina (Figura 5).
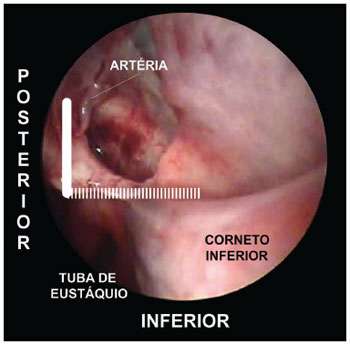
Figura 5. Fotografia da fossa nasal esquerda. O limite inferior do "quadirilátero esfenopalatino" é a porção superior do corneto inferior. Já a tuba de Eustáquio é o limite posterior do retalho mucoperiosteal.POSTERIOR: Ao se identificar parede anterior do seio esfenoide e a tuba auditiva de Eustáquio, conclui-se a dissecção do retalho mucoperiosteal com a certeza de que todos ramos e forames da artéria esfenopalatina foram identificados (Figura 5).
CONCLUSÃO
A anatomia da artéria esfenopalatina é bastante variável. A espinha etmoidal é um importante marco anatômico, estando presente em quase todos os casos e anterior ao forame esfenopalatino. A principal localização no forame esfenopalatino foi na transição do meato médio com o superior.
REFERÊNCIAS
1. Andrade NA, Felippu Neto A. Epistaxe Grave. In: Campos CAH, Costa HOO. Sociedade Brasileira de Otorrinolaringologia. Tratado de Otorrinolaringologia. São Paulo: Rocca; 2002. p.209-15.
2. Walker TW, Macfarlane TV, McGarry GW. The epidemiology and chronobiology of epistaxis: an investigation of Scottish hospital admissions 1995-2004. Clin Otolaryngol. 2007;32(5):361-5.
3. Pádua FG, Voegels RL. Severe posterior epistaxis-endoscopic surgical anatomy. Laryngoscope. 2008;118(1):156-61.
4. Solari D, Magro F, Cappabianca P, Cavallo LM, Samii A, Esposito F, et al. Anatomical study of the pterygopalatine fossa using an endoscopic endonasal approach: spatial relations and distances between surgical landmarks. J Neurosurg. 2007;106(1):157-63.
5. Prades JM, Asanau A, Timoshenko AP, Faye MB, Martin C. Surgical anatomy of the sphenopalatine foramen and its arterial content. Surg Radiol Anat. 2008;30(7):583-7.
6. Nouraei SA, Maani T, Hajioff D, Saleh HA, Mackay IS. Outcome of endoscopic sphenopalatine artery occlusion for intractable epistaxis: a 10-year experience. Laryngoscope. 2007;117(8):1452-6.
7. Kumar S, Shetty A, Rockey J, Nilssen E. Contemporary surgical treatment of epistaxis. What is the evidence for sphenopalatine artery ligation? Clin Otolaryngol Allied Sci. 2003;28(4):360-3.
8. Herrera Tolosana S, Fernández Liesa R, Escolar Castellón Jde D, Pérez Delgado L, Lisbona Alquezar MP, Tejero-Garcés Galve G, et al. Estudio anatómico del orificio esfenopalatino. Acta Otorrinolaringol Esp. 2001;62(4):274-8.
9. Shires CB, Boughter JD, Sebelik ME. Sphenopalatine artery ligation: a cadaver anatomic study. Otolaryngol Head Neck Surg. 2011;45(3):494-7.
10. Navarro JAC, Navarro PL, Navarro MC. Anatomia da cavidade nasal e seios paranasais. In: Campos CAH, Olival HOO. Tratado de Otorrinolaringologia. São Paulo: Rocca; 2002. p.591-610.
11. Inada E, Saitoh I, Hayasaki H, Yamada C, Iwase Y, Takemoto Y, et al. Cross-sectional growth changes in skeletal and soft tissue cephalometric landmarks of children. Cranio. 2008;26(3):170-81.
12. Wu AW, Mowry SE, Vinuela F, Abemayor E, Wang MB. Bilateral vascular supply in juvenile nasopharyngeal angiofibromas. Laryngoscope. 2011;121(3):639-43.
13. Bolger WE, Borgie RC, Melder P. The role of the crista ethmoidalis in endoscopic sphenopalatine artery ligation. Am J Rhinol. 1999;13(2):81-6.
14. Scanavini ABA, Navarro JAC, Megale SRMCL, Anselmo-Lima WT. Anatomical study of the sphenopalatine foramen. Braz J Otorhinolaryngol. 2009;75(1):37-41.
15. Wareing MJ, Padgham ND. Osteologic classification of the sphenopalatine foramen. Laryngoscope. 1998;108(1 Pt 1):125-7.
16. Simmen DB, Raghavan U, Briner HR, Manestar M, Groscurth P, Jones NS. The anatomy of the sphenopalatine artery for the endoscopic sinus surgeon. Am J Rhinol. 2006;20(5):502-5.
17. Babin E, Moreau S, de Rugy MG, Delmas P, Valdazo A, Bequignon A. Anatomic variations of the arteries of the nasal fossa. Otolaryngol Head Neck Surg. 2003;128(2):236-9.
18. Schwartzbauer HR, Shete M, Tami TA. Endoscopic anatomy of the sphenopalatine and posterior nasal arteries: implications for the endoscopic management of epistaxis. Am J Rhinol. 2003;17(1):63-6.
1. Mestre pela Universidade de Brasília (Otorrinolaringologista do Hospital de Base do Distrito Federal).
2. Otorrinolaringologista pelo Hospital Universitário de Brasília (Fellow em ORL do Hospital Universitário de Brasília).
3. Médica Patologista (Chefe do Departamento de Anatomia Patológica do Hospital de Base do Distrito Federal).
4. Pós-Doutorado pela Harvard Medical School, Boston, MA, EUA (Professor Adjunto e Chefe do Departamento de Otorrinolaringologia e Cirurgia de Cabeça e Pescoço, Universidade de Brasília).
5. Doutor em Otorrinolaringologia pela Faculdade de Medicina da Universidade de São Paulo (Professor Adjunto do Departamento de Otorrinolaringologia e Cirurgia de Cabeça e Pescoço, Universidade de Brasília e Otorrinolaringologista da Secretaria de Saúde do Distrito Federal).
Universidade de Brasília.
Endereço para correspondência:
Gustavo Lara Rezende
SHIS Qi 15, bloco O, torre 1, sala 11A
Brasília - DF. CEP: 70390-050
Tel: (61) 3364-4661
Email: glararezende@gmail.com
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da BJORL em 4 de novembro de 2011. cod. 8884.
Artigo aceito em 18 de março de 2012.