Ano: 2009 Vol. 75 Ed. 5 - Setembro - Outubro - (13º)
Seção: Artigo Original
Páginas: 694 a 700
Análise do Efeito Citoprotetor da Amifostina na Orelha Interna Irradiada de Cobaias: Estudo Experimental
Analysis of the Cytoprotective Effect of Amifostine on the Irradiated Inner Ear of Guinea Pigs: An Experimental Study
Autor(es): Ricardo Miranda Lessa1, José Antônio Aparecido de Oliveira2, Maria Rossato3, Thomaz Ghilardi Netto4
Palavras-chave: amifostina, irradiação, orelha interna, perda auditiva, órgão de corti.
Keywords: amifostine, irradiation, inner ear, hearing loss, organ of corti.
Resumo:
A radiação pode causar lesão na orelha interna podendo provocar surdez sensório-neural e inclusive levar à anacusia. A amifostina é uma substância citoprotetora seletiva de tecidos sadios, amplamente utilizada durante a radio e quimioterapia de tumores malignos. Objetivo: O objetivo deste estudo experimental foi verificar se existe efeito antioxidante e radioprotetor da amifostina no órgão de Corti de cobaias albinas irradiadas em região de cabeça e pescoço. Material e Método: O estudo realizado envolveu quatro grupos de animais: um grupo foi submetido à irradiação em dose única de 350cGy. Dois grupos receberam a mesma dose de radiação, porém receberam doses de 100 e 200mg/kg de amifostina, 30 minutos antes da irradiação. Um grupo recebeu apenas amifostina, na dose de 200mg/Kg. Todas as cobaias foram sacrificadas 30 dias após o experimento e suas bulas retiradas para estudo em microscópio de varredura. Resultado: O grau de lesão das células ciliadas externas foi menor nos dois grupos que receberam a amifostina que no grupo apenas irradiado. Não foi encontrada diferença de proteção entre os grupos que receberam doses de 100 e 200mg/kg de amifostina. Não houve lesão no grupo que recebeu apenas amifostina. Conclusão: Amifostina mostrou ser um radioprotetor do órgão de Corti de cobaias albinas irradiadas.
Abstract:
Radiation can cause damage to the inner ear, from a simple hearing loss all the way to profound deafness. Amifostine is a cytoprotective substance extensively used during radio-chemotherapy for malignant tumors. Aim: the objective of the present investigation was to establish the antioxidant and radioprotective effects of amifostine on the organ of Corti of albino guinea pigs irradiated in the head and neck region. Materials and Methods: An experimental study conducted on four groups of guinea pigs were used; One group received only amifostine, one group was submitted to a single dose of 350 cGy and the other two were similarly irradiated but received amifostine doses of 100 or 200 mg/kg. All animals were slaughtered 30 days after the experiment, their bullae were removed and the damaged outer hair cells were counted. Result: The extent of injury was lower in the outer hair cells of the two groups treated with amifostine compared to the group that was only irradiated. There was no difference between the group treated with 100 and 200 mg/kg of amifostine. The group that received only amifostine had no cochlear damage. Conclusion: Amifostine is an effective cytoprotective substance in the Organ of Corti of irradiated guinea pigs.
![]()
INTRODUÇÃO
A radioterapia constitui uma das formas de tratamento mais utilizada nos tumores malignos localizados na região da cabeça e pescoço. O seu mecanismo de ação sobre as células cancerígenas se baseia na desestruturação da sequência de seus nucleotídeos, desta forma, modificando as moléculas, proteínas e DNA (ácido desoxirribonucleico) das células, comprometendo o seu metabolismo e o mecanismo de divisão celular, impedindo assim, o crescimento tumoral.
Um dos grandes inconvenientes da radioterapia em cabeça e pescoço é o fato de o osso temporal e as estruturas da orelha interna se encontrarem no campo de radiação da maioria dos tumores, tal como ocorre nos tumores da rinofaringe, onde o aparelho auditivo pode ser inevitavelmente envolvido no campo de irradiação e o paciente poder evoluir com de perda auditiva de variados graus de intensidade, podendo inclusive tornar-se anacúsico1,2.
Ao atingir o órgão vestíbulo-coclear, distúrbios auditivos e do equilíbrio podem surgir3. Dentre eles, a perda auditiva sensório-neural é a complicação mais comum e está em maior frequência associada à lesão e perda de células ciliadas externas do órgão de Corti4.
Muitos esforços têm sido feitos na tentativa de minimizar ou neutralizar a ação da irradiação na orelha interna, porém os maiores avanços têm sido notados apenas no campo do desenvolvimento de novas técnicas e equipamentos emissores de radiação e fontes de energia tipo prótons, os quais têm reduzido os efeitos da radiação sobre o órgão auditivo5,6.
Vários estudos com drogas citoprotetoras contra os efeitos deletérios da radiação em tecidos normais estão disponíveis na literatura. No entanto, quase não existem estudos relacionados à ação de drogas protetoras da radiação especificamente nas estruturas da orelha interna.
Uma das principais drogas em evidência no momento, pela sua baixa toxicidade e por se tratar de um potente citoprotetor seletivo de tecidos normais contra os efeitos adversos da radioterapia é a amifostina.
O objetivo deste estudo foi verificar se a amifostina, administrada nas doses de 100 e 200mg/Kg, intraperitoneal, previamente à irradiação da orelha interna na dose de 350cGy, desempenha função citoprotetora na orelha interna e se, existindo essa proteção, ela se faz de forma diferenciada e seletiva privilegiando determinadas espiras ou grupos de células ciliadas dentro de uma mesma espira.
MATERIAL E MÉTODO
O presente estudo envolveu 51 cobaias albinas, do sexo masculino pesando entre 300 e 450g que passaram na triagem auditiva pelo reflexo de Preyer positivo7 e presença de Emissões otoacústicas - produtos de distorção, previamente ao início do estudo, realizados em equipamento da marca ILO 92 CAE System Otodynamics LTD. A intensidade do estímulo desencadeante foi de 70dB NPS tanto para F1 quanto para F2, seguindo a relação de frequências 2F1-F2 com proporção F1:F2 = 1,22 e resolução dois pontos por oitava.
Os animais foram divididos em quatro grupos distintos, a saber: Grupo amifostina - composto de quatro animais, recebeu isoladamente amifostina na dose de 200mg/Kg, intraperitoneal (IP), e serviu com um controle negativo do experimento, uma vez que não se encontra descrito na literatura nenhum efeito ototóxico dessa droga; Grupo Irradiação (Irr) - formado por 11 cobaias que receberam apenas a irradiação na região de cabeça e pescoço na dose de 350cGy, simetricamente em cada orelha; Grupo amifostina 100mg+Irradiação (Irr+100mg)- composto de 18 cobaias que receberam amifostina na dose de 100mg/kg, IP, 30 minutos antes da irradiação na dose de 350cGy; Grupo amifostina 200mg+Irradiação (Irr+200mg) - composto de 18 cobaias que receberam amifostina na dose de 200mg/kg,IP, 30 minutos antes da irradiação na dose de 350cGy. Todos os grupos permaneceram no laboratório de cirurgia experimental, atendendo as exigências de alimentação e confinamento preconizados pelo Comitê de Ética em Experimentação Animal, protocolo 043/2005 aprovado em 27 de março de 2006, sendo sacrificados 30 dias após a data do experimento.
O método utilizado para comparação do grau de lesão do órgão de Corti foi a contagem das células ciliadas externas que se encontravam ausentes nas três fileiras de três espiras da cóclea: E1, E2, E3. O parâmetro para classificação de lesão considerado foi a ausência total de cílios, ou seja, a perda completa da projeção filamentar dos cílios sobre a placa cuticular. O local escolhido para contagem das células foi o seguimento médio de cada espira, obtendo-se o maior número de células possível, dentro de um campo microscópico fotográfico a um aumento de 350 a 700 vezes. Todas as espiras foram fotografadas e os negativos revelados para posterior processo de análise. Os números resultantes desta contagem celular foram transformados em frações do numero total de células ausentes dividido pela população total de células daquele campo fotográfico analisado.
Para a comparação entre os grupos de estudo foram feitas três análises: a primeira comparou o percentual de células lesadas entre os grupos (Irr, Irr+100mg e Irr+200mg) levando-se em consideração o percentual do somatório de células ciliadas externas lesadas nas três espiras (E1, E2 e E3) de cada grupo; a segunda comparou o percentual de células ciliadas externas lesadas em cada espira (E1, E2 e E3) entre os três grupos estudados; a terceira comparou o percentual de células ciliadas externas lesadas em cada fileira (F1, F2 e F3) entre os três grupos.
Os resultados então foram submetidos à análise estatística utilizando-se o programa Statistical Package for Social Sciencies - (SPSS). Na comparação dos valores entre os três grupos foi utilizado o teste não-paramétrico de Kruskal-Wallis com teste post hoc de Dunn quando verificado a existência de diferença significativa. Para esta análise estatística foi adotado como nível de significância um valor de p < 0,05.
RESULTADOS
O presente trabalho envolveu um total de 51 cobaias, sendo que ocorreram sete mortes. Dessas, duas foram do grupo Irr+200mg, quatro do grupo Irr+100mg, e uma do grupo amifostina. Todas as mortes ocorreram por conta de diarreia de provável causa viral. Das 44 cobaias restantes resultaram 88 cócleas, sendo que no final do estudo foram computadas apenas 84, pois três cócleas foram excluídas do trabalho, visto que as cobaias apresentaram sinais de inflamação/infecção na orelha média e 1 cóclea foi perdida por ficar extremamente danificada após a sua dissecação.
Por não ter havido nenhum grau de lesão no grupo que recebeu apenas amifostina, o que condiz com achados da literatura, os estudos comparativos foram procedidos apenas entre os demais grupos do estudo.
Comparação do percentual do total de CCE entre os grupos
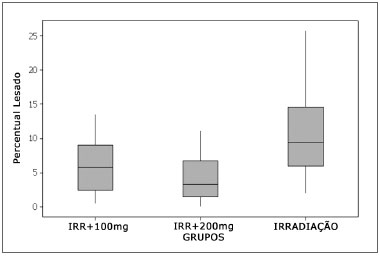
Na comparação dos totais de CCE lesadas em cada grupo do estudo observou-se que, no grupo Irr o percentual total de lesões das CCE foi significativamente maior que nos grupos Irr+100mg e Irr+200mg, que se equivaleram (Figura 1).
Figura 1. Percentuais de CCE lesadas em cada grupo.
Comparação do percentual de células ciliadas externas lesadas em cada espira (E1, E2 eE3) entre os grupos
Espira 1
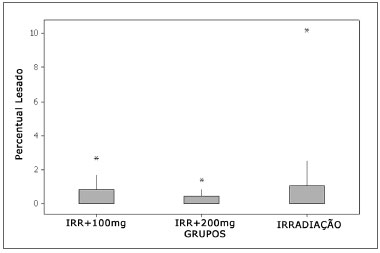
Na espira 1 quase não foram observadas lesões em nenhum dos grupos estudados e, quando elas ocorreram, foram de forma isolada e inconstante. Aplicando-se o teste estatístico, não houve diferença significativa entre os grupos que receberam amifostina (100mg/kg e 200mg/kg) antes da irradiação e o que foi irradiado isoladamente na dose de 350cGy (Figura 2 e 3).
Figura 2. Percentuais de CCE lesadas na espira 1.
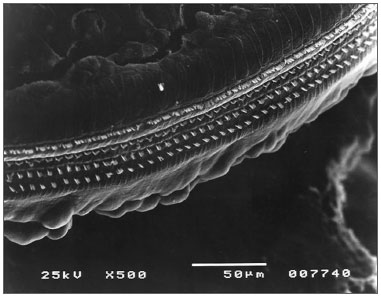
Figura 3. Seguimento sem lesões da espira 1 do grupo Irr.
Espira 2
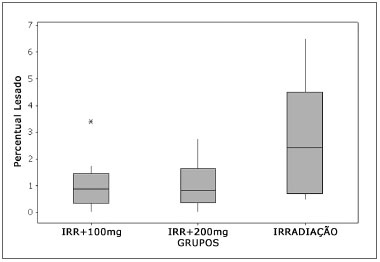
Na segunda espira, observou-se um aumento nas falhas nas fileiras de células ciliadas externas, principalmente ocorridas no grupo que não usou amifostina previamente à irradiação. O maior grau de lesão ocorrida neste grupo foi estatisticamente significante quando comparados os totais de células lesadas desta espira com os outros dois grupos que receberam amifostina antes da irradiação. Entre os grupos que receberam amifostina não existiu diferença significante (Figuras 4 e 5).
Figura 4. Percentuais de CCE lesadas na espira 2.
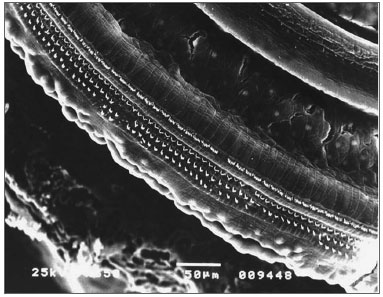
Figura 5. Espira 2 do grupo Irr+200mg mostrando preservação CCE.
Espira 3
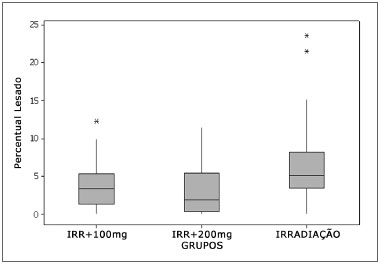
Na terceira espira, em comparação com a E2, observou-se uma maior tendência de lesão nos três grupos. Aqui, também os grupos Irr+100mg e Irr+200mg mostraram valores significativamente inferiores ao grupo irradiado isoladamente. Os dois grupos que usaram amifostina se equivaleram e não mostram diferença significante (Figuras 6 e 7).
Figura 6. Percentuais de CCE lesadas na Espira 3.
Figura 7. Espira 3 do grupo Irr+200mg com preservação CCE.
Comparação do percentual de células ciliadas externas lesadas em cada fileira (F1, F2 e F3) entre os grupos.
Espira 1 - Fileiras 1, 2 e 3
Na comparação feita entre as fileiras da primeira espira, não houve diferença significativa entre os percentuais de CCE lesadas nos grupos em estudo (Figura 8).
Figura 8. Espira 1 do grupo Irr+200mg sem lesões.
Espira 2 - Fileiras 1,2 e 3
Na comparação dos percentuais de CCE lesadas entre as fileiras isoladamente nos grupos, observou-se que, apesar de as maiores médias de lesão ocorreram na segunda (F2) e terceira (F3) fileiras, apenas na primeira fileira (F1) foi notada diferença significativa pelo teste post hoc de Dunn, onde o grupo irradiado isoladamente (Irr) apresentou valores significativamente superiores de lesão aos dos grupos Irr+ 100mg e Irr+200mg, que se equivaleram (Figura 9).
Figura 9. Espira 2 do grupo Irr mostrando lesão de F2 e F3 e preservação de F1
Espira 3 - Fileiras 1,2 e 3
Comparando-se os percentuais de CCE lesadas entre as fileiras isoladamente nessa espira, notou-se uma tendência de maiores médias de lesões na segunda (F2) e terceira (F3) fileiras, repetindo o que ocorreu na espira 2. Porém aqui, apenas na terceira (F3) fileira houve aumento estatisticamente significante de lesão no grupo apenas irradiado, comparado aos outros dois grupos que receberam amifostina nas doses de 100mg e 200mg/kg, que se equivaleram (Figura 10).
Figura 10. Espira 3 do grupo Irr com grande número de lesões ciliadas em F2 e F3.
DISCUSSÃO
A perda auditiva induzida pela radioterapia, apesar de ser um assunto da maior relevância, ainda é pouco diagnosticada nos dias atuais e, de certa forma, pouco valorizada e prevenida no meio dos profissionais envolvidos com esta modalidade de tratamento. Isto se deve, em parte, ao desconhecimento dos avanços de novas técnicas de radioterapia com maior potencial otoprotetor e das recentes descobertas de drogas com potencial radioprotetor para tecidos normais adjacentes ao tumor, inclusive do órgão auditivo.
Quanto aos tipos de disacusia induzidos pela radioterapia, é sabido que podem ser condutivas, sensório-neurais e mistas. A perda auditiva sensório-neural é, sem dúvida, a mais frequente, segundo alguns autores podendo ocorrer em até 75% dos pacientes irradiados na região do osso temporal, e costuma desenvolver-se pela lesão ao órgão de Corti e em menor frequência uma degeneração do VIII par craniano, visto que as estruturas do sistema nervoso central têm uma maior resistência a essa modalidade de tratamento8.
Quanto à dose lesiva para o órgão de Corti, quanto maior a dose de irradiação na orelha interna, maior é a probabilidade de dano auditivo9. Em geral, a dose total de radiação necessária para produzir uma lesão ao sistema auditivo varia entre 3000 e 6000 cGy, quando dividida em pequenas frações10-12. Em nosso estudo, a dose utilizada suficiente para provocar lesão imediata às células ciliadas foi 350cGy, aplicada em dose única. Esta dose foi determinada através de um estudo piloto, previamente realizado em nosso Departamento, visto que não existiam informações na literatura sobre a dose média lesiva ao órgão de Corti de cobaias albinas.
A perda da audição após a radiação pode instalar-se de forma imediata ou tardia2. A complicação imediata resulta da injúria celular direta pela radiação sobre estruturas do órgão de Corti e da estria vascular. Já os efeitos tardios ocorrem pela ação indireta da radiação sobre os vasos da orelha interna, gerando o processo de endoarterite obliterante, que progressivamente interrompe o aporte sanguíneo a estruturas vitais como o neuroepitélio da cóclea e o VIII par craniano13-15.
Com referência à faixa de frequências mais atingida, as frequências graves e médias raramente são comprometidas. Já os tons agudos são os mais afetados destacando-se a faixa de frequências entre 4000 a 8000Hz4,15. Os nossos achados apontaram para a lesão preferencialmente ocorrendo nas segunda e terceira espiras, com a preservação da primeira espira e a espira apical. Na comparação do grau de lesão entre a E2 e E3 notou-se que os percentuais de lesão foram superiores na terceira espira ultrapassando, na maioria dos casos, em duas vezes o que ocorrera na segunda espira. Esse mecanismo de seletividade para as espiras e consequentemente para as frequências auditivas é provável que se deva ao maior consumo de oxigênio existente nas células ciliadas e estria vascular mais próximas da base da cóclea, o que as torna mais sensíveis16.
Outro dado também observado foi que houve uma tendência a um aumento dos percentuais de células lesadas na segunda e terceira espiras, principalmente nas duas últimas fileiras mais externas, com preservação da primeira e mais interna. Este fato também notado em outros estudos experimentais envolvendo a radiação se deve, provavelmente, a diferentes necessidades metabólicas que ocorrem entre esses grupos celulares já apontadas por alguns autores que detectaram diferenças anatômicas e de constituição bioquímica nas células ciliadas externas, em diferentes setores da cóclea4,17-19.
No tocante ao emprego de drogas otoprotetoras na radioterapia, Atlas et al. (2006) conseguiram reduzir os danos cocleares induzidos pela radiação no gânglio espiral, estria vascular, células ciliadas internas e externas de cobaias que foram tratadas com piracetam uma hora antes da irradiação na dose de 60Gy, pelo mecanismo de inibição da apoptose celular20.
A amifostina é uma pró-droga que é convertida pela fosfatase alcalina na molécula ativa WR-1065. O WR-1065 interage com radicais livres doando íons hidrogênio que se ligam às moléculas de oxigênio e aos metabólitos ativos dos agentes antineoplásicos21,22. Isso já conferiu à amifostina o status de um eficiente citoprotetor na hematotoxicidade da ciclofosfamida e carboplastina, na neurotoxicidade, nefrotoxicidade, hematoxicidade e ototoxicidade da cisplatina23-25. Glover et al. (1984) estudaram o efeito da amifostina na orelha interna de pacientes que receberam quimioterapia pela cisplatina e constataram redução dos índices de disacusia em pacientes recebendo cisplatina na dose de 150mg/m²26. Hyppolito et al. (2005) compararam o numero de células ciliadas externas lesadas e o comportamento das EOAPD em cobaias tratadas com e sem amifostina e que receberam a cisplatina. Concluíram que a perda de células ciliadas externas foi menor no grupo amifostina e que as emissões otoacústicas encontravam-se presentes em todos os animais deste grupo após uso do ototóxico27.
Na radioterapia a amifostina protege várias linhagens celulares dos efeitos da irradiação. Esta droga já foi testada amplamente e mostrou ser efetiva na radioproteção da medula óssea reduzindo os índices de hematotoxicidade minimizando a trombocitopenia, anemia e leucopenia28,29. Em tumores de cabeça e pescoço acredita-se que a amifostina possa reduzir a radiotoxicidade às glândulas salivares, mucosa esofágica e da cavidade oral, minimizando os efeitos adversos da mucosite e xerostomia que comprometem substancialmente a qualidade de vida dos pacientes pós-irradiados30,31.
Em nosso estudo ficou evidente que a amifostina protegeu de maneira significativa os grupos Irr+100mg e Irr+200mg que receberam a droga pela via intraperitoneal, 30 minutos antes da irradiação da orelha interna, porém não se observou diferença significante de proteção apenas com a variação da dose de 100mg/kg para 200mg/kg. Essa proteção foi visivelmente marcada nas proporções de células ciliadas lesadas e representou uma redução de até 40% dos percentuais de lesão nas CCE dos grupos que receberam a amifostina. Essa redução provavelmente se deveu às diferenças de lesão ocorridas na segunda e terceira espiras que, na comparação entre os grupos, apontou para uma redução no percentual de lesão ocorridas nos grupos Irr+100mg e Irr+200mg quando comparados ao grupo Irr. Na comparação dos percentuais de lesão da espira 1 entre os grupos, não houve diferença significante de lesão em nenhum dos três grupos. Isso pode ser explicado pelo baixo nível de lesão ocorrida pela radiação neste setor da cóclea em particular.
Quando comparados os grupos em termos de fileiras, apenas a primeira fileira da E2 e a terceira fileira da E3 mostraram valores inferiores e estatisticamente significantes de lesão ciliada nos grupos Irr+100mg e Irr+200mg. Esse, sem dúvida, é um achado desse trabalho, mas que mereceria aguardar novos experimentos para se verificar se foi um fenômeno casual ou uma especificidade para a droga utilizada.
CONCLUSÕES
A amifostina utilizada previamente à radiação da orelha interna protegeu significativamente as células ciliadas externas do órgão de Corti de Cobaias irradiadas em região de cabeça e pescoço pelo Cobalto 60, na dose de 350cGy e de maneira significativa protegeu a segunda e terceira espiras da cóclea, fato que não se repetiu na primeira espira. Apenas a primeira fileira da segunda espira e a terceira fileira da terceira espira mostraram valores significativamente inferiores de lesão ciliada nos grupos que receberam o citotoprotetor e não houve diferença significante na resposta protetora das células ciliadas externas quando se aumentou a dose da amifostina de 100mg para 200mg/kg.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Sataloff RT, Rosen DC. Effects of irradiation on hearing acuity: a review of the literature. Am J Otol. 1994;15:772-80.
2. Young, Y. & Lou, P. Post-irradiation sudden deafness. J Laryngol Otol. 1999;113(9):815-7.
3. Gamble JE, Peterson EA, Chandler JR. Radiation effects on the inner ear. Arch Otolaryngol. 1968;88:64-9.
4. Winther FO. X Ray irradiation of the inner ear of the guinea pig, early degenerative changes in the cochlea. Acta Otolaryngol. 1969;68:98-117.
5. Lin R, Hug EB, Schaefer RA, Miller DW, Slater JM, Slater JD. Conformal proton radiation therapy of the posterior fossa:a study comparing protons with three-dimensional planned photons in limiting dose to auditory structures. Int J Radiat Oncol Biol Phys. 2000;48:1219-26.
6. Huang E, Teh BS, Strother DR, Davis QG, Chiu JK, Lu HH et al. Intensity-modulated radiation therapy for pediatric medulloblastoma: early report on reduction of ototoxicity. Int J Radiat Oncol Biol Phys. 2002;52:599-605.
7. Jero J, Coling DE, Lalwani AK. The use of preyer's reflex in evaluation of hearing in mice. Acta Otolaryngol. 2001;121(5):586-9.
8. Leighton SEJ, Kay R, Leung SF, Woo JKS, Hasselt CAV. Auditory brainstem responses after radiotherapy for nasopharyngeal carcinoma. Clin Otolaryngol. 1997;22:350-4.
9. Ondrey FG, Greig JR, Hersher L. Radiation dose to the otologic structures during head and neck cancer radiation therapy. Laryngoscope. 2000;110:217-21.
10. Talmi YP, Finkelstein Y, Zohar Y. Post irradiation Hearing loss. Audiology. 1989;28:121-6.
11. Chen W, Liao C, Wang C, Tsai H, Tang SG, Yeh J et al. Radiation-induced hearing impairment in patients treated for malignant parotid tumor. Ann Otol Rhinol Laryngol. 1999;108:1159-64.
12. Honoré HB, Bentzen SM, Moller K, Grau C. Sensori-neural hearing loss after radiotherapy for nasopharyngeal carcinoma: individualized risk estimation. Radiother Oncol. 2002;65:9-16.
13. Adler M, Hawke M, Berger G, Harwood A. Radiation effect on the external auditory canal. J Otolaryngol. 1985;14:226-32.
14. Schot LJ, Hilgers FJM, Keus RB, Schouwenburg PF, Dreschler WA. Late effects of radiotherapy on hearing. Eur Arch Otorhinolaryngol. 1992;249:305-8.
15. Hoistad D, Ondrey FG, Mutlu C, Schachern PA, Paparella MM, Adams G. Histopathology of human temporal bone after cis-platinum, radiation, or both. Otolaryngol Head Neck Surg. 1998;118:825-32.
16. Ho WK, Wei WI, Kwong DLW, Sham JST, Tai PTH, Yuen APW et al. Long-term sensório-neural hearing deficit following radiotherapy in patients suffering from nasopharyngeal carcinoma:a prospective study. Head Neck. 1999;21:547-53.
17. Berg NO, Lindgren M. Dose factors and morphology of delayed radiation lesions of the internal and middle ear in rabbits. Acta Radiol. 1961;56:305-19.
18. Hultcrantz M, Anniko M, Borg E. The influence of prenatal gamma irradiation on the ageing of the cochlea. Acta Otolaryngol. 1989;108:414-23.
19. Kim CS, Shin SO. Ultrastructural changes in the cochlea of the guinea pig after fast neutron irradiation. Otolaryngol Head Neck Surg. 1994;110:419-27.
20. Atlas E, Ertekin MV, Kuduban O, Gundogdu C, Demirci E, Sutbeyaz Y. Effects of piracetam supplementation on cochlear damage ocurring in guinea pigs to irradiation. Biol Pharm Bull. 2006;29(7):1460-5.
21. Calabro-Jones PM, Fahey RC, Smoluk GD, Ward JF. Alkaline phosphatase promotes radioprotection and accumulation of WR-1065 in V79-171 cells incubated in medium containing WR-2721. Int J Radiat Biol Relat Stud Phys Chem Med. 1985;47:23-7.
22. Capizzi RL. Amifostine: The preclinical basis for broad-spectrum selective cytoprotection of normal tissues from cytotoxic therapy.Semin Oncol. 1996;23(Suppl 8):2-17.
23. Wasserman HT. Radiotherapeutic Studies With Amifostine. Semin Oncol. 1994;21(5 suppl 11):21-5.
24. Hussain AE, Blakley BW, Nicolas M, Balderston J. Assessment of the effects of amifostine against cisplatin-induced toxicity. J Otolaryngol. 2003;32(5):294-7.
25. Konings AW, Faber H, Vissink A, Coppes RP. Radioprotective effect of amifostine on parotid gland functioning is region dependent. Int J Radiat Oncol Biol Phys. 2005;63(5):1584-91.
26. Glover D, Negendank W, Delivoria-Papadopoulos M, Glick JH. Alterations in oxygen transport following WR-2721. Int J Radiat Oncol Biol Phys. 1984;10(9):1565-8.
27. Hyppolito MA, Oliveira JA, Lessa RM, Rossato M. Otoproteção da Amifostina aos efeitos ototóxicos da cisplatina:estudo em cobaias albinas por emissões otoacústicas produtos de distorção e microscopia eletrônica de varredura. Braz J Otorhinolaryngol. 2005;71(3):268-73.
28. List AF, Heaton R, Glinsmann GB. Amifostine protects primitive human hematopoietic progenitors against cytotoxicity from diverse antineoplastics. Proc Am Soc Clin Oncol. 1996;15:448-50.
29. Capizzi RL, Oster W. Chemoprotective and radioprotective effects of amifostine: an update of clinical trials. Int J Hematol. 2000;72:425-35.
30. Koukourakis MI, Danielidis V. Preventing radiation induced xerostomia. Cancer Treat Rev. 2005;31(7):546-54.
31. Buentzel J, Micke O, Adamietz IA, Monnier A, Glatzel M, Vries A. Intravenous amifostine during chemoradiotherapy for head-and-neck cancer:a randomized placebo controlled phase III study. Int J Oncol Biol Phys. 2006;64(3):684-91.
1 Doutorado, Médico Assistente do Hospital das Clínicas da Faculdade de Medicina da USP de Ribeirão Preto.
2 Livre-Docente, Professor Titular Aposentado do Departamento de Oftalmologia,Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da Faculdade de Medicina da USP de Ribeirão Preto.
3 Graduada, Técnica de laboratório do Departamento de Oftalmologia,Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da Faculdade de Medicina da USP de Ribeirão Preto.
4 Livre-Docente, Coordenador e Supervisor das Atividades Técnicas e Administrativas do Serviço de Radioterapia do Hospital das Clínicas da USP de Ribeirão Preto.
Departamento de Oftalmologia, Otorrinolaringologia e Cirurgia de Cabeça e Pescoço da Faculdade de Medicina da USP de Ribeirão Preto.
Endereço para correspondência:
Hospital das Clínicas da USP
Ribeirão Preto 12º andar
Av. dos Bandeirantes, 3900 - Campus Universitário
Monte Alegre, 14048-900, Ribeirão Preto São Paulo
E-mail: rmlessa@terra.com.br
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da BJORL em 5 de junho de 2008. cod. 5878
Artigo aceito em 6 de novembro de 2008.