Ano: 2000 Vol. 66 Ed. 6 - Novembro - Dezembro - (2º)
Seção: Artigos Originais
Páginas: 580 a 590
ACOMPANHAMENTO AUDIOLÓGICO EM PACIENTES COM OSTEOSSARCOMA SUBMETIDOS À QUIMIOTERAPIA COM CISPLATINA.
Audiological Follow Up in Patients with Osteosarcoma Who Had Chemotherapy Using Cisplatin.
Autor(es):
Andréa Dishtchekenian*,
Maria C. M. Iorio**,
Antonio S. Petrilli***,
Elias R. Paiva****,
Marisa F. Azevedo*****.
Palavras-chave: audiometria, perda auditiva de alta freqüência, cisplatina.
Keywords: audiometry, high frequency hearing loss, cisplatin
Resumo:
Introdução: A comunicação humana processa-se por meio da linguagem e da fala, e é através da audição que o homem as adquire e conserva. A deficiência auditiva é considerada doença severamente incapacitante e pode ser causada por diversos fatores, como o uso de ototóxicos. A cisplatina é um antineoplásico, utilizado com bons resultados em diversos tumores, mas apresenta alto grau de toxicidade, causando alterações renais e auditivas. Sendo assim, a monitorização dos limiares de audibilidade, especialmente nas altas freqüências, é importante durante a administração desta droga. A audiometria de altas freqüências tem sido realizada em pacientes tratados com quimioterápicos, possibilitando a detecção de alterações auditivas antes mesmo que as freqüências importantes para a compreensão da fala sejam comprometidas. Objetivo: O objetivo deste estudo foi monitorizar os limiares de audibilidade de pacientes com osteossarcoma, sem tratamento prévio, submetidos à quimioterapia com cisplatina e carboplatina. Material e método: Foram estudados os limiares de audibilidade obtidos em 27 pacientes, nos períodos pré, durante e pós-tratamento quimioterápico. Resultados: A audiometria de altas freqüências identificou mudanças nos limiares de audibilidade em 100% dos casos, na primeira avaliação audiológica realizada durante o tratamento. Em 33,3% dos casos, os limiares permaneceram normais na faixa de freqüências convencional até o término do tratamento; e em 66,6%, alterados. Conclusão: Observamos que na dose de 300 mg/m2 de cisplatina ocorrem mudanças significativas dos limiares de audibilidade, que se mantêm até o término do tratamento quimioterápico, não havendo mudanças significativas nas avaliações subseqüentes. Estes dados sugerem que a avaliação audiológica seja realizada a cada ciclo de administração de cisplatina.
Abstract:
Introduction: Human communication is based on language and speech and hearing plays a definite role in this acquisition process. Hearing loss is-considered as a severe impairment, it can have many etiologies, and ototoxicity is among them. Cisplatin is a chemotherapeutic agent used with success in various tumors. However its high level of toxicity is also known, leading to renal and hearing disorders. Therefore, evaluation of hearing thresholds, specially in high frequency range, is very important during the treatment. High frequency audiometry has been useful in determining hearing disorders before the frequency range for speech is compromised in patients undergoing chemotherapy. Aim: The aim of this study was to evaluate and monitor hearing thresholds of patients with osteosarcoma, without previous treatment, who had undergone chemotherapy using cisplatin and carboplatin. Material and metods: Hearing thresholds of 27 patients, pre, during and post chemotherapy were studied. Results: High frequency audiometry carried out during the treatment has showed changes in hearing thresholds in all cases. Hearing thresholds were within normal limits in conventional frequency range in 33,3% of the cases and 66,6% of patients had altered thresholds by the end of the treatment. Conclusion: We have observed significant changes in hearing thresholds at 300 mg/m2 dose of cisplatin, and these changes were stable throughout the treatment. These findings suggest that hearing evaluation should be performed after each stage of cisplatin administration.
![]()
INTRODUÇÃO
A comunicação humana processa-se principalmente por meio da linguagem e da fala, e é fundamentalmente através da audição que o homem as adquire e conserva.
A deficiência auditiva tem sido considerada uma doença severamente incapacitante, em virtude do papel da audição na comunicação humana. Esta pode ser causada por diversos fatores etiológicos, congênitos ou adquiridos, além de apresentar graus e tipos variáveis.
Uma das causas da deficiência auditiva adquirida é o uso de drogas ototóxicas. Essas drogas lesam as estruturas sensoriais da orelha interna, podendo afetar tanto o sistema auditivo quanto o vestibular.
Vários fatores podem influenciar no potencial da toxicidade, como o agente, a dose, a duração, a função renal, o uso prévio de outras drogas e a susceptibilidade individual.
A causa mais comum de perda auditiva permanente por drogas ototóxicas tem sido especialmente verificada com o uso de aminoglicosídeos e derivados da platina, como a cisplatina9.
A cisplatina é um agente alquilante quimioterápico antineoplásico derivado de sais inorgânicos da platina, que tem sido utilizada com bons resultados em tumores ósseos, como o osteossarcoma.
O osteossarcoma é uma neoplasia maligna primária do osso, encontrada mais freqüentemente em crianças e adolescentes. Pode ocorrer em qualquer osso ou mesmo em partes moles; mas, na maioria das vezes, acomete o úmero, a tíbia ou o fêmur.
A forma de tratamento eficaz no combate a este tumor tem sido a associação de quimioterapia e cirurgia.
Como já foi mencionado, o uso da cisplatina nestes tumores tem demonstrado atividade antitumoral eficaz em seres humanos, mas possui alto grau de toxicidade, causando efeitos indesejáveis, como alterações renais e auditivas1, 26.
Tendo em vista alterações auditivas causadas pela sua utilização, é importante a monitorização da audição em pacientes usuários de drogas ototóxicas, para determinar a progressão da ototoxicidade quando ela se inicia.
Sabe-se que, inicialmente, o dano auditivo ocorre na base da cóclea, acometendo primeiramente as altas freqüências, podendo evoluir progressivamente para o ápice, comprometendo as médias e baixas freqüências29.
Desta forma, a monitorização dos limiares de audibilidade, especialmente nas altas freqüências, é importante durante a administração da droga.
Convém ressaltar que um programa efetivo de monitorização dos efeitos tóxicos da droga na audição resultaria em detecção precoce da perda auditiva, o que possibilitaria a escolha de tratamentos alternativos3, 11.
No momento em que mudanças dos limiares de audibilidade são notadas, algumas medidas podem ser tomadas pelo médico especialista, como: a interrupção da medicação utilizada; utilização de tratamentos alternativos; redução ou mudança da dose; ou ainda a continuidade ao regime de tratamento preparando a família para prevenir uma eventual perda de audição24, 11, 21.
É importante ressaltar que a audiometria de altas freqüências tem sido considerada o método de escolha na detecção mais precoce de perda auditiva induzida por drogas ototóxicas, uma vez que possibilita a constatação de alterações auditivas antes mesmo que as freqüências mais importantes para a compreensão da fala sejam comprometidas9, 18, 14, 10, 12, 13, 8. Este procedimento inclusive, tem se revelado mais sensível do que as emissões otoacústicas4, 5, uma vez que os equipamentos atualmente disponíveis permitem o registro dos dados até 10.000 Hz. Em contraste, sabemos existirem audiômetros que permitem avaliar os limiares de audibilidade até 20.000 Hz.
Por outro lado, alguns autores mencionam que as emissões otoacústicas podem identificar mais precocemente as alterações auditivas do que a audiometria tonal na faixa de freqüências convencional, pois uma redução na amplitude das emissões pode ocorrer anteriormente às alterações dos limiares tonais25, 30, 22, 20, 17.
Trabalhos experimentais foram iniciados pelo Prof. Dr. Lazlo Stein (Comunicação Pessoal, 2000)28, na Northwestern University - Chicago - IL, utilizando altas freqüências para evocar as emissões otoacústicas, com a finalidade de monitorar a audição de pacientes submetidos à quimioterapia. Concordando com a utilização da audiometria de altas freqüências como um procedimento efetivo na avaliação dos efeitos ototóxicos, a American Speech-Language-Hearing Association (ASHA), em 19941, padronizou um protocolo recomendando alguns procedimentos para monitorar a audição de pacientes que realizam tratamento com drogas ototóxicas. Segundo a ASNA (1994)1, primeiramente é realizada a anamnese, seguida da otoscopia; e, posteriormente, da avaliação audiológica constituída por: audiometria tonal liminar (faixa de freqüências convencional); audiometria de altas freqüências (acima de 8.000 Hz); logoaudiometria e medidas de imitância acústica. Geralmente, a logoaudiometria e as medidas da imitância acústica são obtidas na primeira avaliação, mas não necessariamente retestadas nas avaliações subseqüentes, a menos que mudanças dos limiares de audibilidade sejam notadas. Caso o paciente esteja impossibilitado de responder aos testes audiológicos subjetivos, medidas objetivas podem ser realizadas, como a audiometria de tronco cerebral e as emissões otoacústicas.
A partir destes pressupostos, realizamos um estudo cujo objetivo foi monitorar os limiares de audibilidade de pacientes com diagnóstico de osteossarcoma submetido à quimioterapia, sem tratamento prévio.
MATERIAL E MÉTODO
O material deste estudo foi constituído pelos limiares de audibilidade obtidos em 27 pacientes (54 orelhas) com diagnóstico de osteossarcoma, sem tratamento prévio, submetidos à quimioterapia com cisplatina, carboplatina e outras drogas associadas. Os pacientes foram encaminhados pelo Setor de Oncologia Pediátrica do Departamento de Pediatria da Universidade Federal de São Paulo - Escola Paulista de Medicina, ao Ambulatório da Disciplina de Distúrbios da Audição da Universidade Federal de São Paulo - Escola Paulista de Medicina.
Dos 27 pacientes avaliados, 19 eram do sexo masculino; e oito, do feminino - na faixa etária de 11 a 20 anos.
Todos os pacientes foram submetidos a anamnese, com a finalidade de obter informações pregressas e atuais relacionadas à audição. Os pacientes com queixas pregressas de alteração auditiva foram excluídos deste estudo.
A seguir, foi realizada a otoscopia, a fim de investigar a presença de cerume excessivo, corpos estranhos, ou algum sinal de infecção que pudesse comprometer a realização da avaliação audiológica.
A avaliação audiológica constituiu de: audiometria tonal liminar na faixa de freqüências convencional (250 a 8.000 Hz); audiometria de altas freqüências (9.000 a 18.000 Hz); logoaudiometria, sendo realizada a pesquisa do limiar de reconhecimento de fala e o índice percentual de reconhecimento de fala, em cabina acústica; medidas da imitância acústica: timpanometria e pesquisa dos reflexos acústicos, no modo contra e ipsilateral, como uma forma de avaliação clínica utilizada para descartar qualquer alteração de orelha média.
Para a realização da audiometria tonal liminar convencional e logoaudiometria foi utilizado o audiômetro da marca Maico, modelo MA-412, com fones TDH-39 e coxim MX-41z. Para a audiometria de altas freqüências foi utilizado o audiômetro da marca Interacoustics, modelo AS 10 HF e fones KOSS HV-1A, com limiares de audibilidade expressos em dB NPS (decibel Nível de Pressão Sonora).
Para a realização das medidas da imitância acústica, foi utilizado o analisador de orelha média da marca Interacoustics, modelo AZ-7.
Todos os pacientes realizaram o mesmo protocolo de tratamento quimioterápico, que consistiu de nove ciclos de quimioterapia, com intervalos de 21 dias entre um ciclo e outro. No período pré-operatória (semana zero, três e seis) os pacientes receberam três doses de 100 mg/m2 de cisplatina (total de 300 mg2), 500 mg/m2 de carboplatina (total de 1.500 mg/m2) e 70 mg/m2 de doxorrubicina (total de 210 mg/m2). No período pós-operatório, foram administradas mais duas doses de 100 mg/m2 de cisplatina (semanas 11 e 20, total de - 200 mg/m2), duas doses de 500 mg/m2 de carboplatina (semanas 17 e 26, total de 1.000 mg/m2), três doses de 70 mg/m2 de doxorrubicina (semanas 14, 17 e 23, total de 210 mg/m2) e cinco doses de 9 g/m2 de ifosfamida/mesna (semanas 11, 14, 20, 23 e 26, total de 45 g/m2). Conforme pode ser observado no esquema abaixo, a cisplatina foi administrada na dose de 100 mg/m2 em cinco dos nove ciclos de tratamento.
Esquema do tratamento quimioterápico:
S = semana de tratamento.
A dose total das drogas utilizadas no tratamento quimioterápico foi:
Quadr. - Cisplatina 100 mg/m2 X 5 = 500 mg/m2
Trian. - Carboplatina 500 mg/m2 X 5 = 2.500 mg/m2
Circu. - Doxorrubicina 70 mg/m2 X 6 = 420 mg/m2
Losan. - Ifosfamida 9 g/m2 X 5 = 45 g/m2
Setac. - Mesna 9 g/m2 X 5 = 45 g/m2
De acordo com o protocolo proposto, foram realizadas quatro avaliações audiológicas, uma avaliação audiológica no período pré, duas durante o tratamento (após as semanas 6 e 17) e uma no pós-tratamento quimioterápico.
Para o estudo dos limiares de audibilidade, foi utilizada a mesma referência em todas as freqüências estudadas, sendo que os valores obtidos em dB NA (decibel Nível de Audição), limiares das freqüências de 250 a 8.000 Hz, foram transformados em dB NPS, segundo os valores determinados pelo padrão ANSI-692.
Valores propostos pela Norma ANSI-692 para o 0 dB NA:
250 500 1.000 2.000 3.000 4.000 6.000 8.000 Hz
25,5 11,5 7,5 9,5 10,0 9,5 15,0 13,0 dBNPS
Para a análise estatística dos resultados, foram utilizados testes não paramétricos, levando-se em consideração a natureza das variáveis estudadas.
Para a avaliação de possíveis diferenças entre os limiares obtidos por freqüência testada nos períodos estudados, para cada freqüência dentro de cada grupo utilizou-se o teste não paramétrico para K amostras não independentes de Friedman27, complementado pelo teste de comparações múltiplas16.
Em todos os testes, fixou-se em 0,05 ou 5% o nível para a rejeição da hipótese de nulidade, assinalando-se com asterisco os valores significantes.
RESULTADOS E DISCUSSÃO
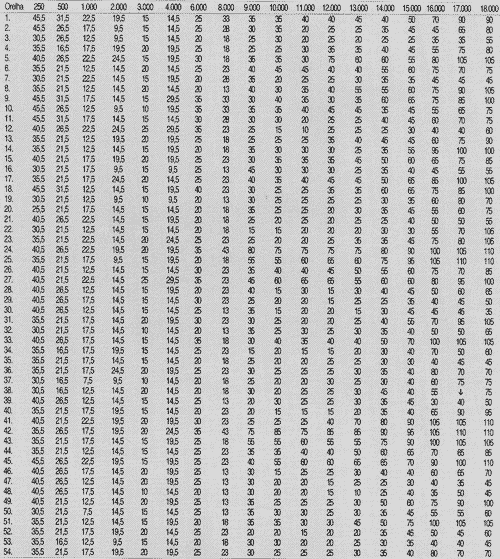
Foi realizado inicialmente o levantamento dos limiares de audibilidade obtidos nos 27 pacientes - 54 orelhas, na faixa de freqüências de 250 a 18.000 Hz, nos períodos pré, semana 6 e semana 17 e no pós-tratamento quimioterápico, conforme pode ser verificado nas Tabelas 1, 2, 3 e 4.TABELA 1 - Limiares de audibilidade (dB NPS) obtidos na faixa de freqüências de 250 a 18.000 Hz, por orelha testada, no período pré-tratamento quimioterápico.
?= ausência de resposta
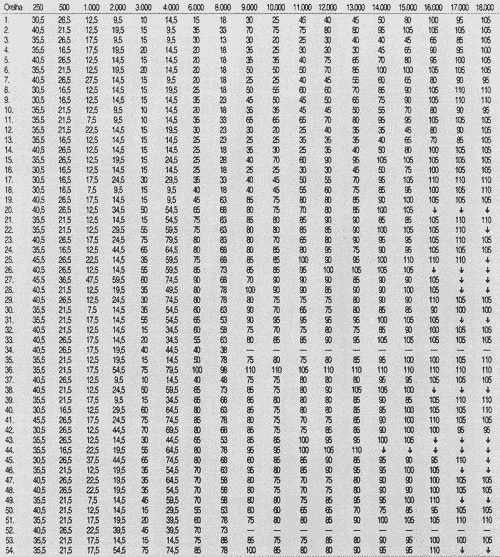
TABELA 2 - Limiares de audibilidade (d BNPS) obtidos na faixa de freqüências de 250 a 18.000 Hz, por orelha testada, na semana 6.
- = não foi realizada ?= ausência de resposta
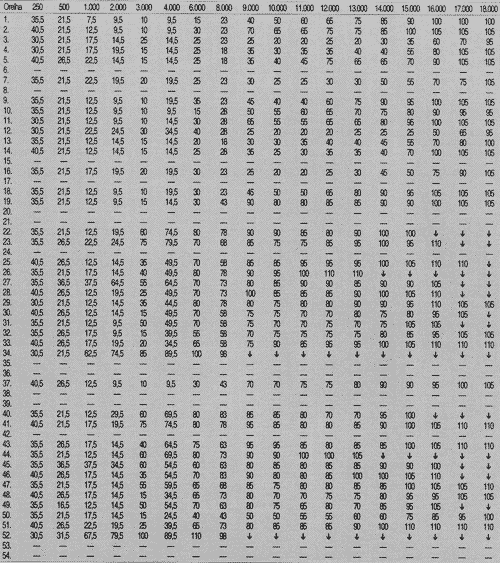
TABELA 3 - Limiares de audibilidade (dB NPS) obtidos na faixa de freqüências de 250 a 18.000 Hz, por orelha testada, na semana 17.
- = não foi realizada ?= ausência de resposta
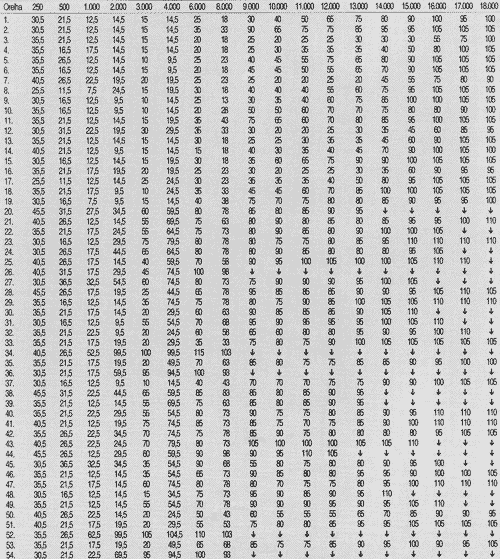
TABELA 4 - Limiares de audibilidade (dB NPS) obtidos na faixa de freqüências de 250 a 18.000 Hz, por orelha testada, no período pós-tratamento quimioterápico.
?= ausência de resposta
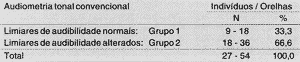
TABELA 5 - Indivíduos e respectivas orelhas segundo a audiometria tonal convencional.
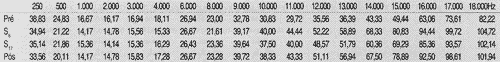
TABELA 6 - Valores médios dos limiares de audibilidade (dB NPS), obtidos na faixa de freqüências de 250 a 18.000 Hz, por orelha testada, no Grupo 1, nos períodos pré, S6, S17 e pós-tratamento quimioterápico.
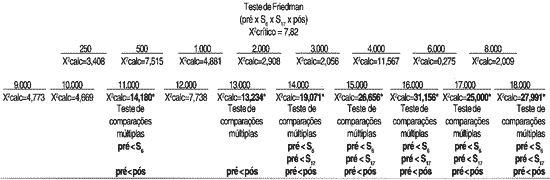
X2 calc = X2 calculado
Teste de Friedman
Verificou-se que nove pacientes - 18 orelhas (33,3%), apresentaram limiares de audibilidade normais na faixa de freqüências convencional até o término do tratamento; e 18 pacientes - 36 orelhas (66,6%) apresentaram alteração dos limiares de audibilidade na faixa de freqüências convencional, durante o tratamento quimioterápico. Desta forma, a amostra foi dividida em dois grupos: Grupo 1, pacientes que apresentaram limiares de audibilidade normais na faixa de freqüências de 250 a 8.000 Hz após o término do tratamento quimioterápico, isto é, limiares não superiores a 25 dB NA'; e Grupo 2, pacientes que apresentaram limiares de audibilidade alterados na faixa de freqüências convencional após o final do tratamento quimioterápico (Tabela 5). Tal dado demonstra que a alteração auditiva pode variar de um paciente para outro, devido à susceptibilidade individual. -Este fato também é referido por Aguilar-Markulis1 e Brock6.
As Tabelas 6 e 7 mostram as médias dos limiares de audibilidade (dB NPS), obtidos em cada freqüência testada (Hz), nos períodos pré, semana 6, semana 17 e pós-tratamento quimioterápico, nos Grupos 1 e 2, respectivamente.
Pode se observar que houve um predomínio de acometimento de perda auditiva neurossensorìal, bilateral e simétrica, com predomínio nas altas freqüências, tanto no Grupo 1, quanto no 2, conforme mostram as Figuras 1 e 2. O acometimento auditivo bilateral e simétrico acompanhado de perda auditiva nas altas freqüências também é descrito por Aguilar-Markulis1 e Fausti9, 11.TABELA 7 - Valores médios dos limiares de audibilidade (dB NPS), obtidos na faixa de freqüências de 250 a 18.000 Hz, por orelha testada, no Grupo 2, nos períodos pré, S6, S17 e pós-tratamento quimioterápico.
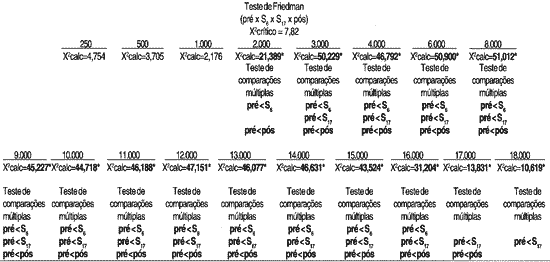
X2 calc = X2 calculado
Teste de Friedman
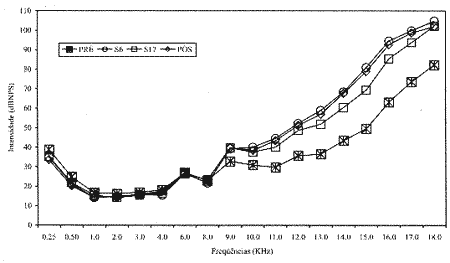
Figura 1. Valores médios dos limiares de audibilidade (dB NPS), obtidos na faixa de freqüências de 0,25 a 18,0 KHz, por orelha testada, no Grupo 1, nos períodos pré, S6, S17 e pós-tratamento quimioterápico.
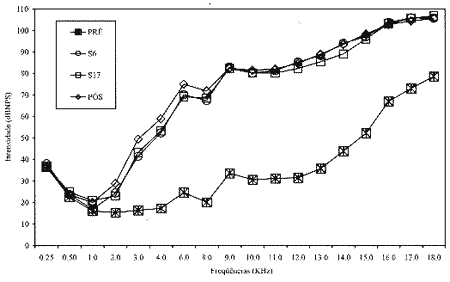
Figura 2. Valores médios dos limiares de audibilidade (dB NPS), obtidos na faixa de freqüências de 0,25 a 18,0 KHz, por orelha testada, no Grupo 2, nos períodos pré, S6, S17 e pós-tratamento quimioterápico.
A audiometria de altas freqüências identificou mudanças nos limiares de audibilidade em 100% dos casos já na primeira avaliação audiológica realizada durante o tratamento quimioterápico, na dose de 300 mg/m2 de cisplatina. Há uma concordância entre alguns estudos mostrando que mudanças dos limiares de audibilidade ocorrem primeiramente nas altas freqüências e a partir de uma dose alta de cisplatina, superior a 300mg/m2 18, 19, 11, 23.
No Grupo 1, observou-se que as alterações auditivas ocorreram a partir da freqüência de 11.000 Hz não havendo mudanças significativas dos limiares de audibilidade nas avaliações subseqüentes. No Grupo 2, as alterações ocorreram a partir da freqüência de 2.000 Hz, com variação de até 70 dB, entre os limiares de audibilidade, sendo estas mais observadas entre 3.000 e 18.000 Hz. Park23 também não verificou mudanças significativas dos limiares de audibilidade nas freqüências de 250 a 2.000 Hz, mesmo após a dose total de cisplatina utilizada.
O início das alterações auditivas predominou na semana 6, isto é, após a administração de 300 mg/m2 de cisplatina, não tendo sido verificadas diferenças estatisticamente significativas entre os limiares obtidos após a primeira avaliação durante o tratamento e as demais. Houve uma tendência à estabilização dos limiares de audibilidade, mesmo com o aumento da dose da cisplatina, concordando com os achados de Park23. Este efeito foi denominado "fenômeno de platô"18, ou seja, a partir de determinadas doses, não haveria piora dos limiares de audibilidade. Este fenômeno foi verificado por Skinner26 na dose de 600 mg/m2 de cisplatina.
Não foi realizada, no entanto, a avaliação audiológica dos pacientes entre os três primeiros ciclos de quimioterapia (S0, S3 e S6), tendo se verificado aí a maior concentração da cisplatina. Tal fato, não permitiu verificar em qual ciclo ocorreu a instalação inicial das alterações auditivas. Outros autores, porém, atribuem maior efeito ototóxico em doses mais altas, acima de 100 mg/m2 e doses cumulativas elevadas15, 29, 6.
CONCLUSÕES
O tratamento quimioterápico proposto por este protocolo leva à perda auditiva neurossensorial, bilateral e simétrica, predominantemente nas altas freqüências.
Em 33,3% dos casos induz perda auditiva somente nas altas freqüências.
Em 66,6% dos casos provoca perda auditiva que inicia-se na faixa de freqüências convencional.
Na dose de 300 mg/m2 de cisplatina ocorrem mudanças significativas dos limiares de audibilidade, que se mantêm até o término do tratamento quimioterápico, não havendo mudanças significativas nas avaliações subseqüentes.
Estes dados sugerem que a avaliação audiológica seja realizada entre os três primeiros ciclos de 100 mg/m2 de cisplatina (S0, S3 e S6).
REFERÊNCIAS BIBLIOGRÁFICAS
1. AGUILAR-MARKULIS, N. V.; BECKLEY, S.; PRIORE, R.; METTLIN, C. - Auditory toxicity effects of long-term cisdichlorodiammineplatinum II therapy in genitourinary cancer patients. J. Surg. Oncol., 16: 111-23, 1981.
2. AMERICAN NATIONAL STANDARD INSTITUTE - American National Standards Specification for audiometers. American Standard S3.6-1969. New York, 1969.
3. AMERICAN SPEECH-LANGUAGE-HEARING ASSOCIATION - Guidelines for the audiologic management of individuals receiving cochleotoxic drug therapy. ASHA, 36: 11-19, 1994.
4. BENSADON, R. L. - Estudo clínico da olotoxicidade da cisplatina: comparação entre os exames de audiometria tonal convencional, audiometria de altas freqüências e emissões otoacústicas. São Paulo, 1999. [Tese de Doutorado - Universidade de São Paulo] 100p. -
5. BERG, A. L.; SPITZER, J. B.; GARVINJ. H. Jr. - Ototoxic impact of cisplatin in pediatric oncology patients. Laryngoscope, 109: 1806-14, 1999.
6. BROCK, P.; BELLMAN, S.; YEOMANS, E. C.; PINKERTON, C. R.; PRITCHARD, J. - Ototoxicity of high dose cisplatinum in children: a practical grading system. Med. Pediatr. Oncol., 19:295-300, 1991.
7. DAVIS, H. & SILVERMAN, S. R. - Hearing and deafness. 3.ed., New York, Rinehart & Winston, 1970. 522p.
8. DISHTCHEKENIAN, A.; KECHICHIAN, R.; PETRILLI, A. S.; AZEVEDO, M. F.; IORIO, M. C. M. - A study of the hearing of osteosarcoma patients treated with carboplatin and cisplatin chemotherapy. In: CONGRESSO DA ACADEMIA AMERICANA DE AUDIOLOGIA, X. Los Angeles, 1998. Anais. Los Angeles, 1998.
9. FAUSTI, S. A.; SCHECHTER, M. A.; RAPPAPORT, B. Z.; FREY, R. H.; MASS, R. E. - Early detection of cisplatin ototoxicity. Cancer, 53: 224-31, 1984.
10. FAUSTI, S. A.; FREY, R. H.; HENRY, J. A.; OLSON, D. J.; SCHAFFER, H. I. - High-frequency testing techniques and instrumentation for early detection of ototoxicity. J. Rehab. Res. Dev., 30(3): 333-41, 1993a.
11. FAUSTI, S. A.; HENRY, J. A.; SCHAFFER, H. I.; OLSON, D. J.; FREY, R. H.; BAGBY Jr., G. C. - High frequency monitoring for early detection of cisplatin ototoxicity. Arch. Otolaryngol. Head Neck Surg., 119: 661-6, 1993b.
12. FAUSTI, S. A.; LARSON, V. D., NOFFSINGER, D., WILSON, R. H., PHILLIPS, D. S.; FOWLER, C. G. - High-frequency audiometric monitoring strategies for early detection monitoring of ototoxicity. Ear Hear., 15: 232-39, 1994.
13. FAUSTI, S. A.; HENRY, J. A.; HAYDEN, D.; PHILLIPS, D, S.; FREY, R. H. - Intrasubject reliability of high-frequency (9-14kHz) thresholds: tested separately vs, following conventional frequency testing. J. Am. Acad. Audiol., 9: 147-52, 1998.
14. FRANK, R. & DREISBACH, L. E. - Repeatability of high frequency thresholds. Ear Hear, 12: 294-95, 1991.
15. HALL, 1).J.; DIASIO, R. & GOPLERUD, D. R. - Cis-platinum in gynecologic cancer. Am. J. Obstet. Gynecol., 141: 309-12, 1981.
16. HOLANDER, M. & WOLFE, D. A. - Nonparametric statistical methods. New York, John Wiley & Sons. 1973. 503p.
17. KASHIVIAMURA, M. - Studies of the evaluation of cochlea function with distortion product otacoustic emission. Hokkaido Igaku Zasshi, 73: 641-62, 1998.
18. KOPELMAN, J.; BUDNICK, A. S.; SESSIONS, R. B.; KRAMER, M. B.; WONG, G. Y. - Ototoxicity of high-dose cisplatin by bolus administration in patients with advanced cancers and normal hearing. Laryngoscope, 98:858-64, 1988.
19. KRETSCHMARN, C. S.; WARREN, M. P.; LAVALLY, B. L.; DYER, S.; TARBELL, N. J. - Ototoxicity of preradiation cisplatin for children with central nervous system tumors. J. Clin. Oncol, 8:1191-8, 1990.
20. LITTMAN, T. A.; MAGRUDER, A. & STROTHER, D. R. - Monitoring and predicting ototoxic damage using distortion-product otoacoustic emissions: pediatric case study. J Am. Acad. Audiol, 9: 257-62, 1998.
21. MENCHER, G. T.; NOVOTNY, G.; MENCHER, L.; GULLIVER, M.-Ototoxicity and irradiation: additional etiologies of hearing loss in adults. J. Am. Acad. Audiol, 6-351-57, 1995.
22. OZTURAN, O.; JERGER, J.; LEW,11.; LYNCH, G. R. -Monitoring of cisplatin ototoxicity by distortion-product otoacoustic emissions. Auris Nasus Larynx, 23: 147-51, 1996.
23. PARK, K. R. - The utility of acoustic reflex thresholds and other conventional audiologic tests for monitoring cisplatin ototoxicity in the pediatric population. Ear Hear., 17 107-15, 1996.
24. PASIC, T. R. & 13OBIE, R. A. - Cis-platinum ototoxicity in children. Laryngoscope, 101: 985-91, 1991.
25. PROBST, R.; HARRIS, F. P. & HAUSER, R. - Clinical monitoring using otoacoustic emissions. Br. J. Audiol, 27- 85-90, 1993.
26. SKINNER, R.; PEARSON, A. D. J.; AMINEDDINE, H. A.; MAMAS, D. B.; CRAFT, A. W. - Ototoxicity of cisplatinum in children and adolescents. Br. J. Cancer, 61: 927-30, 1990.
27. SIEGEL, S. - Estatística não paramétrica. Mexico, Trillas. 1975. 346p.
28. STEIN, L. - Comunicação pessoal. Northwestern University - Chicago - IL, 2000.
29. STUART, N. S. A.; WOODROFFE, C. M.; GRUNDY, R.; CULLEN, M. H. - Long-term toxicity of chemotherapy for testicular cancer - the cost of cure. Br J. Cancer, 61: 479-84, 1990.
30. ZOROWKA, P. G.; SCHMITT, H. J. & GUTJAHR, P. - Evoked otoacoustic emissions and pure tone threshold audiometry in patients receiving cisplatinum therapy. Int. J. Pediatr. Otorhinolaryngol., 25: 73-80, 1993.
* Mestre em Distúrbios da Comunicação Humana - Campo Fonoaudiológico, pela Universidade Federal de São Paulo - Escola Paulista de Medicina.
** Professora Adjunta, Doutora, Chefe da Disciplina de Distúrbios da Audição do Departamento de Otorrinolaringologia e Distúrbios cia Comunicação Humana, Universidade Federal de São Paulo - Escola Paulista de Medicina.
*** Professor, Doutor, Chefe do Setor de Oncologia Pediátrica do Departamento de Pediatria da Universidade Federal de São Paulo - Escola Paulista de Medicina.
**** Professor Adjunto (Aposentado) do Departamento de Medicina Preventiva da Universidade Federal de São Pauto - Escola Paulista de Medicina.
***** Professora Adjunta, Doutora, do Departamento de Otorrinolaringologia e Distúrbios da Comunicação Humana, da Universidade Federal de São Paulo - Escola Paulista de Medicina.
Instituição: Disciplina dos Distúrbios da Audição, da Universidade Federal de São Paulo - Escola Paulista de Medicina.
Trabalho apresentado no XI Congresso da Academia Americana de Audiologia, no dia 30 de abril de 1999, em Miami - Estados Unidos da América.
Endereço para correspondência: Andréa Dishtchekenian - Rua do Acre, 729 - 03181-1000 São Paulo/ SP - Telefone: (0xx11) 6604-2165 - E-mail: andreadi@terra.com.br
Artigo recebido em 16 de outubro de 1999. Artigo aceito em 13 de julho de 2000.